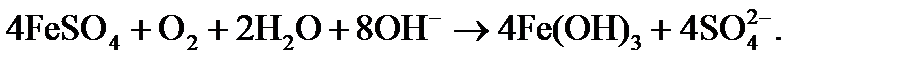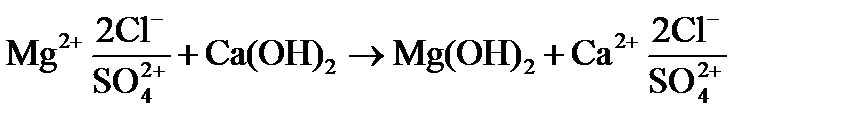Известь и вода уравнение реакции
В строительстве также негашеную известь. Известь в виде молотой кипелки используется в известково-гипсовых, известково-шлаковых и известково-глиняных составах для штукатурки, а также для изготовления искусственных безобжиговых камней и смешанных вяжущих веществ (нзвестково-шлакового и др.)
С применением молотой кипелки схватывание, твердение и высыхание материала ускоряется.
При правильном подборе соотношения: между водой и известью — водоизвесткового отношения (обычно в пределах 0,9 —1,5) — тонкомолотый, порошок извести-кипелки в смеси с песком или шлаком быстро схватывается (подобно гипсу) и затем твердеет. При этом никаких трещин от гашения извести не образуется.
Саморазогревание материала ускоряет твердение, что особенно важно в холодное время и при зимних работах, например штукатурных. Способ И. В. Смирнова имеет еще и то преимущество, что при нем не получается никаких отходов: известь целиком размалывается и используется. Таким образом, из вещества, медленно схватывающегося и твердеющего, известь превратилась в быстро схватывающееся и твердеющее вещество.
Формула гашения извести
Реакция гашения извести экзотермична, т. е. происходит с выделением тепла: на 1 грамм-молекулу (40 + 16 = 56 г) СаО выделяется 15,5 ккал тепла. Происходящую здесь термохимическую реакцию можно выразить следующим образом:
СаО + Н2О = Са(ОН)3 + 15,5 ккал.
В зависимости от температуры гашения комовая известь разделяется по ГОСТ на:
- а)низкоэкзотермическую — с температурой гашения ниже 70°;
- б)высокоэкзотермическую — с температурой гашения свыше 70°.
Вследствие выделения тепла известь во время гашения разогревается, особенно тогда, когда гашение ведут в закрытом аппарате или с небольшим количеством воды. При открытом гашении часть воды испаряется, поэтому в данном случае нужно значительно больше воды, чем по приведенной выше реакции.
Известь-кипелка начинает гаситься под действием атмосферной влаги уже при хранении на складе. Гашение происходит с поверхности; образовавшийся слой гашеной извести начинает карбонизироваться, теряя вяжущие свойства; поэтому в строительстве следует применять свежеобожженную известь. Известь можно гасить в порошок, называемый пушонкой, или в известковое тесто.
Гасить известь в пушонку необходимо в закрытом аппарате, так как при этом тепловая энергия и водяные пары полностью используются для превращения извести в тончайший порошок (тоньше обычного цемента). Такое гашение производится в специальных машинах гидраторах непрерывного действия (цилиндрические барабаны с лопастями) или в барабанах под давлением пара.
При гашении извести в пушонку объем ее значительно увеличивается. Чистая (так. называемая жирная ) известь увеличивается в объеме в 3 — 3,5 раза, тощая известь, т. е. содер жащая негасящиеся примеси, в 1,5—2 раза. Это явление объясняется разрыхлением порошка. Удельный вес гашеной извести 2,1. Объемный вес пушонки в рыхлом состоянии 400 — 450 кг[м3.
На стройках часто гасят известь прямо в известковое тесто. Для этого берут воды значительно больше, чем при гашении в пушонку. В результате образуется густое пластичное тесто. После, отстаивания оно содержит около 50 % гашеной извести — гидрата окиси кальция Са(ОН)2 и 50% воды (по весу). Объемный вес обычного известкового теста 1400 кг/м3.
Простейший способ гашения извести
Простейший способ гашения извести на малых стройках— в творилах и ямах. В земле выкапывают яму, стенки и дно которой обшивают досками, чтобы известь не загрязнялась. Рядом с ямой на земле ставят деревянный ящик (творило), имеющий сбоку отверстие, закрытое крупной сеткой с отверстиями в 3 мм. В этот ящик загружают куски негашеной извести, перемешивают ее с водой и таким образом гасят известь в молоко. Воду добавляют к извести медленно, постепенно, не допуская ее охлаждения.
По окончании гашения полученное жидкое известковое молоко пропускают через сетку в творильную яму. Сетка задерживает нё погасившиеся куски, которые можно использовать после размола; более мелкие не погасившиеся куски проходят сквозь сетку и должны будут догаситься в яме. Для полного гашения необходимо продержать известковое тесто в яме не менее двух недель. Длительное хранение известкового теста в яме под слоем воды безвредно, так как воздушная известь в таких условиях не затвердевает.
Чтобы ускорить гашение, комовую известь предварительно размалывают или применяют механизированное гашение, пропуская известь вместе с водой через молотковую дробилку, бегуны или специальные известегасильные машины, где известь гасится в молоко или тесто. В известе-гасилке Заячковского известь одновременно гасится, размалывается и перемешивается катками; при этом ускоряется гашение и не остает отходов. Для получения известкового теста известковому молоку дают отстояться в специальном отстойнике. Производительность мащины не менее 25 г извести в смену. Обработка извести в смену в этой известе-гасилке повышает активность извести и пластичность изгесткового теста. Иногда для уокорения гашения применяют подогретую воду постоянной температуры. После тщательного гашения достаточно выдержать известковое тесто в отстойнике в течение всего 1—2 суток.
На крупных стройках и на известковых заводах имеются специальные установки, снабжающие стройки высококачественным известковым тестом, пушонкой, молотой кипелкой, карбонатной известью (содержащей 50 % извести-кипелки и 50% молотого известняка) или готовыми известково-пеечаными, известково-шлаковым и и другими растворами.
Известь и вода уравнение реакции
Курс общей и неорганической химии
(для студентов биологического факультета (биофизиков)
и для студентов факультета биоинженерии и биоинформатики)
Программа курса. Материалы лекций. Презентации лекций. Программа сетевых контрольных мероприятий
Лектор — Загорский Вячеслав Викторович — ст.н.сотр., к.х.н., д.п.н.
Гашение извести
(реакция оксида кальция с водой)
Посмотреть видео:
Гашение извести — реакция взаимодействия оксида кальция [CaO] с водой [H 2 O]. Типичная реакция между основным оксидом щелочноземельного металла и воды. Продукт реакции — соответствующая щелочь. В данном случае гидроксид кальция [Ca(OH) 2 ].
В фарфоровую чашку поместили заранее приготовленную прокаливанием мела негашеную известь. При помощи пипетки прикапали в чашку несколько капель воды. В ходе реакции образовался рыхлый гидроксид кальция [Ca(OH) 2 ].
Автор и оператор
Загорский В.В.
Ассистент
Петрова Е.П.
Подготовка публикации
Мочалыгин А.Г.
Редактирование
Миняйлов В.В.


Сервер создается при поддержке Российского фонда фундаментальных исследований
Не разрешается копирование материалов и размещение на других Web-сайтах
Вебдизайн: Copyright (C) И. Миняйлова и В. Миняйлов
Copyright (C) Химический факультет МГУ
Написать письмо редактору
ИЗВЕСТКОВАНИЕ ВОДЫ
Известкование производится при обработке исходной воды в осветлителях суспензией гашеной извести Са(ОН)2, называемой известковым молоком. Основное назначение известкования – снижение щелочности обрабатываемой воды. При этом происходит частичное снижение общей жесткости воды, солесодержания, кремнийсодержания, концентрации соединений железа и одновременно из воды удаляются грубодисперсные примеси.
Сущность процесса известкования состоит в том, что при вводе извести достигается повышение рН обрабатываемой воды до значения 9,5 – 10,3, при котором бикарбонаты 
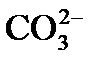
В упрощенном виде при известковании протекают следующие реакции:
1) при вводе извести происходит её диссоциация, приводящая к повышению рН:
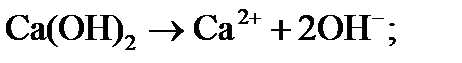
2) в воде появляются ионы ОН — , которые связывают свободную углекислоту с последующей диссоциацией по схеме:
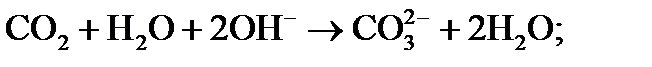
3) происходит диссоциация гидрокарбонатных ионов (бикарбонатов), определяющих щелочность воды:
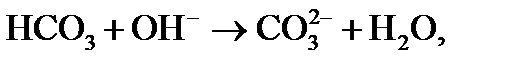
причем по реакции (3) из одного одновалентного иона 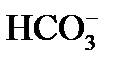
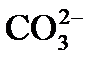
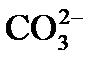
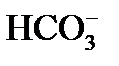
4) выделение в осадок почти нерастворимого СаСО3 происходит при достижении произведения растворимости по карбонату кальция, так как в воде есть кальций, содержащийся в исходной воде, введенный с известью, и вновь образованные карбонаты:
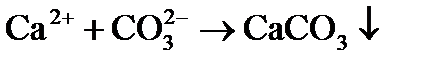
5) при превышении дозы извести над её количеством, необходимым для образования карбонатов в воде, появляется избыток ионов ОН — и может быть превышено произведение растворимости по 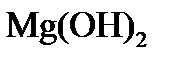

Подсчитаем дозу извести, необходимую для декабонизации, снижения щелочности и переведения ионов Mg 2+ в 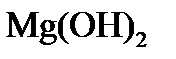
1) для переведения 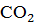
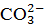
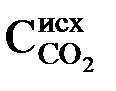
2) для перевода бикарбонатных ионов в карбонатные – в количестве, эквивалентном исходной концентрации 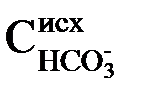
3) для переведения ионов Mg 2+ в 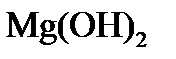

Таким образом, ионы 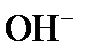
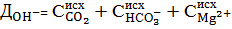
Одновременно с известью вводятся ионы кальция.
Реакции, протекающие при известковании обратимы, поэтому для их смещения в нужном направлении приходится вводить некоторый избыток Са(ОН)2 в количестве 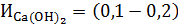
Поэтому практическая доза извести с учетом избытка равна
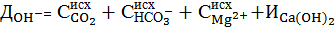
При совмещении процессов известкования и коагуляции в качестве коагулянта используют обычно сульфат двухвалентного железа в дозировке Дк. На образование гидроксида железа при известковании требуется дополнительный расход извести как источника гидроксид-ионов, что должно учитываться при расчете дозы извести согласно реакции
Тогда в формуле (7) следует учесть дозу коагулянта в виде:
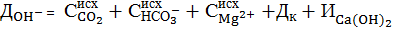
При расчете дозы извести необходимо учитывать ионный состав обрабатываемой воды. Для практического использования расчетная доза извести Ди, мг-экв/дм 3 , определяется для большинства типов вод, для которых 
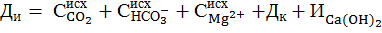
Приведенные реакции (1-9) позволяют определить требуемую дозу извести в процессе известкования с дополнительным осаждением магния. Этот режим называется гидратным и происходит при рН = 10,0 – 10,3.
Формула (9) учитывает расход извести на осаждение магния, но во многих случаях осаждение магния не обязательно.
Режим, в котором осаждение магния не происходит или происходит не полностью, называется карбонатным. В этом случае выделяется, главным образом, СаСО3 при рН = 9,5. Возможны два случая ведения этого режима.
Для вод, имеющих отношение 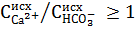
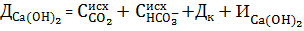
Контроль режима известкования ведется по значению концентрации кальция в известкованной воде, которая должна быть примерно равна:
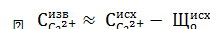
где 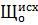
Для вод, имеющих отношение 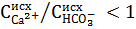
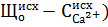
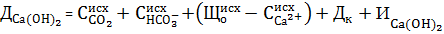
В карбонатном режиме шлам имеет структуру песка, быстро оседает, но столб жидкости над границей раздела осветляется плохо.
В промышленных условиях вести строгий режим дозирования извести, обеспечивающий отсутствие гидратной щелочности, практически невозможно. Поэтому обычно процесс известкования проводят в гидратном режиме с остаточной гидратной щелочностью, равной 0,1 – 0,3 мг-экв/дм 3 (формула 8). В гидратном режиме образуется шлам, имеющий однородную творожную структуру с крупными хорошо осаждающимися хлопьями. К преимуществам гидратного режима известкования относится также то, что присутствие гидроксида магния в осадке способствует снижению кремнийсодержания на 25 – 30 % за счет адсорбции ионов 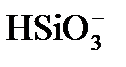
Передозировка извести по отношению к доле выделенного магния Mg 2+ при гидратном режиме не сопровождается снижением жесткости и щелочности, а вызывает замену некарбонатной магниевой жесткости на кальциевую по реакции
К моменту прохождения всех стадий известкования остаточная карбонатная щелочность (т.е. сумма 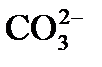
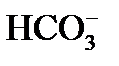
Ухудшение реальных результатов по щелочности, концентрациям ионов Са 2+ (на 0,15 – 0,3 мг-экв/дм 3 ) и Mg 2+ (на 0,1 – 0,15 мг-экв/дм 3 ) в процессе известкования по сравнению с равновесными их значениями связывают с влиянием кинетических факторов: достаточно медленной кристаллизацией образующейся твердой фазы СаСО3 и Mg(OH)2 при приближении системы к состоянию равновесия и «тормозящей» роли органических примесей (защитных коллоидов) исходной воды, а также с выносом из осветлителя микрокристаллов твердой фазы.
6. Лабораторная работа № 1
М е т о д и к а п р о в е д е н и я р а б о т ы и о б р а б о т к а
р е з у л ь т а т о в о п ы т о в
Работа выполняется в следующей последовательности:
а) выполняются анализы исходной воды согласно методикам аналитического контроля, приведенным в прил. 1: необходимо определить окисляемость, общую жесткость и общую щелочность;
сначала проводят анализ окисляемости, для чего ставят кипятить пробу с исходной водой в термостойкой колбе с добавленными в неё реактивами, засекают время с момента закипания;
пока кипятится проба на окисляемость, проводят анализы исходной воды на общую жесткость и щелочность;
затем заканчивают анализ окисляемости согласно методике;
аналогично выполняется анализ окисляемости для контрольной пробы с дистиллятом;
б) для проведения процесса коагуляции в коническую колбу емкостью 750 мл отбирают 500 мл исходной воды и нагревают её до 40 о С, контролируя температуру нагрева воды лабораторным термометром; по указанию преподавателя корректируют значение рН, добавляя в исходную подогретую воду 0,1 н раствор НCl или 0,1 н раствор NaOH из бюреток в заданном количестве;
в) проводят процесс коагуляции, для чего в воду добавляют дозу коагулянта, указанную преподавателем (1% раствор Al2(SO4)3 или FeSO4); содержимое колбы осторожно перемешивают 5 – 8 минут, затем оставляют в покое в течение 15 — 25 минут;
г) фильтруют коагулированную воду через бумажный фильтр, уложенный в воронку, осторожно сливая отстоявшуюся прозрачную жидкость; к концу фильтрования переносят на фильтр осадок;
д) проводят в коагулированной воде определение окисляемости, общей жесткости и общей щелочности;
е) результаты анализов заносят в отчет.
С о д е р ж а н и е о т ч е т а
Отчет по работе должен содержать:
— описание процесса коагуляции;
— описание условий проведения коагуляции (корректировка рН, доза и тип коагулянта);
— рабочие записи при выполнении анализов воды, в которых указывается методика определения, реактивы, используемые для анализа, расчет результатов титрования;
— результаты анализов оформляются в виде табл. 1;
— выводы, поясняющие эффективность процесса коагуляции;
— ответы на контрольные вопросы.
Таблица 1. Результаты измерений
| Исследуемая вода | Окисляемость | рН | Щелочность, мг-экв/дм 3 | Жесткость, мг-экв/дм 3 |
| мг О2/дм 3 | % сни- жения | Общая | Некарбо- натная | |
| Исходная | ||||
| После коагуляции |
Некарбонатную жесткость вычисляют по формуле: Жнк=Жо – Жк; карбонатную жесткость Жк принимают равной бикарбонатной щелочности, определенной в результате анализов исходной и коагулированной воды.
К о н т р о л ь н ы е в о п р о с ы
1. Какие примеси природных вод удаляются в процессе коагуляции?
2. Какие коагулянты используются в процессах обработки воды?
3. Почему при использовании коагулянта Al2(SO4)3 необходимо поддерживать определенные значения рН?
4. Как изменяется щелочность воды при коагуляции?
5. Как изменяется жесткость воды при коагуляции?
6. С какой целью воду перед коагулированием подогревают?
http://www.chem.msu.su/rus/teaching/zagorskii2/lesson0/v002.html
http://mydocx.ru/3-54172.html