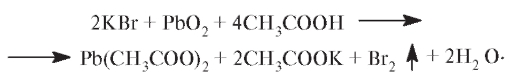Качественная реакция на бромид ион уравнение реакции

Галогенид-ионы можно определить с помощью нитрата серебра AgNO 3 .
Приготовим пробирки с иодидом калия KI , бромидом натрия NaBr , хлоридом натрия NaCl . Добавляем нитрат серебра. В пробирках появляются творожистые осадки нерастворимых галогенидов серебра. Осадок хлорида серебра — белого цвета
Осадок бромида серебра -бледно-желтого цвета
Осадок иодида серебра — желтого цвета.
Реакция с нитратом серебра – качественная реакция на хлорид-, бромид- и иодид-ионы.
Оборудование: пробирки, штатив для пробирок.
Техника безопасности . Необходимо соблюдать осторожность при работе с раствором нитрата серебра.
Постановка опыта – Елена Махиненко, текст – к.п.н. Павел Беспалов.
КАЧЕСТВЕННЫЕ РЕАКЦИИ НА ХЛОРИД-, БРОМИД-, ЙОДИД-ИОНЫ.
ЙОД МОЛЕКУЛЯРНЫЙ.
а) на хлорид-ион – действие раствора нитрата серебра → образуется белый творожистый осадок хлорида серебра:
Осадок нерастворим в азотной кислоте, но легко растворим в аммиаке с образованием комплексного соединения:
хлорид диаммин серебра
При прибавлении к раствору хлорида диаммина серебра концентрированной серной кислоты осадок снова выделяется:
Реакция является фармакопейной.
AgCl – также растворим в тиосульфате натрия.
Т.В.: к 2 каплям раствора NaCl прибавляют 2 капли раствора AgNO3.
К раствору с выпавшим осадком прибавляют концентрированный раствор аммиака до полного растворения осадка. Полученный раствор подкисляют концентрированной азотной кислотой и наблюдают выпадение осадка.
1) действие нитрата серебра → желтовато-белый осадок бромида серебра:
Осадок не растворяется в HNO3, плохо растворим в аммиаке в отличие от хлорида серебра и хорошо растворяется в растворе тиосульфата натрия.
Реакция является фармакопейной.
Т.В.: К 4 каплям раствора NaBr прибавляют 4 капли раствора AgNO3. Раствор с осадком делят на две части. К одной части прибавляют раствор тиосульфата натрия, а к другой – концентрированный раствор аммиака и сравнивают растворение осадка AgBr в этих реактивах.
2) с хлорной водой
Хлорная вода, прибавленная к раствору бромида, выделяет из него свободный бром, который растворяется в сероуглероде или хлороформе, окрашивая слой растворителя в оранжевый цвет:
Cl2 + 2 NaBr = 2 NaCl + Br2
При большом избытке хлорной воды окраска исчезает вследствие образования BrCl, имеющего более светлую окраску.
Т.В. К 5 каплям раствора NaBr прибавляют 1 мл хлороформа, 1-2 капли разбавленной H2SO4 и затем по каплям, при энергичном встряхивании 2-3 капли хлорной воды. Наблюдается окрашивание слоя хлороформа.
1) нитрат серебра выделяет из иодидов светло-желтый творожистый осадок серебра:
Осадок не растворяется в азотной кислоте и растворе аммиака и плохо растворяется в растворе тиосульфата натрия.
Реакция является фармакопейной.
Т.В.: К раствору KI прибавляют немного раствора AgNO3. Проверяют растворение выпавшего осадка в растворе натрия тиосульфата.
2) Хлорная вода выделяет из растворов иодидов свободный йод, который окрашивает сероуглерод или хлороформ в красновато-фиолетовый цвет, а раствор крахмала – в синий.
Т.В.: К 5 каплям раствора NI (KI) прибавить 1 мл хлороформа, 2-3 капли разбавленной H2SO4 и затем по каплям, при энергичном взбалтывании 2-3 капли хлорной воды. Наблюдают окрашивание слоя хлороформа в красновато-фиолетовый цвет. В другую пробирку наливают 1 каплю раствора KI, 1 каплю хлорной воды и 2 капли раствора крахмала. Наблюдают изменение окраски.
3) Хлорид железа (III), конц. H2SO4 и некоторые другие окислители окисляют ион I — до свободного йода; например:
2 FeCl3 + 2 KI = 2 FeCl2 + 2 KCl + I2
Реакция является фармакопейной.
Т.В.: На фильтровальную бумагу в одном месте последовательно по 1 капле наносят растворы KI, HCl, FeCl3. Наблюдают появление бурого пятна, синеющего от капли крахмала.
г) На йод молекулярный → действие крахмала → синее окрашивание.
Выводы: а) на хлорид-ион – действие раствора нитрата серебра → образуется белый творожистый осадок хлорида серебра:
Осадок нерастворим в азотной кислоте, но легко растворим в аммиаке с образованием комплексного соединения:
хлорид диаммин серебра
При прибавлении к раствору хлорида диаммина серебра концентрированной серной кислоты осадок снова выделяется:
Реакция является фармакопейной.
AgCl – также растворим в тиосульфате натрия.
Т.В.: к 2 каплям раствора NaCl прибавляют 2 капли раствора AgNO3.
К раствору с выпавшим осадком прибавляют концентрированный раствор аммиака до полного растворения осадка. Полученный раствор подкисляют концентрированной азотной кислотой и наблюдают выпадение осадка.
1) действие нитрата серебра → желтовато-белый осадок бромида серебра:
Осадок не растворяется в HNO3, плохо растворим в аммиаке в отличие от хлорида серебра и хорошо растворяется в растворе тиосульфата натрия.
Реакция является фармакопейной.
Т.В.: К 4 каплям раствора NaBr прибавляют 4 капли раствора AgNO3. Раствор с осадком делят на две части. К одной части прибавляют раствор тиосульфата натрия, а к другой – концентрированный раствор аммиака и сравнивают растворение осадка AgBr в этих реактивах.
2) с хлорной водой
Хлорная вода, прибавленная к раствору бромида, выделяет из него свободный бром, который растворяется в сероуглероде или хлороформе, окрашивая слой растворителя в оранжевый цвет:
Cl2 + 2 NaBr = 2 NaCl + Br2
При большом избытке хлорной воды окраска исчезает вследствие образования BrCl, имеющего более светлую окраску.
Т.В. К 5 каплям раствора NaBr прибавляют 1 мл хлороформа, 1-2 капли разбавленной H2SO4 и затем по каплям, при энергичном встряхивании 2-3 капли хлорной воды. Наблюдается окрашивание слоя хлороформа.
1) нитрат серебра выделяет из иодидов светло-желтый творожистый осадок серебра:
Осадок не растворяется в азотной кислоте и растворе аммиака и плохо растворяется в растворе тиосульфата натрия.
Реакция является фармакопейной.
Т.В.: К раствору KI прибавляют немного раствора AgNO3. Проверяют растворение выпавшего осадка в растворе натрия тиосульфата.
2) Хлорная вода выделяет из растворов иодидов свободный йод, который окрашивает сероуглерод или хлороформ в красновато-фиолетовый цвет, а раствор крахмала – в синий.
Т.В.: К 5 каплям раствора NI (KI) прибавить 1 мл хлороформа, 2-3 капли разбавленной H2SO4 и затем по каплям, при энергичном взбалтывании 2-3 капли хлорной воды. Наблюдают окрашивание слоя хлороформа в красновато-фиолетовый цвет. В другую пробирку наливают 1 каплю раствора KI, 1 каплю хлорной воды и 2 капли раствора крахмала. Наблюдают изменение окраски.
3) Хлорид железа (III), конц. H2SO4 и некоторые другие окислители окисляют ион I — до свободного йода; например:
2 FeCl3 + 2 KI = 2 FeCl2 + 2 KCl + I2
Реакция является фармакопейной.
Т.В.: На фильтровальную бумагу в одном месте последовательно по 1 капле наносят растворы KI, HCl, FeCl3. Наблюдают появление бурого пятна, синеющего от капли крахмала.
г) На йод молекулярный → действие крахмала → синее окрашивание.
а)на хлорид-ион – действие раствора нитрата серебра → образуется белый творожистый осадок хлорида серебра;осадок нерастворим в азотной кислоте, но легко растворим в аммиаке с образованием комплексного соединения хлориддиаммин серебра.
При прибавлении к раствору хлориддиаммина серебра концентрированной серной кислоты осадок снова выделяется:
Реакция является фармакопейной.
1) действие нитрата серебра → желтовато-белый осадок бромида серебра;осадок не растворяется в HNO3, плохо растворим в аммиаке в отличие от хлорида серебра и хорошо растворяется в растворе тиосульфата натрия.
Реакция является фармакопейной.
2) с хлорной водой
Хлорная вода, прибавленная к раствору бромида, выделяет из него свободный бром, который растворяется в сероуглероде или хлороформе, окрашивая слой растворителя в оранжевый цвет.
1) нитрат серебра выделяет из иодидов светло-желтый творожистый осадок серебра.
Осадок не растворяется в азотной кислоте и растворе аммиака и плохо растворяется в растворе тиосульфата натрия.
Реакция является фармакопейной.
2) Хлорная вода выделяет из растворов иодидов свободный йод, который окрашивает сероуглерод или хлороформ в красновато-фиолетовый цвет, а раствор крахмала – в синий.
3) Хлорид железа (III) окисляет ион I — до свободного йода;
Реакция является фармакопейной.
г) На йод молекулярный → действие крахмала → синее окрашивание.
Качественные реакции на бромид-, хлорид- и йодид-ионы
Реакция окисления галогенидов до свободных галогенов
Применяя различные окислители, определяют бромиды и йодиды. Образующиеся в результате окислительно-восстановительной реакции галогены извлекают хлороформом и наблюдают окраску хлороформного слоя.
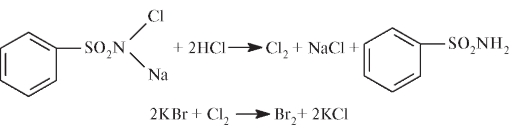
Например, для обнаружения бромид-иона в качестве окислителя используют хлорамин в присутствии кислоты хлороводородной. Образующийся хлор окисляет бромид-ион. Выделяющийся молекулярный бром окрашивает слой хлороформа в желто-бурый цвет:
В качестве окислителей могут использоваться также броматионы: 5Br — + BrO3 — + 6H+ → 3Br2 + 3H2O.
При добавлении к раствору бромида таких сильных окислителей, как PbO2 или CrO3, в уксуснокислой среде происходит выделение паров брома:
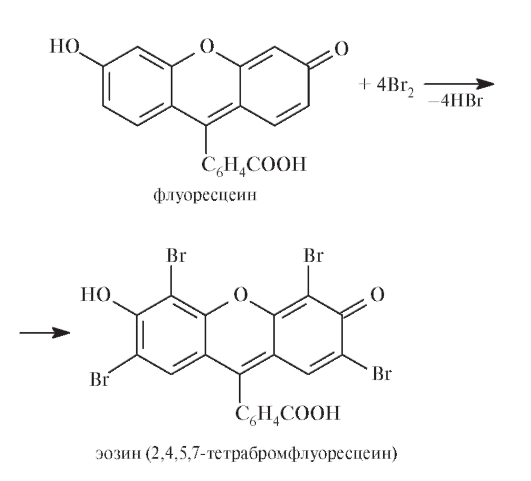
Выделяющийся бром реагирует с флуоресцеином, водноспиртовым раствором которого пропитана фильтровальная бумага, накрывающая пробирку с реакционной смесью. В результате можно наблюдать красное окрашивание образующегося эозина:
Для открытия йодидов можно использовать раствор железа(Ш) хлорида или нитрита натрия. Например, окисление йодид-ионов нитритом протекает по схеме реакции:
Реакция осаждения раствором азотнокислого серебра
Хлориды, бромиды и йодиды при действии серебра нитрата
в присутствии азотной кислоты дают творожистые осадки галогенидов серебра белого или желтого цвета:
Образующиеся осадки нерастворимы в азотной кислоте, но растворимы в растворах натрия тиосульфата, например:
Различить их можно по растворимости в растворах аммиака и карбоната аммония (см. табл. 8.2).
Свойства галогенидов серебра
| Соль | Реактив | |||
| HNO3 | Na2S2O3 | NH3• H20 | (NH4)2CO3 | |
| AgCl | Нерастворим | Растворим [Ag(S2O3)2] 3- | Растворим [Ag(NH3)2]+ | Растворим [Ag(NH3)2]+ |
| AgBr | Нерастворим | Растворим [Ag(S2O3)2] 3- | Частично растворим в концентрированном растворе аммиака | Нерастворим |
| AgI | Нерастворим | Растворим [Ag(S2O3)2] 3- | Нерастворим | Нерастворим |
Хлорид серебра легко растворяется в разбавленных растворах аммиака и аммония карбоната с образованием комплексных ионов. Бромид серебра нерастворим в растворе (NH4)2CO3, мало растворим в разбавленных растворах аммиака, но растворяется в концентрированных растворах аммиака.
Йодид серебра нерастворим ни в растворах аммиака, ни в растворах карбоната аммония.
http://helpiks.org/8-62822.html
http://lektsii.org/8-54421.html