Реферат Качественные реакции ионов серебра
LXIX Московская олимпиада школьников по химии
Качественные реакции ионов серебра
ученик 9 класса ГБОУ гимназии № 000
«Московская городская педагогическая гимназия-лаборатория» г. Москвы
§1. Понятие качественной реакции. 4
§2. Качественные реакции ионов серебра. 4-7
2.1 Качественные реакции ионов серебра с неорганическими реагентами. 4-6
2.2 Качественные реакции ионов серебра с органическими реагентами. 6-7
Список литературы. 8
Серебро знакомо человеку с незапамятных времен. Оно часто встречалось в самородном виде, и его не надо было выплавлять из руды. Благодаря своим свойствам серебро использовалось для изготовления посуды, украшений и чеканки монет.
В IV в. до н. э. когда войска Александра Македонского вторглись в Индию, на берегах реки Инд среди его солдат разразилась эпидемия которая, почему-то не затронула военачальников. Оказалось, что простые воины пользовались оловянной посудой, а их командиры – серебряной. Тогда вспомнили, что еще персидский царь Кир II Великий (VI в. до н. э.) во время своих военных походов приказывал хранить питьевую воду только в серебряных сосудах. Позднее римские легионеры стали носить панцири, наколенники и поножи, изготовленные из серебра. Все это делали, потому что заметили свойство серебра обеззараживать воду и раны.
Из-за способности некоторых соединений серебра легко восстанавливаться при освещении и давать на пластинке скрытое изображение появилась фотография.
С развитием техники сплавы серебра стали применяться в качестве катализаторов, для электрических контактов, например, припоя.
И по настоящее время в санитарии и медицине используется бактерицидные свойства серебра на микроорганизмы. Для того чтобы прекратить развитие бактерий в воде должно содержаться от 20-30 ионов на миллиард молекул воды. А для того чтобы вода была полностью пригодна для питья, на тонну воды должно приходится около 50 мг серебра.
Широкое использование серебра и его соединений издавна стимулировало разработку методов качественного обнаружения серебра.
В данном реферате мы хотим рассмотреть качественные реакции ионов серебра.
Чтобы справиться с поставленной целью, необходимо выполнить следующие задачи:
· рассмотреть само понятие «качественная реакция»,
· ознакомиться с качественными реакциями на ионы серебра и их практическим значением.
§1 «Понятие качественной реакции»
Химический анализ веществ — одно из важнейших применений химии, он подразделяется на качественный и количественный. Качественный анализ предшествует количественному. Качественный анализ идентифицирует вещество и устанавливает наличие в нем тех или иных примесей. С помощью количественного анализа определяется соотношение основного вещества и примесей. Иными словами, качественный анализ отвечает на вопрос «что?», а количественный — «сколько?».
Качественный анализ в химии основан на обнаружении в растворах веществ ионов с помощью характерных реакций — реакций, протекающих с изменением окраски, с выпадением или растворением осадка, или с выделением газа. Характерная качественная реакция является селективной, так как с ее помощью определяется данный ион в присутствии многих других ионов.
Чувствительность – одна из важных характеристик качественной реакции – выражается наименьшей концентрацией раствора, при которой данный ион может быть обнаружен без предварительной обработке раствора для увеличении его концентрации.
Специфическими называются качественные реакции, обладающие большой чувствительностью и селективностью.
§2 Качественные реакции ионов серебра
2.1 Качественные реакции ионов серебра с неорганическими реагентами
Ионы серебра можно определить по образованию характерных осадков при действии разных неорганических реагентов. Рассмотрим некоторые из реакций.
2.1.1.Реакция с солями.
a) Нитрат серебра взаимодействует с хроматом калия, образуется нитрат калия и осадок кирпично-красного цвета, растворимый в аммиаке и азотной кислоте, — хромат серебра
2AgNO3 + K2CrO4 = Ag2CrO4↓ + 2KNO3
2Ag+ +2NO3̄ +2K++CrO42-= Ag2CrO4↓+2K++2 NO3-
b) При взаимодействии любой растворимой соли серебра с карбонатом натрия образуется нитрат натрия и нерастворимая соль карбонат серебра.
Ag2CO3 – осадок белого цвета, растворим в уксусной и минеральных кислотах.
с) Нитрат серебра при реакции с нитритом натрия образует нитрат натрия и осадок — нитрит серебра.
AgNO2 – нерастворимый в воде осадок, но растворяется в растворах щелочных нитритов. Имеет желтую окраску, и форму игл.
Ag++NO3̄ +Na++NO2̄ = AgNO2↓+ Na++ NO3̄
d) Нитрат серебра реагирует с ортофосфатом натрия с образованием нитрата натрия и ортофосфатом серебра.
Ag3PO4- осадок желтого цвета, нерастворим в воде, но хорошо растворим в минеральных кислотах и растворе аммиака.
3Ag++3NO3̄ +3Na++ PO43-= Ag3PO4↓+3Na++3NO3̄
е) При реакции нитрата серебра с сульфатом натрия образуется нитрат натрия и сульфат серебра.
Ag2SO4- осадок в форме ромбических кристаллов, бесцветный, нерастворимый в воде.
2AgNO3+Na2SO4= Ag2SO4↓+ 2NaNO3
2Ag++2NO3̄ +2Na++SO42-= Ag2SO4↓+2Na++2NO3̄
2Ag++ SO42-= Ag2SO4↓
f) Тиосульфат серебра можно получить при сливании растворов тиосульфата натрия и нитрата серебра.
Ag2S2O3- белый, постепенно желтеющий в воде осадок.
2Na++ S2O32-+2Ag++2NO3̄ = Ag2S2O3↓+2Na++2NO3̄
2Ag+ +S2O32-= Ag2S2O3↓
g) При реакции серебра, сероводорода и кислорода воздуха образуется сульфид серебра и вода. Сульфид серебра наименее растворимая соль серебра, представляет собой осадок черного цвета. Также его можно получить при действии сероводорода или сульфидов щелочных металлов на растворимые соли серебра.
2Na++ S2-+2Ag++2NO3̄ = Ag2S↓+2Na++2NO3̄
2.1.2 Реакция с щелочами.
2AgNO3 + 2NaOH = Ag2O↓ + 2NaNO3 + H2О
Ag2О — осадок бурого цвета. При пропускании углекислого газа через оксид серебра образуется нерастворимый карбонат серебра.
Ag2O + CO2 = Ag2CО3↓
2.1.3. Реакции с растворами галогенидов:
AgNO3 + NaCl = AgCl↓ + NaNO3
AgNO3 + NaBr = AgBr↓ + NaNO3
AgNO3 + KI = AgI↓ + KNO3
В общем виде ионые уравнения реакции:
AgNO3 + NaM=AgM↓+ NaNO3
Ag++NO3̄ +Na++M-= AgM↓+Na++NO3̄
AgCl — белый творожистый осадок, разлагается при солнечном свете 2AgCl=2Ag+Cl2.
AgBr — бледно-желтый осадок,
AgI — желтый осадок.
Все галогениды, кроме иодида, хорошо растворимы в аммиаке из-за того что образуются растворимые комплексы, например хлорид серебра
2.1.4. Реакция с кислотами.
Сульфат серебра можно также образовать с помощью реакции нитрата серебра и серной кислоты.
2Ag++2NO3̄ +2H++SO42-= Ag2SO4↓+2H++2NO3̄
2Ag++ SO42-= Ag2SO4↓
2.2 Качественные реакции ионов серебра с органическими реагентами
Серебро также может быть обнаружено с помощью органических реагентов. Большую значимость имеют те реагенты, которые при реакции с серебром образуют окрашенные комплексные соединения и осадки.
Рассмотрим наиболее известные реакции ионов серебра с органическими реагентами.
a) Ацетиленид серебра легко может быть получен при пропускании ацетилена через аммиачный раствор соли серебра.
2AgNO3 + 2NH3+H2O = Ag2O↓ + 2NH4NO3
[Ag(NH3)2]OH – реактив Толленса.
С помощью данной реакции можно определить ацетилен и непредельные углеводороды с концевой тройной связью.
b) Реакция «серебряного зеркала».
Происходит при небольшом нагревании альдегидов с реактивом Толленса, в данной реакции происходит восстановление серебра и образование соли соответствующей карбоновой кислоты.
2[Ag(NH3)2]OH+HCHO t →2Ag↓+HCOONH4+3NH3+H2O
в) С помощью реакции «серебряного зеркала» можно отличить раствор глюкозы от раствора сахарозы.
HOCH2(CHOH)4CHO +2[Ag(NH3)2]OH t → HOCH2(CHOH)4COONH4+2Ag↓+3NH3+H2O
Серебро играет в жизни людей важную роль. У этого металла есть многие отличительные способности, которые люди используют с древности. Например, способность убивать многие бактерии. Поэтому, когда воду наливают в серебряные сосуды, некоторое количество ионов обеззараживает воду. Еще одна отличительная особенность серебра, это хорошая электропроводность. Но, так как делать провода из серебра очень затратно, люди используют его в виде сплавов, например с кадмием, а потом как припой. Также серебро используется для изготовления пломб для зубов.
В данном реферате мы рассмотрели понятие «качественная реакция» и самые часто встречаемые реакции для определения ионов серебра. Чаще всего используют реакции с выпадением осадков, из-за того что многие соли серебра нерастворимы и благодаря данному свойству солей серебра, с помощью реакции обмена можно получить нерастворимый осадок. Люди используют серебро и свойства ионов серебра с древности, и безусловно будут использовать в будущем.
Аналитическая химия серебра М., 1975.
Электрон. Данные. – М., 2006. – Режим доступа: http://www. lib. *****/fulltext/m/2006/m9.pdf, свободный. – Загл. С экрана. – Данные соответствуют 14.03.13.
Неорганическая химия в 3 томах. том 3 «Химия переходных эелеметнов» М., 2007
Химические свойства неорганических веществ. М., 1996
«Органическая химия 10 класс» М., 2007
, Химия 9 класс Санкт-Петербург., 1999
Энциклопедия для детей, том химия. М.: Астрель, 2013.
4.1.4. Качественные реакции на неорганические вещества и ионы.
Представим себе такую ситуацию:
Вы работаете в лаборатории и решили провести какой-либо эксперимент. Для этого вы открыли шкаф с реактивами и неожиданно увидели на одной из полок следующую картину. У двух баночек с реактивами отклеились этикетки, которые благополучно остались лежать неподалеку. При этом установить точно какой банке соответствует какая этикетка уже невозможно, а внешние признаки веществ, по которым их можно было бы различить, одинаковы.
В таком случае проблема может быть решена с использованием, так называемых, качественных реакций.
Качественными реакциями называют такие реакции, которые позволяют отличить одни вещества от других, а также узнать качественный состав неизвестных веществ.
Например, известно, что катионы некоторых металлов при внесении их солей в пламя горелки окрашивают его в определенный цвет:
Данный метод может сработать только в том случае, если различаемые вещества по разному меняют цвет пламени, или же одно из них не меняет цвет вовсе.
Но, допустим, как назло, вам определяемые вещества цвет пламени не окрашивают, или окрашивают его в один и тот же цвет.
В этих случаях придется отличать вещества с применением других реагентов.
В каком случае мы можем отличить одно вещество от другого с помощью какого-либо реагента?
Возможны два варианта:
- Одно вещество реагирует с добавленным реагентом, а второе нет. При этом обязательно, должно быть ясно видно, что реакция одного из исходных веществ с добавленным реагентом действительно прошла, то есть наблюдается какой-либо ее внешний признак — выпадал осадок, выделился газ, произошло изменение цвета и т.п.
Например, нельзя отличить воду от раствора гидроксида натрия с помощью соляной кислоты, не смотря на то, что щелочи с кислотами прекрасно реагируют:
NaOH + HCl = NaCl + H2O
Связано это с отсутствием каких-либо внешних признаков реакции. Прозрачный бесцветный раствор соляной кислоты при смешении с бесцветным раствором гидроксида образует такой же прозрачный раствор:
Но зато, можно воду от водного раствора щелочи можно различить, например, с помощью раствора хлорида магния – в данной реакции выпадает белый осадок:
2) также вещества можно отличить друг от друга, если они оба реагируют с добавляемым реагентом, но делают это по-разному.
Например, различить раствор карбоната натрия от раствора нитрата серебра можно с помощью раствора соляной кислоты.
с карбонатом натрия соляная кислота реагирует с выделением бесцветного газа без запаха — углекислого газа (СО2):
а с нитратом серебра с образованием белого творожистого осадка AgCl
Ниже в таблицах представлены различные варианты обнаружения конкретных ионов:
Качественные реакции на катионы
| Катион | Реактив | Признак реакции |
| Ba 2+ | SO4 2- | |
| Al 3+ | Щелочь (амфотерные свойства гидроксида) | |
| NH4 + | OH − , нагрев | |
| H + (кислая среда) | Красное окрашивание |
Качественные реакции на анионы
| Анион | Воздействие или реактив | Признак реакции. Уравнение реакции | ||||||||||||||
| SO4 2- | Ba 2+ | |||||||||||||||
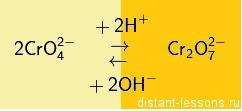
| CrO4 2- | Ba 2+ | |||||||||||||||
| CO2 | Известковая вода Ca(OH)2 |
| Индикатор | Цвет в кислой среде pH | Цвет в нейтральной среде pH = 7 Цвет в щелочной среде pH > 7 | |
| Лакмус фиолетовый | Красный | Фиолетовый | Синий |
| Метиловый оранжевый | Красный | Оранжевый | Желтый |
| Фенолфталеин | Нет (бесцветный) | Нет (бесцветный) | Малиновый |
Существует несколько мнемонических правил для запоминания цветов индикаторов:
Фенолфталеиновый в щелочах малиновый, но несмотря на это в кислотах он без цвета.
В кислотах лакмус красный – цвет такой прекрасный, а в щелочах он синий как январский иней, а в нейтральной среде фиолетовый, как нигде. (Этот стишок сочинили когда-то мы с товарищем. Хоть он не совсем складный и мы так и не можем объяснить, с чего бы это иней, который обычно белый, в январе вдруг станет синим, стишок как-то по-особенному запал в мою память, всегда им пользуюсь)
Кислота – начинается на букву К, как и слово «кислый» — помогает вспомнить цвет лакмуса и метилоранжа в кислотах.
– элементы VIIA -группы( F , Cl , Br , I ), типичные неметаллы.
Пойдем по порядку:
Фтор – F 2 – желтый газ с легким зеленым отливом. Самый электроотрицательный неметалл, поэтому с кислородом образует не оксид фтора, а фторид кислорода: OF 2 степень окисления кислорода в нем равна +2. Чрезвычайно активное вещество, реагирует со всем, с чем не лень. И большинство реакций протекает бурно, взрывообразно.
Фторид-ионы ( F — ) в растворе определяются добавлением катионов кальция ( Ca 2+ ), наблюдается выпадение белого осадка :
2 KF + CaCl 2 → 2 KCl + CaF 2 ↓
Сокращенное ионное уравнение: Ca 2+ + 2 F — → CaF 2 ↓
- Хлор – Cl 2 – зеленый газ, с характерным резким запахом, сильный яд, тяжелее воздуха (при химической атаке стелется по земле):
Хлорид-ионы ( Cl — ) в растворе определяются добавлением катионов серебра ( Ag + ), наблюдается выпадение белого творожистого осадка (об этой реакции говорилось ранее в разделе серебро):
KCl + AgNO 3 → AgCl ↓ + KNO 3
Сокращенное ионное уравнение: Ag + + Cl — → AgCl ↓
- Бром – Br 2 – красно-бурая летучая жидкость, имеющая очень резкий неприятный запах.
Бромд-ионы ( Br — ) в растворе определяются добавлением катионов серебра ( Ag + ), наблюдается выпадение слегка желтоватого осадка :
KBr + AgNO 3 → AgBr ↓ + KNO 3
Сокращенное ионное уравнение: Ag + + Br — → AgBr ↓
- Иод – I 2 – летучие черно-серые с фиолетовым отливом кристаллы. Пары фиолетовые, имеют характерный запах.
Иодид-ионы ( I — ) в растворе определяются добавлением катионов серебра ( Ag + ), наблюдается выпадение желтоватого осадка (цвет интенсивнее, чем у бромида серебра) :
Сокращенное ионное уравнение: Ag + + I — → AgI ↓
Осадки-галогениды не растворяются в разбавленных кислотах.
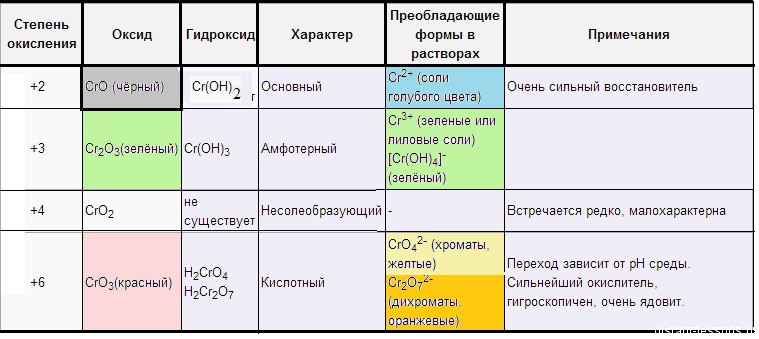
Простое вещество сера – хрупкие желтые кристаллы.
Сера может проявлять различные степени окисления:
Степень окисления -2:
в сульфИД-ионе ( S 2- ) и гидросульфИД-ионе ( HS — ).
СульфИДы (и гидросульфИДы) – это соли сероводородной кислоты, которая является слабым электролитом. Поэтому сильные кислоты вытесняют ее из растворов солей. Выделяется H 2 S – сероводород, газ с неприятным запахом тухлых яиц :
K 2 S + 2HCl → 2KCl + H 2 S↑
Сокращенное ионное уравнение: 2 H + + S 2- → H 2 S ↑
Выделившийся газ ( H 2 S ) на воздухе сгорает синим пламенем (не в смысле, что выделился и сразу сгорел, а если начать сжигать):
Так же сероводород ( H 2 S ) может быть поглощен растворами щелочей: H 2 S + 2 NaOH →
Сероводород является хорошим восстановителем, так как сера в нем в низшей степени окисления.
Еще одна особенность ионов S
2- позволяет легко определить их в растворе. Ионы S 2- образуют осадки со многими тяжелыми металлами:
- Классическая реакция с ионами Pb2+ . Образуется черный осадок сульфида серы :
- С ионами Cu 2+ , Fe 2+ , Ni 2+ , Cu 2+ , Pb 2+ , Hg 2+ , Ag + и ионами многих других металлов тоже образуются осадки черного цвета .
- С ионом Zn 2+ образуется белый осадок (один из немногих нечерных нерастворимых сульфидов):
Так как сера в сульфид-ионе в низшей степени окисления, она может окислиться. При действии сильных окислителей на сульфиды они окисляются до сульфатов (как правило). Классическая ЕГЭ-шная реакция, цитата из С2: «…черный осадок побелел после обработки его пероксидом водорода… ». Речь идет о
черном осадке сульфида свинца ( PbS ). Пероксид водорода H 2 O 2 (сильный окислитель) превращает черный сульфид свинца в белый (тоже нерастворимый) сульфат свинца ( PbSO 4 ):
Степень окисления + 4:
встречается в оксиде серы ( IV ) (сернистом газе – SO 2 ), в соответствующей этому оксиду кислоте – сернистой ( H 2 SO 3 , существующей только в растворе) и в солях сернистой кислоты – сульфИТах и гидросульфИТах.
Сернистый газ ( SO 2 ) – бесцветный газ с резким запахом (по легендам – запахом ада). Его можно почувствовать чиркнув спичку. Образуется при сжигании серы, сероводородов, сульфидов, серосодержащих органических веществ. Классическое школьное уточнение: « обесцвечивает раствор фуксина и фиолетовые чернила », при этом совсем не обязательно знать, что такое фуксин, и какие реакции протекают. Просто хорошо бы запомнить эту формулировку.
Так как является кислотным оксидом, реагирует с растворами щелочей. (формулировка из задания ЕГЭ: «…выделившийся газ с резким запахом был поглощен раствором щелочи…» ). Образуются соли сернистой кислоты – сульфиты:
СульфИТ-ионы и гидросульфИТ-ионы в растворе можно обнаружить добавлением сильной кислоты. При этом из раствора сульфита (гидросульфита) вытесняется сернистая кислота: H 2 SO 3 , которая не стабильная, поэтому быстро разлагается на воду и соответствующий оксид ( SO 2 ). То есть, если совсем коротко: при действии на сульфиты и гидросульфиты кислот выделяется SO 2 – газ с резким запахом (обесцвечивающий раствор фуксина и фиолетовые чернила):
Можно (и грамотнее) записать сразу:
Степень окисления +6
встречается в серном ангидриде (оксиде серы( VI ) – SO 3 ), в соответствующей ему серной кислоте ( H 2 SO 4 ) и в ее солях, сульфАТах.
Серный ангидрид ( SO 3 ) и серная кислота( H 2 SO 4 ) содержат серу в высшей степени окисления, поэтому являются сильными окислителями.
Сульфаты в растворе определяются добавлением катионов бария ( Ba 2+ ). Сульфат-ион с катионом бария образует белый осадок ( нерастворимый в кислотах ):
Сокращенное ионное уравнение: Ва 2+ + S O 4 2- → BaS O 4 ↓
CO 3 2-
– карбонат-ион и HCO 3 — – гидрокарбонат-ион
являются анионом слабой, нестабильной, существующей только в растворе, угольной кислоты. Поэтому она легко вытесняется сильными кислотами из растворов солей (карбонатов и гидрокарбонатов).
Вытесняется и тут же распадается на воду и углекислый газ.
При действии кислот на карбонаты выделяется бесцветный газ без вкуса и запаха :
Можно (и грамотнее) записать сразу: K 2 CO 3 + 2 HCl → 2 KCl + CO 2 ↑ + H 2 O
Эта качественная реакция вам хорошо известна, вы наверняка проводили ее у себя дома. Добавим уксус к соде, и как раз будет выделяться газ, в чем можно убедиться если поднести спичку, она погаснет, так как CO 2 не поддерживает горения:
Выделившийся углекислый газ может быть поглощен раствором щелочи:
В связи со способностью поглощаться щелочами для описания углекислого газа часто встречается следующая формулировка: «… газ, при пропускании его через известковую воду, вызвал ее помутнение… ». Известковая вода – это профильтрованный раствор гидроксида кальция (гидроксид кальция полностью не растворяется в воде, образуется взвесь, и чтобы получить прозрачный раствор – его фильтруют, для очищения от не растворившихся частиц гидроксида кальция). При взаимодействии гидроксида кальция с углекислым газом образуется нерастворимый карбонат кальция, который и обеспечивает мутность:
PO 4 3-
– анион ортофосфорной кислоты (H 3 PO 4 ). В растворе его можно определить добавлением катионов серебра , при этом выпадает интенсивно-желтый осадок :
Сокращенное ионное уравнение: 3 Ag + + PO 4 3- → Ag 3 PO 4 ↓
SiO 3 2-
– анион кремниевой кислоты ( H 2 SiO 3 ) , которая являясь слабым электролитом, вытесняется из растворов ее солей. Кроме того, кремниевая кислота малорастврима в воде, поэтому в момент вытеснения ее из раствора соли, появляется гелеобразный осадок – это и будет H 2 SiO 3 :
Кремниевая кислота настолько слабая, что вытесняется даже угольной:
– оксид азота ( VI ).
Ядовитый газ с неприятным запахом бурого цвета.
В ЕГЭ его обычно именно так и обзывают – бурый газ .
Химически очень активное вещество:
- при взаимодействии не очень активных металлов с HNO 3 концентрированной;
- при разложении нитратов этих металлов.
В реакции с водой диспропорционируется, образуя азотную и азотистую кислоты:
Похожая реакция диспропорционирования происходит при растворении NO 2 в щелочах (образуются не кислоты, а соли этих кислот, нитраты и нитриты соответственно):
В присутствии избытка кислорода реакция идет без образования азотистой кислоты (диспропорционирования не происходит):
OH —
Наличие в растворе ионов OH — указывает на щелочную реакцию среды ( pH >7).
Определить pH можно с помощью индикаторов.
Окраски индикаторов в разных средах указаны в пункте про ион H + . Щелочную среду имеют не только щелочи, но и растворы аммиака и аминов, растворы солей, образованных сильными основаниями и слабыми кислотами.
Если нужно определить щелочь, то к раствору надо добавить соль металла, образующего слабое основание. Щелочь с такой солью даст осадок гидроксида металла:
CuCl 2 + 2NaOH → Cu(OH) 2 ↓ + 2NaCl
http://scienceforyou.ru/teorija-dlja-podgotovki-k-egje/4-1-4-kachestvennye-reakcii-na-neorganicheskie-veshhestva-i-iony
http://distant-lessons.ru/uravneniya-kachestvennyx-reakcij.html