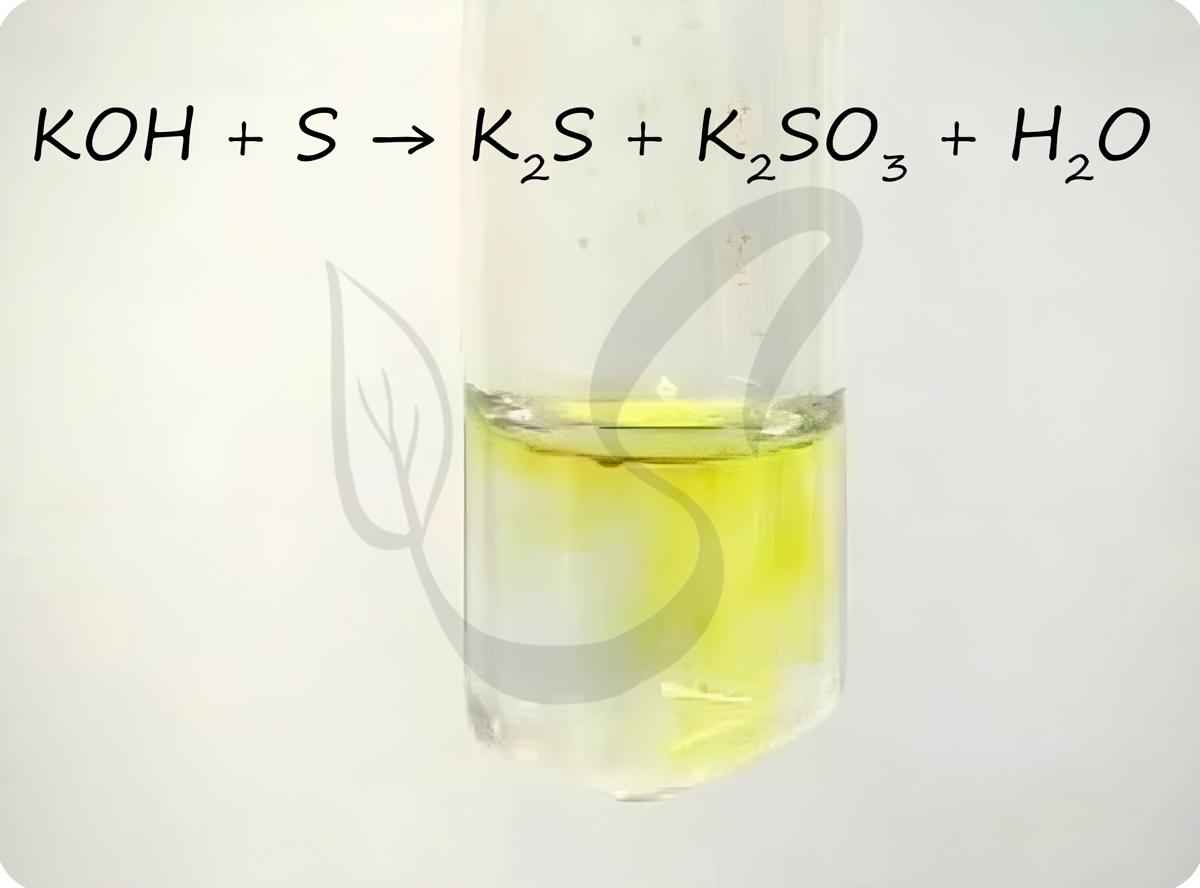Сероводород
Сероводород
Строение молекулы и физические свойства
Сероводород H2S – это бинарное соединение водорода с серой, относится к летучим водородным соединениям. Следовательно, сероводород бесцветный ядовитый газ, с запахом тухлых яиц. Образуется при гниении. В твердом состоянии имеет молекулярную кристаллическую решетку.
Геометрическая форма молекулы сероводорода похожа на структуру воды — уголковая молекула. Но валентный угол H-S-H меньше, чем угол H-O-H в воде и составляет 92,1 о .
Способы получения сероводорода
1. В лаборатории сероводород получают действием минеральных кислот на сульфиды металлов, расположенных в ряду напряжений левее железа.
Например , при действии соляной кислоты на сульфид железа (II):
FeS + 2HCl → FeCl2 + H2S↑
Еще один способ получения сероводорода – прямой синтез из водорода и серы:
Еще один лабораторный способ получения сероводорода – нагревание парафина с серой.
Видеоопыт получения и обнаружения сероводорода можно посмотреть здесь.
2. Также сероводород образуется при взаимодействии растворимых солей хрома (III) и алюминия с растворимыми сульфидами. Сульфиды хрома (III) и алюминия необратимо гидролизуются в водном растворе.
Например: х лорид хрома (III) реагирует с сульфидом натрия с образованием гидроксида хрома (III), сероводорода и хлорида натрия:
Химические свойства сероводорода
1. В водном растворе сероводород проявляет слабые кислотные свойства. Взаимодействует с сильными основаниями, образуя сульфиды и гидросульфиды:
Например , сероводород реагирует с гидроксидом натрия:
H2S + 2NaOH → Na2S + 2H2O
H2S + NaOH → NaНS + H2O
2. Сероводород H2S – очень сильный восстановитель за счет серы в степени окисления -2. При недостатке кислорода и в растворе H2S окисляется до свободной серы (раствор мутнеет):
В избытке кислорода:
3. Как сильный восстановитель, сероводород легко окисляется под действием окислителей.
Например, бром и хлор окисляют сероводород до молекулярной серы:
H2S + Br2 → 2HBr + S↓
H2S + Cl2 → 2HCl + S↓
Под действием избытка хлора в водном растворе сероводород окисляется до серной кислоты:
Например , азотная кислота окисляет сероводород до молекулярной серы:
При кипячении сера окисляется до серной кислоты:
Прочие окислители окисляют сероводород, как правило, до молекулярной серы.
Например , оксид серы (IV) окисляет сероводород:
Соединения железа (III) также окисляют сероводород:
H2S + 2FeCl3 → 2FeCl2 + S + 2HCl
Бихроматы, хроматы и прочие окислители также окисляют сероводород до молекулярной серы:
Серная кислота окисляет сероводород либо до молекулярной серы:
Либо до оксида серы (IV):
4. Сероводород в растворе реагирует с растворимыми солями тяжелых металлов : меди, серебра, свинца, ртути, образуя черные сульфиды, нерастворимые ни в воде, ни в минеральных кислотах.
Например , сероводород реагирует в растворе с нитратом свинца (II). при этом образуется темно-коричневый (почти черный) осадок, нерастворимый ни в воде, ни в минеральных кислотах:
Взаимодействие с нитратом свинца в растворе – это качественная реакция на сероводород и сульфид-ионы.
Видеоопыт взаимодействия сероводорода с нитратом свинца можно посмотреть здесь.
Как из серной кислоты получить сероводород уравнение реакции
Сера — элемент VIa группы 3 периода периодической таблицы Д.И. Менделеева. Относится к группе халькогенов — элементов VIa группы.
Сера — S — простое вещество имеет светло-желтый цвет. Использовалась еще до нашей эры в составе священных курений при религиозных обрядах.
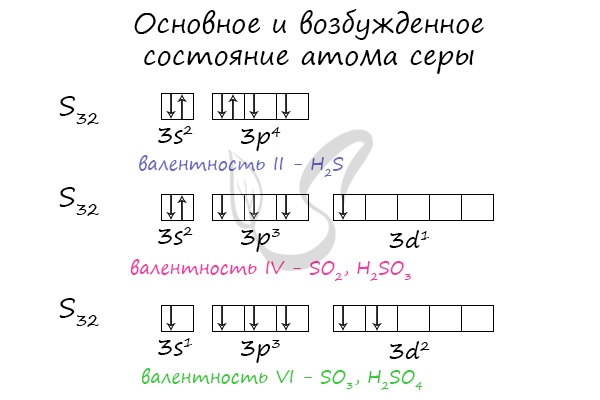
Основное и возбужденное состояние атома серы
Электроны s- и p-подуровня способны распариваться и переходить на d-подуровень. Как и всегда, количество валентных электронов отражает количество возможных связей у атома.
В разных электронных конфигурациях сера способна принимать валентности: II, IV и VI.
Природные соединения
- FeS2 — пирит, колчедан
- ZnS — цинковая обманка
- PbS — свинцовый блеск (галенит), Sb2S3 — сурьмяный блеск, Bi2S3 — висмутовый блеск
- HgS — киноварь
- CuFeS2 — халькопирит
- Cu2S — халькозин
- CuS — ковеллин
- BaSO4 — барит, тяжелый шпат
- CaSO4 — гипс
В местах вулканической активности встречаются залежи самородной серы.
В промышленности серу получают из природного газа, который содержит газообразные соединения серы: H2S, SO2.
Серу можно получить разложением пирита
В лабораторных условиях серу можно получить слив растворы двух кислот: серной и сероводородной.
- Реакции с неметаллами
На воздухе сера окисляется, образуя сернистый газ — SO2. Реагирует со многими неметаллами, без нагревания — только со фтором.
При нагревании сера бурно взаимодействует со многими металлами с образованием сульфидов.
Реакции с кислотами
При взаимодействии с концентрированными кислотами (при длительном нагревании) сера окисляется до сернистого газа или серной кислоты.
Реакции с щелочами
Сера вступает в реакции диспропорционирования с щелочами.
Реакции с солями
Сера вступает в реакции с солями. Например, в кипящем водном растворе сера может реагировать с сульфитами с образованием тиосульфатов.
Сероводород — H2S
Бесцветный газ с характерным запахом тухлых яиц. Огнеопасен. Используется в химической промышленности и в лечебных целях (сероводородные ванны).
Сероводород получают в результате реакции сульфида алюминия с водой, а также взаимодействия разбавленных кислот с сульфидами.
Сероводород плохо диссоциирует в воде, является слабой кислотой. Реагирует с основными оксидами, основаниями с образованием средних и кислых солей (зависит от соотношения основания и кислоты).
KOH + H2S = KHS + H2O (гидросульфид калия, избыток кислоты)
Металлы, стоящие в ряду напряжений до водорода, способны вытеснить водород из кислоты.
Сероводород — сильный восстановитель (сера в минимальной степени окисления S 2- ). Горит в кислороде синим пламенем, реагирует с кислотами.
Качественной реакцией на сероводород является реакция с солями свинца, при котором образуется сульфид свинца.
Оксид серы — SO2
Сернистый газ — SO2 — при нормальных условиях бесцветный газ с характерным резким запахом (запах загорающейся спички).
В промышленных условиях сернистый газ получают обжигом пирита.
В лаборатории SO2 получают реакцией сильных кислот на сульфиты. В ходе подобных реакций образуется сернистая кислота, распадающаяся на сернистый газ и воду.
Сернистый газ получается также в ходе реакций малоактивных металлов с серной кислотой.
С основными оксидами, основаниями образует соли сернистой кислоты — сульфиты.
Химически сернистый газ очень активен. Его восстановительные свойства продемонстрированы в реакциях ниже.
В присутствии сильных восстановителей SO2 способен проявлять окислительные свойства (понижать степень окисления).
Сернистая кислота
Слабая, нестойкая двухосновная кислота. Существует лишь в разбавленных растворах.
Диссоциирует в водном растворе ступенчато.
В реакциях с основными оксидами, основаниями образует соли — сульфиты и гидросульфиты.
H2SO3 + KOH = H2O + KHSO3 (соотношение кислота — основание, 1:1)
С сильными восстановителями сернистая кислота принимает роль окислителя.
Как и сернистый газ, сернистая кислота и ее соли обладают выраженными восстановительными свойствами.
Оксид серы VI — SO3
Является высшим оксидом серы. Бесцветная летучая жидкость с удушающим запахом. Ядовит.
В промышленности данный оксид получают, окисляя SO2 кислородом при нагревании и присутствии катализатора (оксид ванадия — Pr, V2O5).
В лабораторных условиях разложением солей серной кислоты — сульфатов.
Является кислотным оксидом, соответствует серной кислоте. При реакции с основными оксидами и основаниями образует ее соли — сульфаты и гидросульфаты. Реагирует с водой с образованием серной кислоты.
SO3 + 2KOH = K2SO4 + 2H2O (основание в избытке — средняя соль)
SO3 + KOH = KHSO4 + H2O (кислотный оксид в избытке — кислая соль)
SO3 — сильный окислитель. Чаще всего восстанавливается до SO2.
© Беллевич Юрий Сергеевич 2018-2022
Данная статья написана Беллевичем Юрием Сергеевичем и является его интеллектуальной собственностью. Копирование, распространение (в том числе путем копирования на другие сайты и ресурсы в Интернете) или любое иное использование информации и объектов без предварительного согласия правообладателя преследуется по закону. Для получения материалов статьи и разрешения их использования, обратитесь, пожалуйста, к Беллевичу Юрию.
Урок №12. Сероводород. Сульфиды
Повторите тему 9 класса:
ПОЛУЧЕНИЕ СЕРОВОДОРОДА
Сероводород – токсичный бесцветный газ с запахом тухлых яиц.
Сероводород (H 2 S) в лаборатории можно получить нагреванием смеси парафина с серой.
Выделяющийся сероводород можно обнаружить с помощью влажной универсальной индикаторной бумаги: под действием сероводорода она краснеет. При добавлении сульфата меди к сероводородной воде выпадает черный осадок сульфида меди
CuSO 4 + H 2 S = CuS↓+ H 2 SO 4
По черному осадку сульфида свинца можно обнаружить сульфид-ион.
Сероводород получают действием минеральных кислот на сульфиды металлов, расположенных в ряду напряжений левее железа.
FeS (тв.) + 2HCl = FeCl 2 + H 2 S↑
FeS (тв.) + H 2 SO 4 = FeSO 4 + H 2 S↑
Еще один способ получения сероводорода – прямой синтез из водорода и серы:
H 2 + S ↔ H 2 S↑ + 20,92 кДж
Выход H 2 S мал, т.к. обратимая реакция обратима
Наиболее чистый сероводород можно получить при гидролизе сульфида алюминия
Al 2 S 3 (тв.) + 6H 2 O (ж.) = холод = 2Al(OH) 3 ↓ + 3H 2 S↑
Сероводород можно получить в других реакциях:
8Na + 5H 2 SO 4 (конц.) = 4Na 2 SO 4 + H 2 S↑ + 4H 2 O
8HI + H 2 SO 4 (конц.) = 4I 2 + H 2 S↑ + 4H 2 O
ХИМИЧЕСКИЕ СВОЙСТВА СЕРОВОДОРОДА
В водном растворе сероводород проявляет слабые кислотные свойства .
H 2 S ↔ H + + HS — (I ступень)
HS — ↔ H + + S 2- (II ступень)
Изменяет окраску индикаторов на красную – кислая среда.
2) Взаимодействие с растворами оснований. Взаимодействует с сильными основаниями, образуя сульфиды и гидросульфиды:
H 2 S + 2KOH = K 2 S + 2H 2 O
K 2 S средняя соль — сульфид калия
H 2 S (избыток) + KOH = KHS + H 2 O
KHS кислая соль — гидросульфид калия
3) С растворами солей тяжёлых металлов (Cu, Pb, Ni, Cd, Zn):
H 2 S + CuSO 4 = CuS↓ + H 2 SO 4
CuS осадок чёрного цвета
Сульфиды тяжёлых металлов окрашены: PbS; CuS; NiS – чёрные. СdS – жёлтый. ZnS – белый.
Сероводород реагирует в растворе с нитратом свинца (II). при этом образуется темно-коричневый (почти черный) осадок, нерастворимый ни в воде, ни в минеральных кислотах:
H 2 S + Pb(NO 3 ) 2 = PbS + 2HNO 3
Взаимодействие с нитратом свинца в растворе – это качественная реакция на сероводород и сульфид-ионы.
Сероводород – восстановитель
Сероводород H 2 S – очень сильный восстановитель за счет серы в степени окисления -2.
1) При недостатке кислорода и в растворе H 2 S окисляется до свободной серы (раствор мутнеет):
2H 2 S + O 2 (нед.) = 2S↓ +2H 2 O
В избытке кислорода:
2H 2 S + 3O 2 (изб.) = 2SO 2 ↑ + 2H 2 O
2) Как сильный восстановитель, сероводород легко окисляется под действием окислителей.
Бром и хлор окисляют сероводород до молекулярной серы:
H 2 S -2 + Br 2 = S 0 + 2HBr
Br 2 — бромная вода — обесцвечивается
H 2 S + Cl 2 = 2HCl + S↓
Под действием избытка хлора в водном растворе сероводород окисляется до серной кислоты:
H 2 S + 4Cl 2 + 4H 2 O → H 2 SO 4 + 8HCl
Азотная кислота окисляет сероводород до молекулярной серы:
H 2 S + 2HNO 3(конц.) = S + 2NO 2 + 2H 2 O
При кипячении сера окисляется до серной кислоты:
H 2 S + 8HNO 3(конц.) = H 2 SO 4 + 8NO 2 + 4H 2 O
Прочие окислители окисляют сероводород, как правило, до молекулярной серы.
Оксид серы (IV) окисляет сероводород:
2H 2 S + SO 2 = 3S + 2H 2 O
Соединения железа (III) также окисляют сероводород:
H 2 S + 2FeCl 3 = 2FeCl 2 + S + 2HCl
Бихроматы, хроматы и прочие окислители также окисляют сероводород до молекулярной серы:
3H 2 S + K 2 Cr 2 O 7 + 4H 2 SO 4 = 3S + Cr 2 (SO 4 ) 3 + K 2 SO 4 + 7H 2 O
2H 2 S + 4Ag + O 2 = 2Ag 2 S + 2H 2 O
Интересно! Серебряные и медные монеты чернеют на воздухе и в воде, если в среде содержится сероводород:
Серная кислота окисляет сероводород либо до молекулярной серы:
H 2 S + H 2 SO 4(конц.) = S + SO 2 + 2H 2 O
Либо до оксида серы (IV):
H 2 S + 3H 2 SO 4(конц.) = 4SO 2 + 4H 2 O
СУЛЬФИДЫ
Сульфиды – это бинарные соединения серы и металлов или некоторых неметаллов, соли сероводородной кислоты.
По растворимости в воде и кислотах сульфиды разделяют на растворимые в воде, нерастворимые в воде, но растворимые в минеральных кислотах, нерастворимые ни в воде, ни в минеральных кислотах, гидролизуемые водой.
Чёрные сульфиды (CuS, HgS, PbS, Ag 2 S, NiS, CoS)
Белые и цветные сульфиды (ZnS, MnS, FeS, CdS)
ПОЛУЧЕНИЕ СУЛЬФИДОВ
1) Сульфиды получают при взаимодействии серы с металлами . При этом сера проявляет свойства окислителя.
2) Растворимые сульфиды можно получить при взаимодействии сероводорода и щелочей
H 2 S + 2KOH = K 2 S + 2H 2 O
3) Нерастворимые сульфиды получают взаимодействием растворимых сульфидов с солями или взаимодействием сероводорода с солями (только черные сульфиды)
Pb(NO 3 ) 2 + Н 2 S = 2НNO 3 + PbS
ZnSO 4 + Na 2 S = Na 2 SO 4 + ZnS
ХИМИЧЕСКИЕ СВОЙСТВА СУЛЬФИДОВ
1) Гидролиз. Растворимые сульфиды гидролизуются по аниону, среда водных растворов сульфидов щелочная:
Na 2 S+H 2 O↔NaHS+NaOH;
2) С растворами кислот. Сульфиды металлов, расположенных в ряду напряжений левее железа (включительно), растворяются в сильных минеральных кислотах.
CaS + 2HCl = CaCl 2 + H 2 S↑
3) С концентрированными кислотами. Нерастворимые сульфиды растворяются в концентрированной азотной кислоте или концентрированной серной кислоте. При этом сера окисляется либо до простого вещества, либо до сульфата.
CuS + 8HNO 3 = CuSO 4 + 8NO 2 + 4H 2 O
или горячей концентрированной серной кислоте:
CuS + 4H 2 SO 4(конц. гор.) = CuSO 4 + 4SO 2 + 4H 2 O
4) Сульфиды проявляют восстановительные свойства и окисляются пероксидом водорода, хлором и другими окислителями.
Сульфид свинца (II) окисляется пероксидом водорода до сульфата свинца (II):
PbS + 4H 2 O 2 = PbSO 4 + 4H 2 O
Сульфид меди (II) окисляется хлором:
СuS + Cl 2 = CuCl 2 + S
5) Обжиг сульфидов. При этом образуются оксиды металла и серы (IV).
2CuS + 3O 2 = 2CuO + 2SO 2
2Cr 2 S 3 + 9O 2 = 2Cr 2 O 3 + 6SO 2
2ZnS + 3O 2 = 2SO 2 + ZnO
6) Реакции сульфидов с растворимыми солями свинца, серебра, меди используют как качественные на ион S 2−
Сульфиды свинца, серебра и меди — черные осадки, нерастворимые в воде и минеральных кислотах:
Na 2 S + Pb(NO 3 ) 2 = PbS↓ + 2NaNO 3
Na 2 S + 2AgNO 3 = Ag 2 S↓ + 2NaNO 3
Na 2 S + Cu(NO 3 ) 2 = CuS↓ + 2NaNO 3
7) Необратимый гидролиз
Al 2 S 3 + 6H 2 O = 2Al(OH) 3 + 3H 2 S
Разложение происходит и при взаимодействии солей трехвалентных металлов с сульфидами щелочных металлов.
3Na 2 S + 2AlCl 3 + 6H 2 O = 2Al(OH) 3 + 3H 2 S + 6NaCl
http://studarium.ru/article/173
http://www.sites.google.com/site/himulacom/%D0%B7%D0%B2%D0%BE%D0%BD%D0%BE%D0%BA-%D0%BD%D0%B0-%D1%83%D1%80%D0%BE%D0%BA/11-%D0%BA%D0%BB%D0%B0%D1%81%D1%81-%D1%87%D0%B5%D1%82%D0%B2%D1%91%D1%80%D1%82%D1%8B%D0%B9-%D0%B3%D0%BE%D0%B4-%D0%BE%D0%B1%D1%83%D1%87%D0%B5%D0%BD%D0%B8%D1%8F/%D1%83%D1%80%D0%BE%D0%BA-12-%D1%81%D0%B5%D1%80%D0%BE%D0%B2%D0%BE%D0%B4%D0%BE%D1%80%D0%BE%D0%B4-%D1%81%D1%83%D0%BB%D1%8C%D1%84%D0%B8%D0%B4%D1%8B