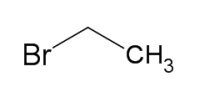
Как из этилена получить бромэтан?
Химия | 10 — 11 классы
Как из этилена получить бромэтан.
C2H4 + Br2 — > ; C2H3Br + HBr.
Иодметан — этан — бромэтан — этилен — 1, 2 — дибромэтан?
Иодметан — этан — бромэтан — этилен — 1, 2 — дибромэтан.
3. Напишите уравнения реакций для следующих превращений : Глюкоза→этанол→этилен→бромэтан→бутан?
3. Напишите уравнения реакций для следующих превращений : Глюкоза→этанол→этилен→бромэтан→бутан.
Этилен — бромэтан — бутан — бутадиен — 1?
Этилен — бромэтан — бутан — бутадиен — 1.
Как из метана получить бромэтан очень срочно?
Как из метана получить бромэтан очень срочно.
Как из этана получить бромэтан?
Как из этана получить бромэтан?
Напишите уравнение реакций, с помощью которых можно осуществить цепочку превращения веществ : этан→этилен→этиловый спирт→бромэтан?
Напишите уравнение реакций, с помощью которых можно осуществить цепочку превращения веществ : этан→этилен→этиловый спирт→бромэтан.
Как из этена получить?
Как из этена получить.
Помогите, пожалуйста?
Очень нужно Решите цепочку превращения веществ : Этилен → этанол → бромэтан → этанол → этаналь.
Как получить ацетальдегид из 1 — бромэтана?
Как получить ацетальдегид из 1 — бромэтана?
Подробно, если можно.
Сколько граммов бромоводорода потребуется для получения 18?
Сколько граммов бромоводорода потребуется для получения 18.
8г бромэтена из ацетилена.
21г бромэтана из этилена?
На этой странице сайта размещен вопрос Как из этилена получить бромэтан? из категории Химия с правильным ответом на него. Уровень сложности вопроса соответствует знаниям учеников 10 — 11 классов. Здесь же находятся ответы по заданному поиску, которые вы найдете с помощью автоматической системы. Одновременно с ответом на ваш вопрос показаны другие, похожие варианты по заданной теме. На этой странице можно обсудить все варианты ответов с другими пользователями сайта и получить от них наиболее полную подсказку.
3NH₃ + H₃PO₄ = (NH₄)₃PO₄ m = 200 г w = 0, 147 масса фосфорной кислоты m(H₃PO₄) = mw m(NH₃) / 3M(NH₃) = m(H₃PO₄) / M(H₃PO₄) масса аммиака m(NH₃) = 3M(NH₃)mw / M(H₃PO₄) m(NH₃) = 3 * 17г / моль * 200г * 0, 147 / (98г / моль) = 15, 3 г.
; ) ; ) ; ) ; ) ; ) к огэ готовишься? 10) 1. 11) 1. 12) 2. 13) 1. Слушай, я сама по химии огэ пишу и задания 11 и 12 я не очень то уверена ; ))) так что.
Acetyl
Наведите курсор на ячейку элемента, чтобы получить его краткое описание.
Чтобы получить подробное описание элемента, кликните по его названию.
| H + | Li + | K + | Na + | NH4 + | Ba 2+ | Ca 2+ | Mg 2+ | Sr 2+ | Al 3+ | Cr 3+ | Fe 2+ | Fe 3+ | Ni 2+ | Co 2+ | Mn 2+ | Zn 2+ | Ag + | Hg 2+ | Pb 2+ | Sn 2+ | Cu 2+ | |
| OH — | Р | Р | Р | Р | Р | М | Н | М | Н | Н | Н | Н | Н | Н | Н | Н | — | — | Н | Н | Н | |
| F — | Р | М | Р | Р | Р | М | Н | Н | М | М | Н | Н | Н | Р | Р | Р | Р | Р | — | Н | Р | Р |
| Cl — | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Н | Р | М | Р | Р |
| Br — | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Н | М | М | Р | Р |
| I — | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | ? | Р | ? | Р | Р | Р | Р | Н | Н | Н | М | ? |
| S 2- | М | Р | Р | Р | Р | — | — | — | Н | — | — | Н | — | Н | Н | Н | Н | Н | Н | Н | Н | Н |
| HS — | Р | Р | Р | Р | Р | Р | Р | Р | Р | ? | ? | ? | ? | ? | Н | ? | ? | ? | ? | ? | ? | ? |
| SO3 2- | Р | Р | Р | Р | Р | Н | Н | М | Н | ? | — | Н | ? | Н | Н | ? | М | М | — | Н | ? | ? |
| HSO3 — | Р | ? | Р | Р | Р | Р | Р | Р | Р | ? | ? | ? | ? | ? | ? | ? | ? | ? | ? | ? | ? | ? |
| SO4 2- | Р | Р | Р | Р | Р | Н | М | Р | Н | Р | Р | Р | Р | Р | Р | Р | Р | М | — | Н | Р | Р |
| HSO4 — | Р | Р | Р | Р | Р | Р | Р | Р | — | ? | ? | ? | ? | ? | ? | ? | ? | ? | ? | Н | ? | ? |
| NO3 — | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | — | Р |
| NO2 — | Р | Р | Р | Р | Р | Р | Р | Р | Р | ? | ? | ? | ? | Р | М | ? | ? | М | ? | ? | ? | ? |
| PO4 3- | Р | Н | Р | Р | — | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н |
| CO3 2- | Р | Р | Р | Р | Р | Н | Н | Н | Н | ? | ? | Н | ? | Н | Н | Н | Н | Н | ? | Н | ? | Н |
| CH3COO — | Р | Р | Р | Р | Р | Р | Р | Р | Р | — | Р | Р | — | Р | Р | Р | Р | Р | Р | Р | — | Р |
| SiO3 2- | Н | Н | Р | Р | ? | Н | Н | Н | Н | ? | ? | Н | ? | ? | ? | Н | Н | ? | ? | Н | ? | ? |
| Растворимые (>1%) | Нерастворимые ( Спасибо! Ваша заявка отправлена, преподаватель свяжется с вами в ближайшее время. Вы можете также связаться с преподавателем напрямую: 8(906)72 3-11-5 2 Скопируйте эту ссылку, чтобы разместить результат запроса » » на другом сайте. Изображение вещества/реакции можно сохранить или скопировать, кликнув по нему правой кнопкой мыши. Если вы считаете, что результат запроса » » содержит ошибку, нажмите на кнопку «Отправить». Этим вы поможете сделать сайт лучше. К сожалению, регистрация на сайте пока недоступна. На сайте есть сноски двух типов: Подсказки — помогают вспомнить определения терминов или поясняют информацию, которая может быть сложна для начинающего. Дополнительная информация — такие сноски содержат примечания или уточнения, выходящие за рамки базовой школьной химии, нужны для углубленного изучения. Здесь вы можете выбрать параметры отображения органических соединений. Бромэтан
Бромэтан (бромистый этил, этилбромид) C2H5Br — прозрачная бесцветная или слегка желтоватая токсичная жидкость с запахом хлороформа. Содержание
ПолучениеПри промышленном производстве бромистый этил получают из этилена: В лабораторных условиях бромэтил получают действием бромоводорода на этанол. Чаще всего бромоводород получают in situ из бромида калия и серной кислоты: Другие лабораторные способы: Способы получения, редко используемые на практике: Физические свойстваБромэтил — прозрачная бесцветная или слегка желтоватая жидкость с запахом хлороформа. Под действием света и воздуха (кислорода) легко разлагается, поэтому его следует хранить в герметически закупоренных темных склянках. Химические свойстваВ воде, как и многие галогенопроизводные, медленно гидролизуется: С водными щелочами взаимодействие идёт быстрее и двумя путями: ПрименениеПрименяется в медицинской промышленности, в производстве этиловой жидкости, как химсырье органического синтеза, а также в качестве рабочего вещества или компонента в автоматических системах пожаротушения, наркотик с узким терапевтическим диапазоном, вызывает повреждение миокарда. ТоксичностьБромэтан в больших количествах весьма токсичен. При остром отравлении наблюдаются наркотическое состояние, тахикардия, цианоз, коллапс. ЛК50: 36 мг/л (белые мыши, экспозиция 2 ч.), 53 мг/л (белые крысы, экспозиция 4 ч.). источники: http://acetyl.ru/o/a21h3.php http://chem.ru/bromjetan.html | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||