Сульфид калия: способы получения и химические свойства
Сульфид калия K2S — белое вещество, плавится без разложения. Термически устойчивый. Хорошо растворяется в воде.
Относительная молекулярная масса Mr = 110,26; относительная плотность для тв. и ж. состояния d = 1,74; tпл = 912º C.
Способ получения
1. Сульфид калия можно получить путем взаимодействия калия и серы при температуре 100 — 200º C:
2K + S = K2S
2. При взаимодействии с углеродом (коксом) сульфат калия при температуре 900º C образует сульфид калия и угарный газ:
3. При температуре 600º C в присутствии оксида железа (III) сульфат калия реагирует с водородом . Взаимодействие сульфата калия с водородом приводит к образованию сульфида калия и воды:
Качественная реакция
Качественная реакция на сульфид калия — взаимодействие его с хлоридом меди, в результате реакции происходит образование черного осадка:
1. При взаимодействии с хлоридом меди , сульфид калия образует осадок сульфид меди и хлорид калия:
CuCl2 + K2S = CuS↓ + 2KCl
Химические свойства
1. Сульфид калия может реагировать с простыми веществами :
Твердый сульфид калия реагирует с кислородом при температуре выше 500º C. При этом образуется сульфат калия:
2. Сульфид калия вступает в реакцию со многими сложными веществами :
2.1. Сульфид калия способен реагировать со многими кислотами :
2.1.1. Сульфид калия реагирует с разбавленной хлороводородной кислотой . Взаимодействие сульфида калия с хлороводородной кислотой приводит к образованию хлорида калия и газа сероводорода:
K2S + 2HCl = 2KCl + H2S↑
2.1.2. Сульфид калия взаимодействует с концентрированной серной кислотой . При этом образуются гидросульфат калия, газ оксид серы, осадок сера и вода:
2.1.3. При взаимодействии сульфида калия с концентрированной азотной кислотой выделяются нитрат калия, газ оксид азота, сера и вода:
2.1.4 . Взаимодействуя с насыщенной сероводородной кислотой холодный сульфид калия образует гидросульфид калия:
Сульфид калия
| Сульфид калия | |
|---|---|
 | |
| Систематическое наименование | калия сульфид |
| Традиционные названия | калий сернистый, сульфид калия, калия моносульфид |
| Хим. формула | K2S |
| Состояние | бесцветный порошок с запахом тухлых яиц |
| Молярная масса | 110,262 г/моль |
| Плотность | 1,805 г/см³ |
| Температура | |
| • плавления | 471; 948 °C |
| Мол. теплоёмк. | 76,15 Дж/(моль·К) |
| Энтальпия | |
| • образования | −387,3 кДж/моль |
| Растворимость | |
| • в воде | растворяется с образованием KSH, KOH |
| • в остальных веществах | растворяется в этаноле и глицерине |
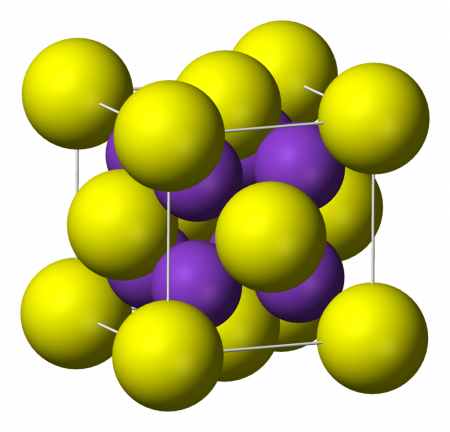
| Кристаллическая структура | кубическая сингония |
| Рег. номер CAS | 1312-73-8 |
| PubChem | 14800 |
| Рег. номер EINECS | 215-197-0 |
| SMILES | |
| RTECS | TT6000000 |
| ChemSpider | 14116 |
| Пиктограммы ECB |   |
| Приведены данные для стандартных условий (25 °C, 100 кПа), если не указано иное. | |
Калия сульфид — бинарное неорганическое химическое соединение калия с серой. Представляет собой соединение с формулой K2S.
Содержание
- 1 Физические свойства
- 2 Получение
- 3 Химические свойства
- 4 Применение
- 4.1 В пиротехническом деле
Физические свойства
Сульфид калия K2S — бесцветные кубические кристаллы (a = 0,739 нм, Z=4; пространственная группа Fm3m). Хорошо растворимы в воде (с гидролизом). Растворим в спирте и глицерине. Гигроскопичен, образует ди- и пентагидраты.
Получение
Прямой синтез из элементов:
2K + S → 100−200oC K2S
Восстановление сульфата калия водородом:
или углеродом (в промышленности — кокс):
Сульфит калия при нагревании диспропорционирует:
Химические свойства
На воздухе медленно окисляется:
в зависимости от условий проведения этой реакции образуются побочные продукты: коллоидная сера, полисульфиды калия.
Сульфид калия при поджигании сгорает:
Так как сероводород является слабой кислотой, то сульфид калия разлагается кислотами:
Концентрированные кислоты могут окислять выделяемый сероводород:
При кипячении раствора сульфида калия с серой или сплавления его с серой образуются полисульфиды:
для калия выделены полисульфиды вплоть до n = 6.
При пропускании через раствор сульфида калия избытка сероводорода образуются гидросульфид калия:
Реагирует, образовывая соединения с сульфидами Ag, Sn и другими.
Применение
Калия сульфид компонент светочувствительных эмульсий в фотографии, аналитический реагент для разделения сульфидов металлов, является компонентом входящим в состав для удаления наружного слоя шкур.
В пиротехническом деле
Сульфид калия образуется при сжигании пороха.
Напишите уравнения не менее трех реакций, с помощью которых можно получить сульфид калия.
Ваш ответ
Похожие вопросы
- Все категории
- экономические 43,296
- гуманитарные 33,622
- юридические 17,900
- школьный раздел 607,211
- разное 16,830
Популярное на сайте:
Как быстро выучить стихотворение наизусть? Запоминание стихов является стандартным заданием во многих школах.
Как научится читать по диагонали? Скорость чтения зависит от скорости восприятия каждого отдельного слова в тексте.
Как быстро и эффективно исправить почерк? Люди часто предполагают, что каллиграфия и почерк являются синонимами, но это не так.
Как научится говорить грамотно и правильно? Общение на хорошем, уверенном и естественном русском языке является достижимой целью.
http://chem.ru/sulfid-kalija.html
http://www.soloby.ru/1386703/%D0%BD%D0%B0%D0%BF%D0%B8%D1%88%D0%B8%D1%82%D0%B5-%D1%83%D1%80%D0%B0%D0%B2%D0%BD%D0%B5%D0%BD%D0%B8%D1%8F-%D1%80%D0%B5%D0%B0%D0%BA%D1%86%D0%B8%D0%B9-%D0%BF%D0%BE%D0%BC%D0%BE%D1%89%D1%8C%D1%8E-%D0%BA%D0%BE%D1%82%D0%BE%D1%80%D1%8B%D1%85-%D0%BF%D0%BE%D0%BB%D1%83%D1%87%D0%B8%D1%82%D1%8C-%D1%81%D1%83%D0%BB%D1%8C%D1%84%D0%B8%D0%B4