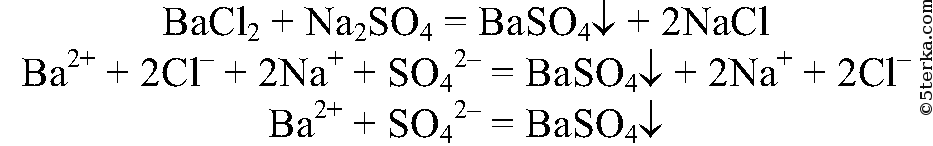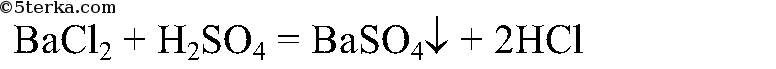Как распознать сульфат натрия уравнение

Определим, в какой из колб находятся растворы хлорида натрия NaCl , карбоната натрия Na 2 CO 3 и сульфата натрия Na 2 SO 4 . Карбонат натрия можно обнаружить по карбонат-иону с помощью раствора соляной кислоты HCl . Карбонат натрия находится в той пробирке, где выделяется газ.
В какой из оставшихся двух пробирок хлорид натрия? Качественная реакция на хлорид-ион – реакция с нитратом серебра AgNO 3 . Белый осадок хлорида серебра выпадает в той пробирке, где находится хлорид натрия.
Убедимся в том, что в оставшейся пробирке сульфат натрия. При добавлении хлорида бария выпадает белый осадок. Это сульфат бария.
Значит, в пробирке был действительно сульфат натрия.
Оборудование: колбы, пробирки, штатив для пробирок, пипетки.
Соблюдать правила работы с кислотами и ядовитыми веществами – хлоридом бария и нитратом серебра. Остерегаться попадания на кожу и слизистые оболочки.
Постановка опыта – Елена Махиненко, текст – к.п.н. Павел Беспалов.
Сульфат натрия: способы получения и химические свойства
Сульфат натрия — соль щелочного металла натрия и серной кислоты. Белый. Плавится и кипит без разложения. Хорошо растворяется в воде (гидролиз не идет).
Относительная молекулярная масса Mr = 142,04; относительная плотность для тв. и ж. состояния d = 2,66; tпл = 884º C; tкип = 1430º C.
Способ получения
1. В результате взаимодействия разбавленной серной кислоты и гидроксида натрия образуется сульфат натрия и вода:
2. При температуре 450–800º C гидросульфат натрия реагирует с хлоридом натрия. В результате реакции образуется сульфат натрия и хлороводородная кислота:
NaHSO4 + NaCl = Na2SO4 + HCl
3. В состоянии кипения в результате реакции между твердым хлоридом натрия и концентрированной серной кислотой происходит образование сульфата натрия и газа хлороводорода:
4. Твердый сульфид натрия и кислород взаимодействуют при температуре выше 400º C с образованием сульфата натрия:
5. При взаимодействии концентрированного раствора пероксида водорода и сульфида натрия образуется сульфат натрия и вода:
Качественная реакция
Качественная реакция на сульфат натрия — взаимодействие его с хлоридом бария, в результате реакции происходит образование белого осадка , который не растворим в азотной кислоте:
1. При взаимодействии с хлоридом бария , сульфат натрия образует сульфат бария и хлорид натрия:
Химические свойства
1. Сульфат натрия может реагировать с простыми веществами :
1.1. Сульфат натрия реагирует со фтором при температуре 100–150º C. При этом образуются фторид натрия, сульфурилфторид и кислород:
1.2. С водородом сульфат натрия реагирует при температуре 550–600º C, в присутствии катализатора Fe2O3 с образованием сульфида натрия и воды:
2. Сульфат натрия вступает в реакцию со многими сложными веществами :
2.1. Сульфат натрия реагирует с гидроксидом бария с образованием гидроксида натрия и сульфата бария:
2.2. При взаимодействии с концентрированной серной кислотой твердый сульфат натрия образует гидросульфат натрия:
2.3. Сульфат натрия реагирует с оксидом серы (VI) . Взаимодействие сульфата натрия с оксидом серы (VI) приводит к образованию пиросульфата натрия:
2.4. Сульфат натрия взаимодействует с хлоридом бария . При этом образуются хлорид натрия и сульфат бария:
Опыт № 5. Распознавание сульфатов
Задание. Распознайте сульфат натрия с помощью качественной реакции.
Соблюдайте правила техники безопасности при работе с кислотами!
Оборудование. Штатив с пробирками.
Вещества. 5% -е растворы сульфата, хлорида и нитрата натрия, 10% -е растворы хлорида бария, серной, соляной и азотной кислот, порошок медного купороса, вода (в стакане).
1. В три пробирки налейте по 1 мл растворов сульфата натрия, хлорида натрия и нитрата натрия. В каждую из этих пробирок добавьте немного хлорида бария. Что вы наблюдаете?
Составьте полные и сокращенные ионные уравнения наблюдаемых реакций.
2. Докажите, что выданные вам голубые кристаллы содержат сульфат меди (II). Составьте уравнения реакций.
3. Налейте в три пробирки серную, азотную и соляную кислоты, добавьте в них раствор хлорида бария. Что вы наблюдаете? Напишите уравнения реакций.
Сделайте общий вывод, с помощью какого реактива можно распознать сульфат-ионы.
Наблюдается появление белого осадка в пробирке с сульфатом натрия. В других пробирках видимых изменений не наблюдается.
В пробирке с серной кислотой выпадет белый осадок. В других пробирках ничего не происходит.
Вывод: сульфат-ионы распознаются с помощью растворимых солей бария.
задача №5
к главе «Лабораторные работы и опыты».
http://chemege.ru/sulfat-natriya/
http://5terka.com/node/10057