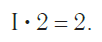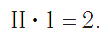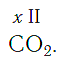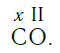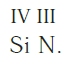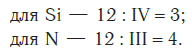Урок 6. Валентность
В уроке 6 «Валентность» из курса «Химия для чайников» дадим определение валентности, научимся ее определять; рассмотрим элементы с постоянной и переменной валентностью, кроме того научимся составлять химические формулы по валентности. Напоминаю, что в прошлом уроке «Химическая формула» мы дали определение химическим формулам и их индексам, а также выяснили различия химических формул веществ молекулярного и немолекулярного строения.
Вы уже знаете, что в химических соединениях атомы разных элементов находятся в определенных числовых соотношениях. От чего зависят эти соотношения?
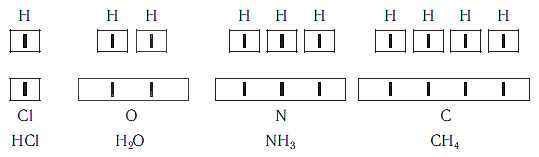
Рассмотрим химические формулы нескольких соединений водорода с атомами других элементов:
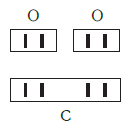
Нетрудно заметить, что атом хлора связан с одним атомом водорода, атом кислорода — с двумя, атом азота — с тремя, а атом углерода — с четырьмя атомами водорода. В то же время в молекуле углекислого газа СО2 атом углерода связан с двумя атомами кислорода. Из этих примеров видно, что атомы обладают разной способностью соединяться с другими атомами. Такая способность атомов выражается с помощью численной характеристики, называемой валентностью.
Валентность — численная характеристика способности атомов данного элемента соединяться с другими атомами.
Поскольку один атом водорода может соединиться только с одним атомом другого элемента, валентность атома водорода принята равной единице. Иначе говорят, что атом водорода обладает одной единицей валентности, т. е. он одновалентен.
Валентность атома какого-либо другого элемента равна числу соединившихся с ним атомов водорода. Поэтому в молекуле HCl у атома хлора валентность равна единице, а в молекуле H2O у атома кислорода валентность равна двум. По той же причине в молекуле NH3 валентность атома азота равна трем, а в молекуле CH4 валентность атома углерода равна четырем. Если условно обозначить единицу валентности черточкой |, вышесказанное можно изобразить схематически:
Следовательно, валентность атома любого элемента есть число, которое показывает, со сколькими атомами одновалентного элемента связан данный атом в химическом соединении.
Численные значения валентности обозначают римскими цифрами над символами химических элементов:
Определение валентности
Однако водород образует соединения далеко не со всеми элементами, а вот кислородные соединения есть почти у всех элементов. И во всех таких соединениях атомы кислорода проявляют валентность, равную двум. Зная это, можно определять валентности атомов других элементов в их бинарных соединениях с кислородом. (Бинарными называются соединения, состоящие из атомов двух химических элементов.)
Чтобы это сделать, необходимо соблюдать простое правило: в химической формуле вещества суммарные числа единиц валентности атомов каждого элемента должны быть одинаковыми.
Так, в молекуле воды H2O общее число единиц валентности двух атомов водорода равно произведению валентности одного атома на соответствующий числовой индекс в формуле:
Так же определяют число единиц валентности атома кислорода:
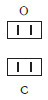
По величине валентности атомов одного элемента можно определить валентность атомов другого элемента. Например, определим валентность атома углерода в молекуле углекислого газа СО2:
Согласно вышеприведенному правилу х ·1 = II · 2 , откуда х = IV .
Существует и другое соединение углерода с кислородом — угарный газ СО, в молекуле которого атом углерода соединен только с одним атомом кислорода:
В этом веществе валентность углерода равна II , так как х ·1 = II · 1 , откуда х = II :
Постоянная и переменная валентность
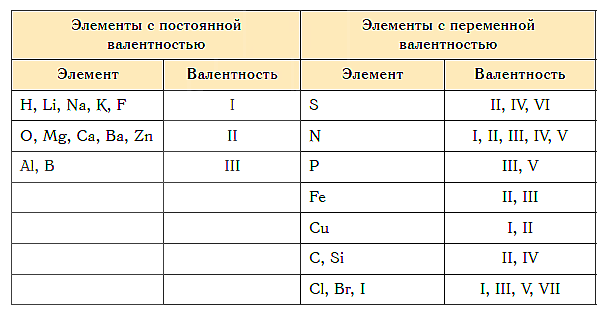
Как видим, углерод соединяется с разным числом атомов кислорода, т. е. имеет переменную валентность. У большинства элементов валентность — величина переменная. Только у водорода, кислорода и еще нескольких элементов она постоянна (см. таблицу).
Составление химических формул по валентности
Зная валентность элементов, можно составлять формулы их бинарных соединений. Например, необходимо записать формулу кислородного соединения хлора, в котором валентность хлора равна семи. Порядок действий здесь таков.
Еще один пример. Составим формулу соединения кремния с азотом, если валентность кремния равна IV , а азота — III .
Записываем рядом символы элементов в следующем виде:
Затем находим НОК валентностей обоих элементов. Оно равно 12 ( IV·III ).
Определяем индексы каждого элемента:
Записываем формулу соединения: Si3N4.
В дальнейшем при составлении формул веществ не обязательно указывать цифрами значения валентностей, а необходимые несложные вычисления можно выполнять в уме.
Краткие выводы урока:
- Численной характеристикой способности атомов данного элемента соединяться с другими атомами является валентность.
- Валентность водорода постоянна и равна единице. Валентность кислорода также постоянна и равна двум.
- Валентность большинства остальных элементов не является постоянной. Ее можно определить по формулам их бинарных соединений с водородом или кислородом.
Надеюсь урок 6 «Валентность» был понятным и познавательным. Если у вас возникли вопросы, пишите их в комментарии.
Химические уравнения Урок-исследование • 8 класс
Обращаем Ваше внимание, что в соответствии с Федеральным законом N 273-ФЗ «Об образовании в Российской Федерации» в организациях, осуществляющих образовательную деятельность, организовывается обучение и воспитание обучающихся с ОВЗ как совместно с другими обучающимися, так и в отдельных классах или группах.
Урок-исследование • 8 класс
Цели. Познакомить учащихся с понятием «химическое уравнение», научить составлять уравнения реакций, закрепить навыки составления формул по валентности элементов, стимулировать познавательную деятельность учащихся через дидактические игры, настроить их на использование имеющихся знаний для изучения нового материала.
Мотивация. Что такое химические уравнения и зачем они нужны?
Оборудование и реактивы (на столе учителя). Спиртовка, держатель; железо, сера.
Ориентация . Ау! Где мы находимся? (Учащиеся знают химические формулы веществ, понятие «химическая реакция», но пока не умеют записывать уравнения реакций.)
Целеполагание (чем конкретно займемся на уроке).
Мотивация (зачем нужны химические уравнения).
Вы – исследователи, которым необходимо ответить на один-единственный вопрос: что такое химическое уравнение?
В нашу исследовательскую лабораторию пришел заказ изучить и создать общее представление о химическом уравнении.
Разминка для эрудитов
1. Что изучает химия?
2. Что такое вещество?
(Это определенный вид материи, то,
из чего состоит тело.
Примеры веществ – сера, железо, вода.)
3. Как мы выражаем состав вещества?
(С помощью химических формул.)
4. Как составить химическую формулу? Что для этого необходимо знать?
(Химические знаки элементов, валентность.)
5. Что такое валентность?
(Это свойство атома присоединять
определенное число других атомов.)
Повторим валентности некоторых элементов (игра в мяч). Один ученик бросает мяч другому и называет химический элемент из ряда: H, O, S, Fe, Cu, Al, Na, Cl. Ученик, который ловит мяч, называет валентность данного элемента.
К нам пришла телеграмма, но запись на ней частично исчезла, необходимо ее восстановить:
В этом задании требуется определить валентности элементов, а затем расставить индексы в химических формулах. Работаем по восстановлению записи. Ученик, который справится с заданием быстрее всех, записывает на доске ответ:
При этом он вслух проговаривает алгоритм составлений формул по валентности: что он делает сначала, откуда берет значения валентности элементов, как составляет формулу по валентности.
А что вам известно об уравнении вообще? На каких предметах вы встречались с уравнениями? (Учащиеся говорят, что используют уравнения на математике и физике.)
Уравнение – это математическое равенство с одной или несколькими неизвестными величинами. Что такое, по-вашему, химическое уравнение? (Версии учащихся.)
Демонстрационный опыт.
Взаимодействие железа с серой
Возьмем железо и серу в соотношении по массе 7:4. В семи частях железа находится столько же атомов, сколько в четырех частях серы. Нагреем смесь. Что произошло? (Протекает химическая реакция.)
По каким признакам мы судим, что произошла реакция? Какие условия необходимы для проведения опыта? (Нагревание, тесное соприкосновение исходных веществ.)
Чем отличаются химические реакции от физических явлений? Как можно выразить (записать) химическую реакцию? (В виде химического уравнения.)
Составим уравнение реакции на доске:
Где мы сегодня уже встречали формулу FeS? (В телеграмме.)
Какой закон необходимо применять при составлении химических уравнений? О чем он гласит? (Масса веществ, вступивших в химическую реакцию, равна массе образующихся веществ.)
Лабораторный опыт.
Прокаливание медной проволоки
Обозначим медную проволоку знаком Cu, кислород воздуха – О2. Что нужно для составления химического уравнения?
Порядок действий следующий:
а) записать формулы исходных веществ;
б) составить формулу продукта реакции справа от знака равенства;
в) уравнять число атомов в правой и левой частях уравнения по закону сохранения массы веществ:
Сформулируем определение химического уравнения.
Химическое уравнение – это условная запись хода химической реакции с помощью формул и коэффициентов.
К нам пришло письмо. Ученик провел опыт, описал его, но не смог составить уравнение реакции и обратился к нам за помощью. Вот текст письма: «Нагретый железный порошок внесли в колбу с газом желто-зеленого цвета – хлором, молекулы которого двухатомны. Порошок воспламенился, в результате появился коричневый дым, образованный частичками хлорида железа(III)». Давайте поможем ученику. Запишите уравнение реакции:
Итак, сегодня мы узнали, что такое химическое уравнение. На трех примерах рассмотрели, что нужно для составления химического уравнения. Пока остается неясным, зачем нужны уравнения реакций. Вот мы и обозначили задачу, над которой будем работать на последующих уроках.
Самоконтроль и самооценка
Учитель подводит итоги: чему научились на уроке, какие моменты требуют дальнейшей отработки. Выслушивает мнения учащихся по этим вопросам, благодарит их за работу на уроке.
Написание формулы по валентности
Валентность — способность атома присоединять то или иное число других атомов с образованием химической связи (см. «Что такое валентность»).
Для того, чтобы выводить химические формулы веществ по валентности элементов, необходимо знать, как минимум, валентности наиболее часто встречающихся элементов.
Алгоритм написания химической формулы вещества по валентности элементов, входящих в него:
- записать химические знаки элементов, входящих в вещество;
- определить валентность этих элементов;
- найти наименьшее общее кратное для валентностей этих элементов;
- определить индексы для атомов.
Составление формулы оксидов по валентности элементов
В качестве примера составим формулу оксида железа (III).
- В оксид железа входят железо и кислород: Fe O;
- Указываем валентность этих элементов: Fe III O II ;
- Находим наименьшее общее кратное (НОК): 3·2=6;
- Делим НОК на число единиц валентности каждого элемента:
- для Fe — 6:3=2;
- для O — 6:2=3.
- Записываем полученные индексы справа внизу от элемента: Fe2O3.
Составление формулы оснований
Важный нюанс, который неободимо знать — группы атомов могут рассматриваться, как единое целое.
Составление формул оснований по валентности элементов отличается от составления формулы оксидов лишь тем, что вместо атома кислорода в формуле стоит гидроксогруппа OH. В случае, если гидроксогруппа в формуле повторяется несколько раз, она берется в скобки.
В качестве примера составим составим формулу гидроксида магния.
На первом месте в основаниях стоит атом металла, гидроксогруппа — на втором.
Составление формулы солей
В солях «роль» гидроксогруппы OH играют кислотные остатки.
На первом месте в формуле средней соли стоит атом(ы) металла, кислотный остаток — на втором.
В качестве примера составим формулу соли фосфата натрия.
Составление формулы кислот
На первом месте в формуле кислот стоит атом(ы) водорода, кислотный остаток — на втором.
В качестве примера составим формулу серной кислоты.
Потренируемся в решении обратной задачи, когда по готовой формуле надо определить валентность элементов.
Определение валентности по готовой формуле
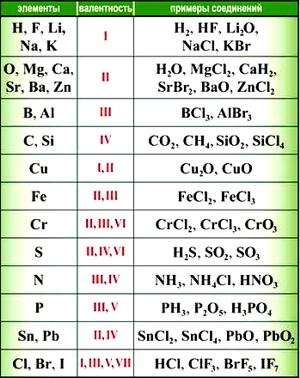
«Фишка» решения подобных задач заключается в том, что некоторые химические элементы в любых соединениях, в которые они входят, имеют постоянную валентность.
Элементы с постоянной валентностью:
- валентность I: H, F, Li, Na, K, Rb, Cs
- валентность II: O, Mg, Ca, Sr, Ba, Zn
- валентность III: Al
Большинство элементов в различных соединениях могут принимать различную валентность,, т. е., образовывать различное число химических связей.
Для нахождения валентности элементов с переменной валентностью в том или ином соединении используют правило валентности.
| x·m=y·n |
| в бинарных соединениях типа AmBn произведение валнетности элемента A(x) на кол-во его атомов m равно произведению валентности элемента B(y) на число его атомов n |
Определим, используя правило валентности, валентность фософра в соединении P2O5.
Поскольку валентность кислорода равна II, то:
Теперь решим ту же задачу, используя алгоритм, описанный выше для выведения формулы по валентности, который будем применять «сзади-наперёд».
Определим валентность фосфора и кислорода в соединении P2O5.
- P2O5
- валентность кислорода равна двум: P2O5 II
- общее число единиц валентности всех атомов вещества будет равно 2·5=10
- делим общее число единиц валентности (10) на индекс кислорода, валентность которого известна: 10:2=5 — это и будет валентность неизвестного, в нашем случае, фосфора
- P2 V O5 II
Немного усложним задачу и определим валентность элементов в соли кислородсодержащей кислоты Al2(SO4)3.
- решение задачи начинается с элемента с известной валентностью, т. е., с кислорода — определяем кол-во его атомов: 4·3=12
- с учётом того, что валентность кислорода равна 2, находим общее число единиц валентности для кислорода: 12·2=24
- по аналогии вычисляем общее число единиц валентности для атомов алюминия (валентность=3): 2·3=6
- от общего числа единиц валентности кислорода вычитаем общее число единиц валентности алюминия: 24-6=18 — это общее число единиц валентности, которое будет приходиться на серу
- по аналогии с кислородом определяем число атомов серы, валентность которой неизвестна: 1·3=3
- чтобы узнать валентность серы следует разделить разность, найденную в п.4, на число атомов серы: 18:3=6
- Al2 III (S VI O4 II )3
Если вам понравился сайт, будем благодарны за его популяризацию 🙂 Расскажите о нас друзьям на форуме, в блоге, сообществе. Это наша кнопочка:
Код кнопки: 
Политика конфиденциальности Об авторе
http://infourok.ru/himicheskie-uravneniya-urok-issledovanie-8-klass-5777771.html
http://prosto-o-slognom.ru/chimia_primery/001-valentnost.html