Характерные химические свойства Be, Mg и щелочноземельных металлов
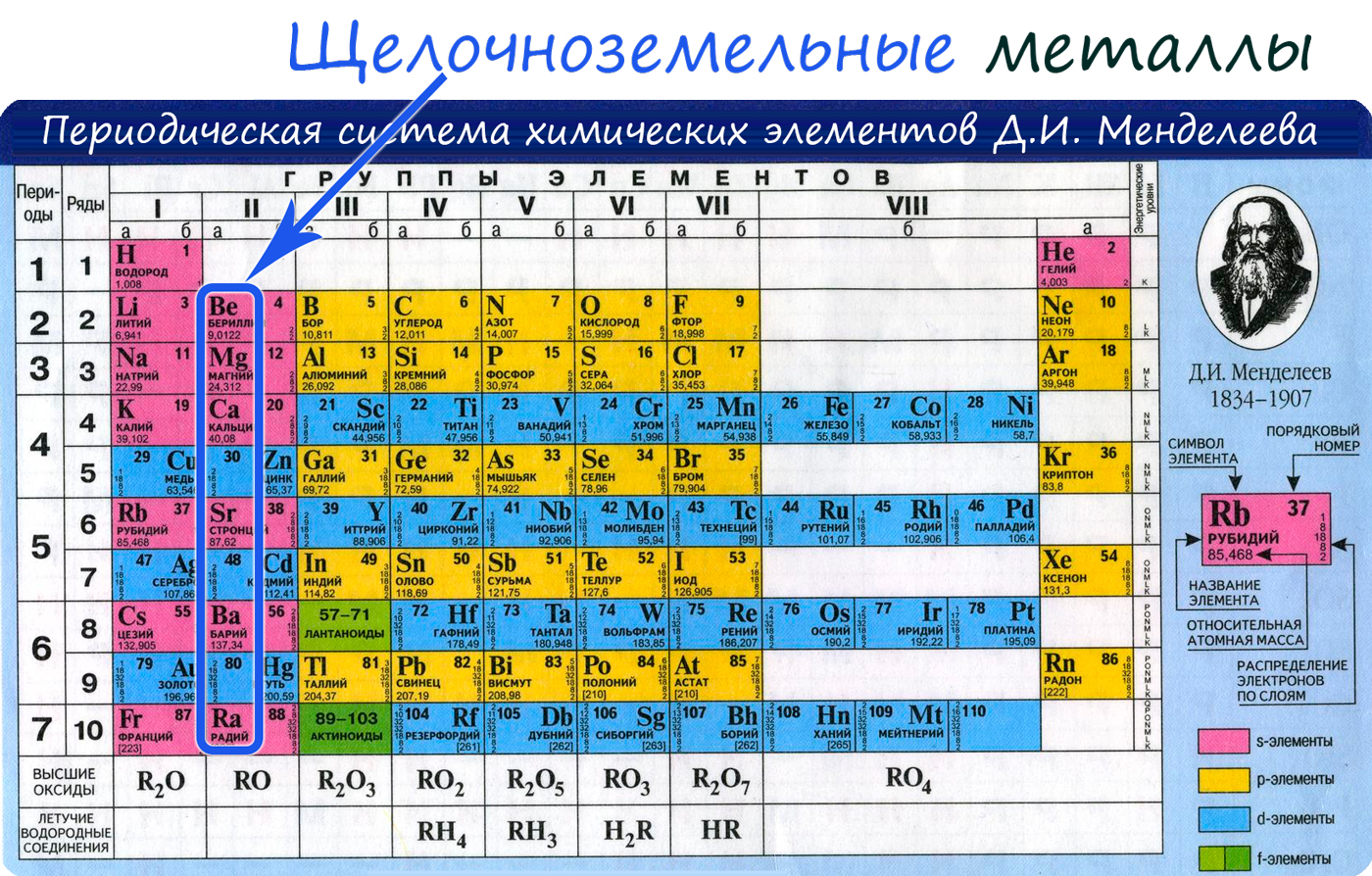
Общая характеристика элементов II а группы
Физические свойства простых веществ
Щелочноземельные металлы (по сравнению со щелочными металлами) обладают более высокими t°пл. и t°кип., потенциалами ионизации, плотностями и твердостью.
Химические свойства щелочноземельных металлов + Be
1. Реакция с водой.
В обычных условиях поверхность Be и Mg покрыты инертной оксидной пленкой, поэтому они устойчивы по отношению к воде. В отличие от них Ca, Sr и Ba растворяются в воде с образованием щелочей:
2. Реакция с кислородом.
Все металлы образуют оксиды RO, барий-пероксид – BaO 2 :
3. С другими неметаллами образуют бинарные соединения:
Be + Cl 2 → BeCl 2 (галогениды)
Ba + S → BaS (сульфиды)
Ca + 2C → CaC 2 (карбиды)
3Ba + 2P → Ba 3 P 2 (фосфиды)
Бериллий и магний сравнительно медленно реагируют с неметаллами.
4. Все щелочноземельные металлы растворяются в кислотах:
5. Бериллий растворяется в водных растворах щелочей:
6. Летучие соединения щёлочноземельных металлов придают пламени характерный цвет:
соединения кальция — кирпично-красный, стронция — карминово-красный, а бария — желтовато-зелёный.


Высокой энергией ионизации атома бериллий заметно отличается от остальных элементов ПА-подгруппы (магния и щелочноземельных металлов). Его химия во многом сходна с химией алюминия (диагональное сходство). Таким образом, это элемент с наличием у его соединений амфотерных качеств, среди которых преобладают все же основные.
Электронная конфигурация Mg: 1s 2 2s 2 2p 6 3s 2 по сравнению с натрием имеет одну существенную особенность: двенадцатый электрон помещается на 2s-орбитали, где уже имеется 1е — .
Ионы магния и кальция ‑ незаменимые элементы жизнедеятельности любой клетки. Их соотношение в организме должно быть строго определённым. Ионы магния участвуют в деятельности ферментов (например, карбоксилазы), кальция – в построении скелета и обмена веществ. Повышение содержания кальция улучшает усвоение пищи. Кальций возбуждает и регулирует работу сердца. Его избыток резко усиливает деятельность сердца. Магний играет отчасти роль антагониста кальция. Введение ионов Mg 2+ под кожу вызывает наркоз без периода возбуждения, паралич мышц, нервов и сердца. Попадая в рану в форме металла, он вызывает долго незаживающие гнойные процессы. Оксид магния в лёгких вызывает так называемую литейную лихорадку. Частый контакт поверхности кожи с его соединениями приводит к дерматитам. Самые широко используемые в медицине соли кальция: сульфат СаSO 4 и хлорид CaCL 2 . Первый используется для гипсовых повязок, а второй применяется для внутривенных вливаний и как внутреннее средство. Он помогает бороться с отёками, воспалениями, аллергией, снимает спазмы сердечно-сосудистой системы, улучшает свертываемость крови.
Все соединения бария, кроме BaSO 4 , ядовиты. Вызывают менегоэнцефалит с поражением мозжечка, поражение гладких сердечных мышц, паралич, а в больших дозах – дегенеративные изменения печени. В малых же дозах соединения бария стимулируют деятельность костного мозга.
При введении в желудок соединений стронция наступает его расстройство, паралич, рвота; поражения по признакам сходны с поражениями от солей бария, но соли стронция менее токсичны. Особую тревогу вызывает появление в организме радиоактивного изотопа стронция 90 Sr. Он исключительно медленно выводится из организма, а его большой период полураспада и, следовательно, длительность действия могут служить причиной лучевой болезни.
Радий опасен для организма своим излучением и огромным периодом полураспада (Т 1/2 = 1617 лет). Первоначально после открытия и получения солей радия в более или менее чистом виде его стали использовать довольно широко для рентгеноскопии, лечения опухолей и некоторых тяжёлых заболеваний. Теперь с появлением других более доступных и дешевых материалов применение радия в медицине практически прекратилось. В некоторых случаях его используют для получения радона и как добавку в минеральные удобрения.
В атоме кальция завершается заполнение 4s-орбитали. Вместе с калием он образует пару s-элементов четвертого периода. Гидроксид кальция ‑ довольно сильное основание. У кальция — наименее активного из всех щелочноземельных металлов — характер связи в соединениях ионный.
По своим характеристикам стронций занимает промежуточное положение между кальцием и барием.
Свойства бария наиболее близки к свойствам щелочных металлов.
Бериллий и магний широко используют в сплавах. Бериллиевые бронзы – упругие сплавы меди с 0,5-3% бериллия; в авиационных сплавах (плотность 1,8) содержится 85-90% магния («электрон»). Бериллий отличается от остальных металлов ИИА группы – не реагирует с водородом и водой, зато растворяется в щелочах, поскольку образует амфотерный гидроксид:
Магний активно реагирует с азотом:
В таблице приведена растворимость гидроксидов элементов II группы.
| Растворимость, моль/л (20 0 С) | Растворимость, г/л |
| Be(OH) 2 Mg(OH) 2 Ca(OH) 2 Sr(OH) 2 Ba ( OH ) 2 Щелочноземельные металлыК щелочноземельным металлам относятся металлы IIa группы: бериллий, магний, кальций, стронций, барий и радий. Отличаются легкостью, мягкостью и сильной реакционной способностью. Общая характеристикаОт Be к Ra (сверху вниз в периодической таблице) происходит увеличение: атомного радиуса, металлических, основных, восстановительных свойств, реакционная способность. Уменьшается электроотрицательность, энергия ионизация, сродство к электрону. Электронные конфигурации у данных элементов схожи, так как они находятся в одной группе (главной подгруппе!), общая формула ns 2 :
Природные соединенияВ природе щелочноземельные металлы встречаются в виде следующих соединений:
ПолучениеЭто активные металлы, которые нельзя получить электролизом раствора. С целью их получения применяют электролиз расплавов, алюминотермию и вытеснением их из солей другими более активными металлами. MgCl2 → (t) Mg + Cl2 (электролиз расплава) CaO + Al → Al2O3 + Ca (алюминотермия — способ получения металлов путем восстановления их оксидов алюминием) Химические свойства
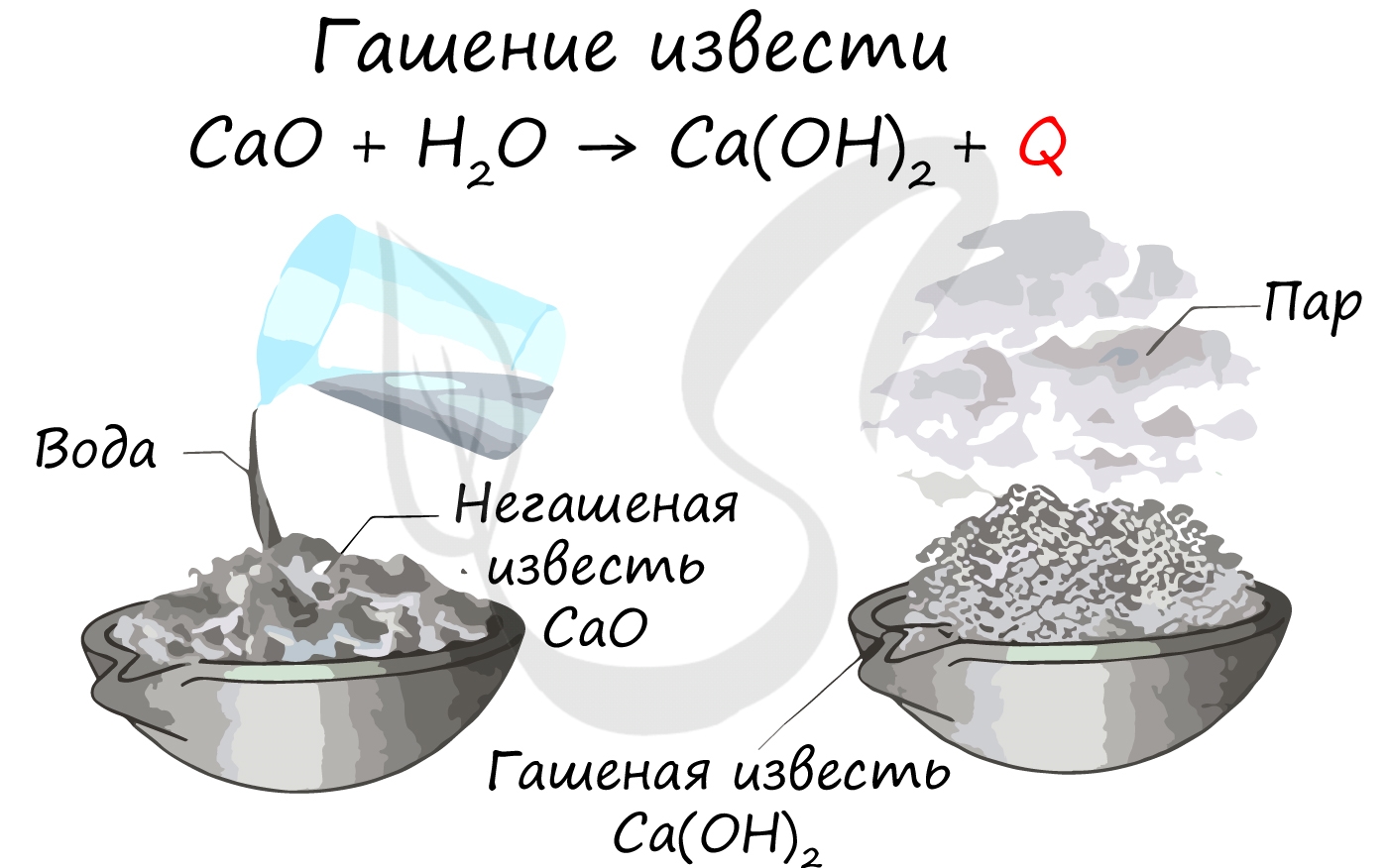
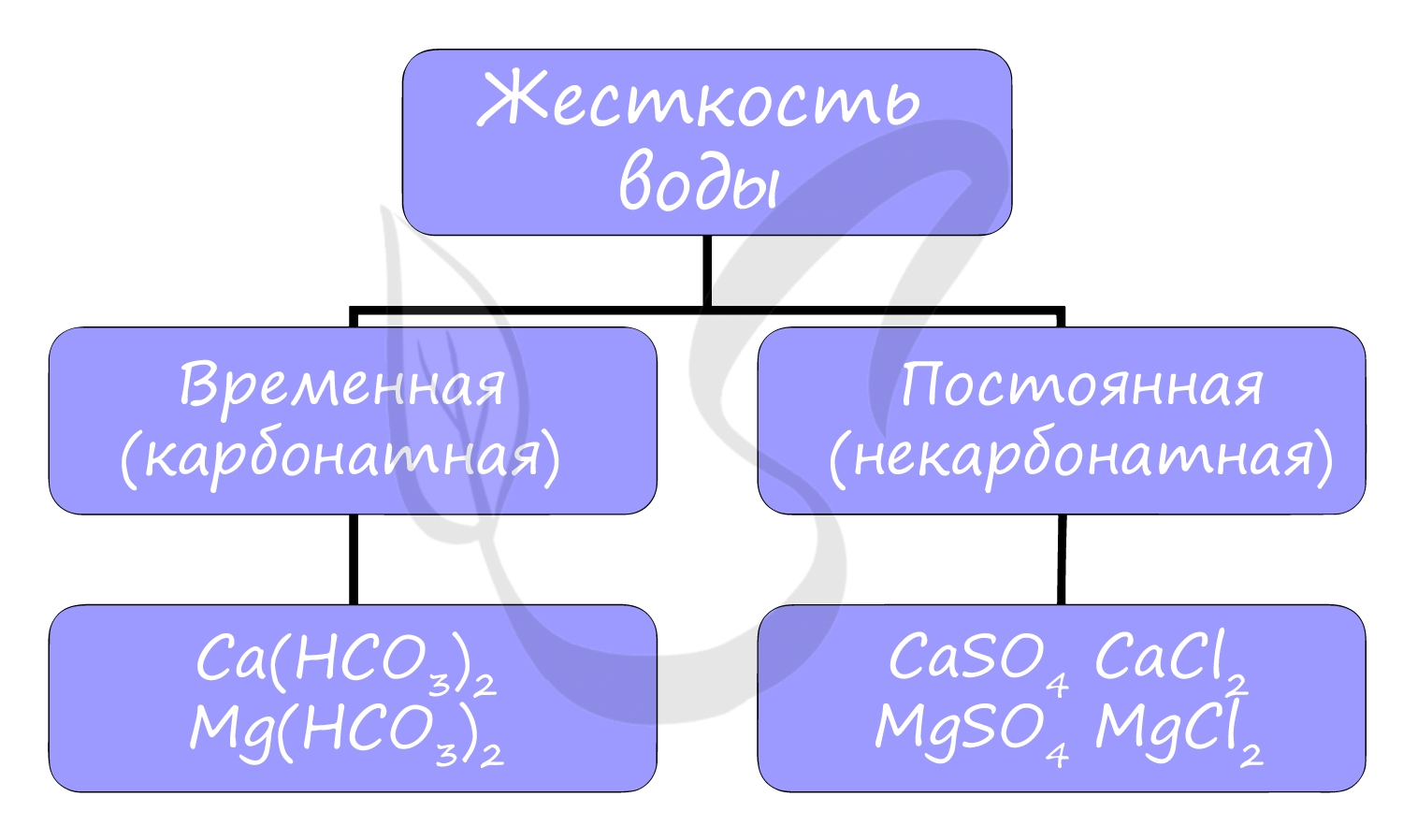
Все щелочноземельные металлы (кроме бериллия и магния) реагируют с холодной водой с образованием соответствующих гидроксидов. Магний реагирует с водой только при нагревании. Щелочноземельные металлы — активные металлы, стоящие в ряду активности левее водорода, и, следовательно, способные вытеснить водород из кислот: Реакции с неметаллами Хорошо реагируют с неметаллами: кислородом, образуя оксиды состава RO, с галогенами (F, Cl, Br, I). Степень окисления у щелочноземельных металлов постоянная +2. Mg + O2 → MgO (оксид магния) При нагревании реагируют с серой, азотом, водородом и углеродом. Mg + S → (t) MgS (сульфид магния) Ca + H2 → (t) CaH2 (гидрид кальция) Ba + C → (t) BaC2 (карбид бария) Ba + TiO2 → BaO + Ti (барий, как более активный металл, вытесняет титан) Оксиды щелочноземельных металловИмеют общую формулу RO, например: MgO, CaO, BaO. ПолучениеОксиды щелочноземельных металлов можно получить путем разложения карбонатов и нитратов: Рекомендую взять на вооружение общую схему разложения нитратов: Химические свойстваПроявляют преимущественно основные свойства, все кроме BeO — амфотерного оксида.
Реакция с водой В нее вступают все, кроме оксида бериллия. Амфотерный оксид бериллия Амфотерные свойства оксида бериллия требуют особого внимания. Этот оксид проявляет двойственные свойства: реагирует с кислотами с образованием солей, и с основаниями с образованием комплексных солей. BeO + NaOH + H2O → Na2[Be(OH)4] (тетрагидроксобериллат натрия) Если реакция проходит при высоких температурах (в расплаве) комплексная соль не образуется, так как происходит испарение воды: BeO + NaOH → Na2BeO2 + H2O (бериллат натрия) Гидроксиды щелочноземельных металловПроявляют основные свойства, за исключением гидроксида бериллия — амфотерного гидроксида. ПолучениеПолучают гидроксиды в реакции соответствующего оксида металла и воды (все кроме Be(OH)2) Химические свойстваОсновные свойства большинства гидроксидов располагают к реакциям с кислотами и кислотными оксидами. Реакции с солями (и не только) идут в том случае, если соль растворимы и по итогам реакции выделяется газ, выпадает осадок или образуется слабый электролит (вода). Гидроксид бериллия относится к амфотерным: проявляет двойственные свойства, реагируя и с кислотами, и с основаниями. Жесткость водыЖесткостью воды называют совокупность свойств воды, зависящую от присутствия в ней преимущественно солей кальция и магния: гидрокарбонатов, сульфатов и хлоридов. Различают временную (карбонатную) и постоянную (некарбонатную) жесткость. Вероятно, вы часто устраняете жесткость воды у себя дома, осмелюсь предположить — каждый день. Временная жесткость воды устраняется обычным кипячением воды в чайнике, и известь на его стенках — CaCO3 — бесспорное доказательство устранения жесткости: Также временную жесткость можно устранить, добавив Na2CO3 в воду: С постоянной жесткостью бороться кипячением бесполезно: сульфаты и хлориды не выпадут в осадок при кипячении. Постоянную жесткость воды устраняют добавлением в воду Na2CO3: Жесткость воды можно определить с помощью различных тестов. Чрезмерно высокая жесткость воды приводит к быстрому образованию накипи на стенках котлов, труб, чайника. © Беллевич Юрий Сергеевич 2018-2022 Данная статья написана Беллевичем Юрием Сергеевичем и является его интеллектуальной собственностью. Копирование, распространение (в том числе путем копирования на другие сайты и ресурсы в Интернете) или любое иное использование информации и объектов без предварительного согласия правообладателя преследуется по закону. Для получения материалов статьи и разрешения их использования, обратитесь, пожалуйста, к Беллевичу Юрию. Блиц-опрос по теме Щелочноземельные металлы Щелочноземельные металлы и их соединенияЭлементы II группы главной подгруппы Элементы II группы главной подгруппыПоложение в периодической системе химических элементовЩелочноземельные металлы расположены во второй группе главной подгруппе периодической системы химических элементов Д.И. Менделеева (или просто во 2 группе в длиннопериодной форме ПСХЭ). На практике к щелочноземельным металлам относят только кальций Ca, стронций Sr, барий Ba и радий Ra. Бериллий Be по свойствам больше похож на алюминий, магний Mg проявляет некоторые свойства щелочноземельных металлов, но в целом отличается от них. Однако, согласно номенклатуре ИЮПАК, щелочноземельными принято считать все металлы II группы главной подгруппы. Электронное строение и закономерности изменения свойствЭлектронная конфигурация внешнего энергетического уровня щелочноземельных металлов: ns 2 , на внешнем энергетическом уровне в основном состоянии находится 2 s-электрона. Следовательно, типичная степень окисления щелочноземельных металлов в соединениях +2. Рассмотрим некоторые закономерности изменения свойств щелочноземельных металлов. В ряду Be—Mg—Ca—Sr—Ba—Ra, в соответствии с Периодическим законом, увеличивается атомный радиус , усиливаются металлические свойства , ослабевают неметаллические свойства , уменьшается электроотрицательность . Физические свойстваВсе щелочноземельные металлы — вещества серого цвета и гораздо более твердые, чем щелочные металлы. Бериллий Be устойчив на воздухе. Магний и кальций (Mg и Ca) устойчивы в сухом воздухе. Стронций Sr и барий Ba хранят под слоем керосина. Кристаллическая решетка щелочноземельных металлов в твёрдом состоянии — металлическая. Следовательно, они обладают высокой тепло- и электропроводимостью. Кипят и плавятся при высоких температурах. Нахождение в природеКак правило, щелочноземельные металлы в природе присутствуют в виде минеральных солей: хлоридов, бромидов, йодидов, карбонатов, нитратов и др. Основные минералы, в которых присутствуют щелочноземельные металлы: Доломит — CaCO3 · MgCO3 — карбонат кальция-магния. Магнезит MgCO3 – карбонат магния. Кальцит CaCO3 – карбонат кальция. Гипс CaSO4 · 2H2O – дигидрат сульфата кальция. Барит BaSO4 — сульфат бария. Витерит BaCO3 – карбонат бария. Способы полученияМагний получают электролизом расплавленного карналлита или хлорида магния с добавками хлорида натрия при 720–750°С: или восстановлением прокаленного доломита в электропечах при 1200–1300°С: 2(CaO · MgO) + Si → 2Mg + Ca2SiO4 Кальций получают электролизом расплавленного хлорида кальция с добавками фторида кальция: Барий получают восстановлением оксида бария алюминием в вакууме при 1200 °C: 4BaO + 2Al → 3Ba + Ba(AlO2)2 Качественные реакцииКачественная реакция на щелочноземельные металлы — окрашивание пламени солями щелочноземельных металлов . Цвет пламени: Качественная реакция на ионы магния : взаим одействие с щелочами. Ионы магния осаждаются щелочами с образованием белого осадка гидроксида магния: Mg 2+ + 2OH — → Mg(OH)2↓ Качественная реакция на ионы кальция, стронция, бария : взаим одействие с карбонатами. При взаимодействии солей кальция, стронция и бария с карбонатами выпадает белый осадок карбоната кальция, стронция или бария : Ca 2+ + CO3 2- → CaCO3↓ Ba 2+ + CO3 2- → BaCO3↓ Качественная реакция на ионы стронция и бария : взаим одействие с сульфатами. При взаимодействии солей стронция и бария с сульфатами выпадает белый осадок сульфата бария и сульфата стронция : Ba 2+ + SO4 2- → BaSO4↓ Sr 2+ + SO4 2- → SrSO4↓ Также осадки белого цвета образуются при взаимодействии солей кальция, стронция и бария с сульфитами и фосфатами. Например , при взаимодействии хлорида кальция с фосфатом натрия образуется белый осадок фосфата кальция: Химические свойства1. Щелочноземельные металлы — сильные восстановители . Поэтому они реагируют почти со всеми неметаллами . 1.1. Щелочноземельные металлы реагируют с галогенами с образованием галогенидов при нагревании. Например , бериллий взаимодействует с хлором с образованием хлорида бериллия: 1.2. Щелочноземельные металлы реагируют при нагревании с серой и фосфором с образованием сульфидов и фосфидов. Например , кальций взаимодействует с серой при нагревании: Ca + S → CaS Кальций взаимодействует с фосфором с образованием фосфидов: 1.3. Щелочноземельные металлы реагируют с водородом при нагревании. При этом образуются бинарные соединения — гидриды. Бериллий с водородом не взаимодействует , магний реагирует лишь при повышенном давлении. 1.4. С азотом магний взаимодействует при комнатной температуре с образованием нитрида: Остальные щелочноземельные металлы реагируют с азотом при нагревании. 1.5. Щелочноземельные металлы реагируют с углеродом с образованием карбидов, преимущественно ацетиленидов. Например , кальций взаимодействует с углеродом с образованием карбида кальция: Ca + 2C → CaC2 Бериллий реагирует с углеродом при нагревании с образованием карбида — метанида: 2Be + C → Be2C 1.6. Бериллий сгорает на воздухе при температуре около 900°С: 2Be + O2 → 2BeO Магний горит на воздухе при 650°С с выделением большого количества света. При этом образуются оксиды и нитриды: 2Mg + O2 → 2MgO Щелочноземельные металлы горят на воздухе при температуре около 500°С, в результате также образуются оксиды и нитриды. Видеоопыт : горение кальция на воздухе можно посмотреть здесь. 2. Щелочноземельные металлы взаимодействуют со сложными веществами: 2.1. Щелочноземельные металлы реагируют с водой . Взаимодействие с водой приводит к образованию щелочи и водорода. Бериллий с водой не реагирует. Магний реагирует с водой при кипячении. Кальций, стронций и барий реагируют с водой при комнатной температуре. Например , кальций реагирует с водой с образованием гидроксида кальция и водорода: 2 Ca 0 + 2 H2 + O = 2 Ca + ( OH)2 + H2 0 2.2. Щелочноземельные металлы взаимодействуют с минеральными кислотами (с соляной, фосфорной, разбавленной серной кислотой и др.). При этом образуются соль и водород. Например , магний реагирует с соляной кислотой : 2Mg + 2HCl → MgCl2 + H2↑ 2.3. При взаимодействии щелочноземельных металлов с концентрированной серной кислотой образуется сера. Например , при взаимодействии кальция с концентрированной серной кислотой образуется сульфат кальция, сера и вода: 2.4. Щелочноземельные металлы реагируют с азотной кислотой . При взаимодействии кальция и магния с концентрированной или разбавленной азотной кислотой образуется оксид азота (I): При взаимодействии щелочноземельных металлов с очень разбавленной азотной кислотой образуется нитрат аммония: 2.5. Щелочноземельные металлы могут восстанавливать некоторые неметаллы (кремний, бор, углерод) из оксидов. Например , при взаимодействии кальция с оксидом кремния (IV) образуются кремний и оксид кальция: 2Ca + SiO2 → 2CaO + Si Магний горит в атмосфере углекислого газа . При этом образуется сажа и оксид магния: 2Mg + CO2 → 2MgO + C 2.6. В расплаве щелочноземельные металлы могут вытеснять менее активные металлы из солей и оксидов . Обратите внимание! В растворе щелочноземельные металлы будут взаимодействовать с водой, а не с солями других металлов. Например , кальций вытесняет медь из расплава хлорида меди (II): Ca + CuCl2 → CaCl2 + Cu Оксиды щелочноземельных металловСпособы получения1. О ксиды щелочноземельных металлов можно получить из простых веществ — окислением металлов кислородом : 2Ca + O2 → 2CaO 2. Оксиды щелочноземельных металлов можно получить термическим разложением некоторых кислородсодержащих солей — карбонатов , нитратов . Например , нитрат кальция разлагается на оксид кальция, оксид азота (IV) и кислород: 3. Оксиды магния и бериллия можно получить термическим разложением гидроксидов : Химические свойстваОксиды кальция, стронция, бария и магния — типичные основные оксиды . Вступают в реакции с кислотными и амфотерными оксидами, кислотами, водой. Оксид бериллия — амфотерный . 1. Оксиды кальция, стронция, бария и магния взаимодействуют с кислотными и амфотерными оксидами : Например , оксид магния взаимодействует с углекислым газом с образованием карбоната магния: 2. Оксиды щелочноземельных металлов взаимодействуют с кислотами с образованием средних и кислых солей (с многоосновными кислотами). Например , оксид кальция взаимодействует с соляной кислотой с образованием хлорида кальция и воды: CaO + 2HCl → CaCl2 + H2O 3. Оксиды кальция, стронция и бария активно взаимодействуют с водой с образованием щелочей. Например , оксид кальция взаимодействует с водой с образованием гидроксида кальция: CaO + H2O → 2Ca(OH)2 Оксид магния реагирует с водой при нагревании: MgO + H2O → Mg(OH)2 Оксид бериллия не взаимодействует с водой. 4. Оксид бериллия взаимодействует с щелочами и основными оксидами. При взаимодействии оксида бериллия с щелочами в расплаве или с основными оксидами образуются соли-бериллаты. Например , оксид натрия реагирует с оксидом бериллия с образованием бериллата натрия: Например , гидроксид натрия реагирует с оксидом бериллия в расплаве с образованием бериллата натрия: При взаимодействии оксида бериллия с щелочами в растворе образуются комплексные соли. Например , оксид бериллия реагирует с гидроксидом калия с растворе с образованием тетрагидроксобериллата калия: Гидроксиды щелочноземельных металловСпособы получения1. Гидроксиды кальция, стронция и бария получают при взаимодействии соответствующих оксидов с водой . Например , оксид кальция (негашеная известь) при взаимодействии с водой образует гидроксид кальция (гашеная известь): Оксид магния взаимодействует с водой только при нагревании: 2. Гидроксиды кальция, стронция и бария получают при взаимодействии соответствующих металлов с водой. Например , кальций реагирует с водой с образованием гидроксида кальция и водорода: Магний взаимодействует с водой только при кипячении: 3. Гидроксиды кальция и магния можно получить при взаимодействии солей кальция и магния с щелочами . Например , нитрат кальция с гидроксидом калия образует нитрат калия и гидроксид кальция: Химические свойства1. Гидроксиды кальция, стронция и бария реагируют с всеми кислотами (и сильными, и слабыми). При этом образуются средние или кислые соли, в зависимости от соотношения реагентов. Гидроксид магния взаимодействует только с сильными кислотами. Например , гидроксид кальция с соляной кислотой реагирует с образова-нием хлорида кальция: 2. Гидроксиды щелочных металлов реагируют с кислотными оксидами . При этом образуются средние или кислые соли, в зависимости от соотношения реагентов. Например , гидроксид бария с углекислым газом реагирует с образова-нием карбонатов или гидрокарбонатов: 3. Гидроксиды кальция, стронция и бария реагируют с амфотерными оксидами и гидроксидами . При этом в расплаве образуются средние соли, а в растворе комплексные соли. Например , гидроксид бария с оксидом алюминия реагирует в расплаве с образованием алюминатов: в растворе образуется комплексная соль — тетрагидроксоалюминат: 4. Гидроксиды кальция, стронция и бария взаимодействуют с кислыми солями. При этом образуются средние соли, или менее кислые соли. Например : гидроксид кальция реагирует с гидрокарбонатом кальция с образованием карбоната кальция: 5. Гидроксиды кальция, стронция и бария взаимодействуют с простыми веществами-неметаллами (кроме инертных газов, азота, кислорода, водорода и углерода). Взаимодействие щелочей с неметаллами подробно рассмотрено в статье про щелочные металлы. 6. Гидроксиды кальция, стронция и бария взаимодействуют с амфотерными металлами , кроме железа и хрома . При этом в расплаве образуются соль и водород: В растворе образуются комплексная соль и водород: 7. Гидроксиды кальция, стронция и бария вступают в обменные реакции с растворимыми солями. Как правило, с этими гидроксидами реагируют растворимые соли тяжелых металлов (в ряду активности расположены правее алюминия), а также растворимые карбонаты, сульфиты, силикаты, и, для гидроксидов стронция и бария — растворимые сульфаты. Например , хлорид железа (II) реагирует с гидроксидом бария с образованием хлорида бария и осадка гидроксида железа (II): Также с гидроксидами кальция, стронция и бария взаимодействуют соли аммония. Например , при взаимодействии бромида аммония и гидроксида кальция образуются бромид кальция, аммиак и вода: 8. Гидроксид кальция разлагается при нагревании до 580 о С, гидроксиды магния и бериллия разлагаются при нагревании: 9. Гидроксиды кальция, стронция и бария проявляют свойства сильных оснований . В воде практически полностью диссоциируют , образуя щелочную среду и меняя окраску индикаторов. Ba(OH)2 ↔ Ba 2+ + 2OH — Гидроксид магния — нерастворимое основание. Гидроксид бериллия проявляет амфотерные свойства. 10. Гидроксид и бериллия взаимодействует с щелочами . В расплаве образуются соли бериллаты, а в растворе щелочей — комплексные соли. Например , гидроксид бериллия реагирует с расплавом гидроксида натрия: При взаимодействии гидроксида бериллия с избытком раствора щелочи образуется комплексная соль: Соли щелочноземельных металловНитраты щелочноземельных металловНитраты кальция, стронция и бария при нагревании разлагаются на нитриты и кислород. Исключение — нитрат магния. Он разлагается на оксид магния, оксид азота (IV) и кислород. Например , нитрат кальция разлагается при нагревании на нитрит кальция и молекулярный кислород: Карбонаты щелочноземельных металлов1. Карбонаты щелочноземельных металлов при нагревании разлагаются на оксид и углекислый газ. Например , карбонат кальция разлагается при температуре 1200 о С на оксид кальция и углекислый газ: 2. Карбонаты щелочноземельных металлов под действием воды и углекислого газа превращаются в растворимые в воде гидрокарбонаты. Например , карбонат кальция взаимодействует с углекислым газом и водой с образованием гидрокарбоната кальция: 3. Карбонаты щелочноземельных металлов взаимодействуют с более сильными кислотами с образованием новой соли, углекислого газа и воды. Более сильные кислоты вытесняют менее сильные из солей. Например , карбонат магния взаимодействует с соляной кислотой: 4. Менее летучие оксиды вытесняют углекислый газ из карбонатов при сплавлении. К менее летучим, чем углекислый газ, оксидам относятся твердые оксиды — оксид кремния (IV), оксиды амфотерных металлов. Менее летучие оксиды вытесняют более летучие оксиды из солей при сплавлении. Например , карбонат кальция взаимодействует с оксидом алюминия при сплавлении: Жесткость водыПостоянная и временная жесткостьЖесткость воды — это характеристика воды, обусловленная содержанием в ней растворенных солей щелочноземельных металлов, в основном кальция и магния (солей жесткости). Временная (карбонатная) жесткость обусловлена присутствием гидрокарбонатов кальция Ca(HCO3)2 и магния Mg(HCO3)2 в воде. Постоянная (некарбонатная) жесткость обусловлена присутствием солей, не выделяющихся при кипячении из раствора: хлоридов (CaCl2) и сульфатов (MgSO4) кальция и магния. Способы устранения жесткостиСуществуют химические и физические способы устранения жесткости. Химические способы устранения временной жесткости: 1. Кипячение. При кипячении гидрокарбонаты кальция и магния распадаются на нерастворимые карбонаты, углекислый газ и воду: 2. Добавление извести (гидроксида кальция). При добавлении щелочи растворимые гидрокарбонаты переходят в нерастворимые карбонаты: Химические способы устранения постоянной жесткости — реакции ионного обмена, которые позволяют осадить ионы кальция и магния из раствора: 1. Добавление соды (карбоната натрия). Карбонат натрия связывает ионы кальция и магния в нерастворимые карбонаты: CaCl2 + Na2CO3 → CaCO3↓+ 2NaCl 2. Добавление фосфатов. Фосфаты также связывают ионы кальция и магния: источники: http://studarium.ru/article/180 http://chemege.ru/shhelochnozem-met/ |