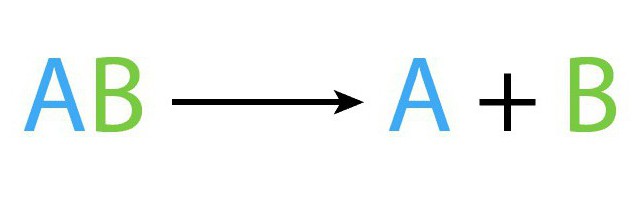
Реакции разложения
При выполнении различных заданий ЕГЭ по химии (например, задачи 34 или задания 32 «мысленный эксперимент») могут пригодиться знания о том, какие вещества при нагревании разлагаются и как они разлагаются.
Рассмотрим термическую устойчивость основных классов неорганических веществ. Я не указываю в условиях температуру протекания процессов, так как в ЕГЭ по химии такая информация, как правило, не встречается. Если возможны различные варианты разложения веществ, я привожу наиболее вероятные, на мой взгляд, реакции.
Разложение оксидов
При нагревании разлагаются оксиды тяжелых металлов:
2HgO = 2Hg + O2
Разложение гидроксидов
Как правило, при нагревании разлагаются нерастворимые гидроксиды. Исключением является гидроксид лития, он растворим, но при нагревании в твердом виде разлагается на оксид и воду:
2LiOH = Li2O + H2O
Гидроксиды других щелочных металлов при нагревании не разлагаются.
Гидроксиды серебра (I) и меди (I) неустойчивы:
2AgOH = Ag2O + H2O
2CuOH = Cu2O + H2O
Гидроксиды большинства металлов при нагревании разлагаются на оксид и воду.
В инертной атмосфере (в отсутствии кислорода воздуха) гидроксиды хрома (III) марганца (II) и железа (II) распадаются на оксид и воду:
Большинство остальных нерастворимых гидроксидов металлов также при нагревании разлагаются:
Разложение кислот
При нагревании разлагаются нерастворимые кислоты.
Например , кремниевая кислота:
Некоторые кислоты неустойчивы и подвергаются разложению в момент образования. Большая часть молекул сернистой кислоты и угольной кислоты распадаются на оксид и воду в момент образования:
В ЕГЭ по химии лучше эти кислоты записывать в виде оксида и воды.
Например , при действии водного раствора углекислого газа на карбонат калия в качестве реагента мы указываем не угольную кислоту, а оксид углерода (IV) и воду, но подразумеваем угольную кислоту при этом:
Азотистая кислота на холоде или при комнатной температуре частично распадается уже в водном растворе, реакция протекает обратимо:
При нагревании выше 100 о С продукты распада несколько отличаются:
Азотная кислота под действием света или при нагревании частично обратимо разлагается:
Разложение солей
Разложение хлоридов
Хлориды щелочных, щелочноземельных металлов, магния, цинка, алюминия и хрома при нагревании не разлагаются.
Хлорид серебра (I) разлагается под действием света:
2AgCl → Ag + Cl2
Хлорид аммония при нагревании выше 340 о С разлагается:
Разложение нитратов
Нитраты щелочных металлов при нагревании разлагаются до нитрита металла и кислорода.
Например , разложение нитрата калия:
Видеоопыт разложения нитрата калия можно посмотреть здесь.
Нитраты магния, стронция, кальция и бария разлагаются до нитрита и кислорода при нагревании до 500 о С:
При более сильном нагревании (выше 500 о С) нитраты магния, стронция, кальция и бария разлагаются до оксида металла, оксида азота (IV) и кислорода:
Нитраты металлов, расположенных в ряду напряжений после магния и до меди (включительно) + нитрат лития разлагаются при нагревании до оксида металла, диоксида азота и кислорода:
Нитраты серебра и ртути разлагаются при нагревании до металла, диоксида азота и кислорода:
Нитрат аммония разлагается при небольшом нагревании до 270 о С оксида азота (I) и воды:
При более высокой температуре образуются азот и кислород:
Разложение карбонатов и гидрокарбонатов
Карбонаты натрия и калия плавятся при нагревании.
Карбонаты лития, щелочноземельных металлов и магния разлагаются на оксид металла и углекислый газ:
Карбонат аммония разлагается при 30 о С на гидрокарбонат аммония и аммиак:
Гидрокарбонат аммония при дальнейшем нагревании разлагается на аммиак, углекислый газ и воду:
Гидрокарбонаты натрия и калия при нагревании разлагаются на карбонаты, углекислый газ и воду:
Гидрокарбонат кальция при нагревании до 100 о С разлагается на карбонат, углекислый газ и воду:
При нагревании до 1200 о С образуются оксиды:
Разложение сульфатов
Сульфаты щелочных металлов при нагревании не разлагаются.
Сульфаты алюминия, щелочноземельных металлов, меди, железа и магния разлагаются до оксида металла, диоксида серы и кислорода:
Сульфаты серебра и ртути разлагаются до металла, диоксида серы и кислорода:
Разложение фосфатов, гидрофосфатов и дигидрофосфатов
Эти реакции, скорее всего, в ЕГЭ по химии не встретятся! Гидрофосфаты щелочных и щелочноземельных металлов разлагаются до пирофосфатов:
Ортофосфаты при нагревании не разлагаются (кроме фосфата аммония).
Разложение сульфитов
Сульфиты щелочных металлов разлагаются до сульфидов и сульфатов:
Разложение солей аммония
Некоторые соли аммония, не содержащие анионы кислот-сильных окислителей, обратимо разлагаются при нагревании без изменения степени окисления. Это хлорид, бромид, йодид, дигидрофосфат аммония:
Cоли аммония, образованные кислотами-окислителями, при нагревании также разлагаются. При этом протекает окислительно-восстановительная реакция. Это дихромат аммония, нитрат и нитрит аммония:
Видеоопыт разложения нитрита аммония можно посмотреть здесь.
Разложение перманганата калия
Разложение хлората и перхлората калия
Хлорат калия при нагревании разлагается до перхлората и хлорида:
4KClO3 → 3KClO4 + KCl
При нагревании в присутствии катализатора (оксид марганца (IV)) образуется хлорид калия и кислород:
2KClO3 → 2KCl + 3O2
Перхлорат калия при нагревании разлагается до хлорида и кислорода:
Реакция разложения: примеры и уравнение
Часто от приличных на вид людей можно услышать о вреде для здоровья какого-то продукта или средства. Причем главным аргументом в пользу такого утверждения будет фраза: «Это химия!». Однако так говорить могут лишь те, кто в школе явно прогуливал уроки по данному предмету. Дело в том, что человеческий, да и любой биологический организм, сам по себе состоит из множества органических и неорганических веществ. При этом поддерживать его жизнеспособность помогают различные процессы, непрерывно происходящие внутри него. Одним из главных среди них — является химическая реакция разложения. Давайте узнаем больше о ней и особенностях ее протекания с органическими и неорганическими веществами.
Что за процесс называется химической реакцией
Прежде всего, стоит узнать значение понятия «химическая реакция». Это словосочетание означает превращение одного и более исходных веществ (называются реагентами) в другие. В процессе подобной метаморфозы ядра атомов взаимодействующих соединений не поддаются изменениям, однако происходит перераспределение электронов. Таким образом, после превращения на выходе образуются новые атомные соединения.
Химические реакции имеют качественное отличие от физических и ядерных.
- В результате первых исходные реагенты никогда не меняют свой состав, хотя и способны образовывать смеси или переходить из одного агрегатного состояния в другое. В отличие от них, процессы химические сопровождаются образованием новых соединений, с совершенно иными свойствами.
- Результатом вторых является изменения изотопного состава и числа атомов. Таким образом, на выходе из одних элементов, образовываются другие. Однако для химических процессов, столь глубокие метаморфозы не характерны. Поскольку изменения, произошедшие из-за них, не влияют на внутреннюю структуру атомов.
Условия протекания химических реакций
Во многих случаях, для успешного протекания процессов такого рода, необходим просто физический контакт реагентов друг с другом или их смешивание. Но часто для начала химической реакции, ей необходимы катализаторы. В этой роли могут выступать как различные вещества, так и определенные внешние условия.
- Воздействие температуры. Для того чтобы запустить отдельные химические процессы, необходимо нагревать реагенты. К примеру, чтобы начать реакцию разложения карбоната кальция, это температуру этого соединений необходимо повысить до 900-1200 °C.
- Электромагнитные волны. Наиболее эффективно стимулирующей протекание любых процессов является воздействие на реагенты световыми волнами. Такие реакции носят название «фотохимические». Классическим примером такой реакции является фотосинтез.
- Ионизирующее излучение.
- Воздействие электрического тока.
- Разного рода механическое влияние на реагирующие вещества.
Какие виды химических реакций существуют
Классификация подобных процессов в основном производится по шести признакам.
- По наличию границы разделения фаз: гомо-/гетерогенные реакции.
- По выделению/поглощению тепла: экзотермически и эндотермические процессы.
- По наличию/отсутствию катализаторов: каталитические и некаталитические реакции.
- По направлению протекания: обратимые и необратимые процессы. В зависимости от данной категории находится тип знака между левой и правой частями химического уравнения. При необратимых — это две стрелки направленные в противоположные стороны, при обратимых — только одна, направленная слева на право.
- По изменению степени окисления. По этому принципу выделяют окислительно-восстановительную реакцию.
- Разложение (расщепление), соединение, замещение и обмен – это виды химических процессов по типу метаморфоз реагентов.
Реакция разложения (расщепления): что это
Под данным термином подразумевается процесс, в результате которого одно сложное вещество разделяется на два и более простых. В большинстве случаев катализатором для этого выступает высокая температура. По этой причине данный процесс еще называют реакцией термического разложения.
В качестве примера можно привести один из классических способов получения чистого кислорода (О2) в промышленности. Это происходит в следствии нагревании KMnO4 (более известен всем под бытовым названием «марганцовка»).
В результате расщепления образуется не только кислород, но и манганат калия (K2MnO4) , а также диоксид марганца (MnO2).
Уравнение реакции разложения
Любое химическое уравнение состоит из двух частей: левой и правой. В первой из них записываются реагирующие соединения, а во второй – продукты реакции. Между ними обычно ставится направленная вправо стрелка. Иногда она бывает двухсторонней, если речь идет об обратимом процессе. В отдельных случаях ее допустимо заменить знаком равенства (=).
Рассматриваемый процесс, как и остальные виды химических процессов, имеет собственную формулу. Схематически уравнение реакции разложения выглядит таким образом: AB (t) → A+B.
Стоит помнить, что преимущественное большинство таких процессов происходит под воздействием тепла. Чтобы сообщить об этом, над стрелкой или рядом с ней часто ставится либо литера t, либо треугольник. Однако, иногда вместо тепла, в роли катализаторов выступают различные вещества, излучения.
В рассмотренной выше формуле AB — то исходное сложное соединения, A, B – это новые вещества, образованные в результате реакции разложения.
Примеры практические такого процесса встречаются очень часто. Можно проиллюстрировать данную формулу, с помощью уравнения процесса, описанного в предыдущем пункте: 2KMnO4 (t) → K2MnO4 + MnO2 + O2↑.
Виды реакций разложения
В зависимости от типа катализатора (который способствует расщеплению сложного вещества на более простые) выделяют несколько видов разложения.
- Биодеградация – распад веществ вследствие деятельности живых организмов (микроорганизмы, грибы, водоросли). Более простым языком данный процесс можно назвать гниением. Именно из-за него портятся продукты. В одной стороны это препятствует их долгому хранению, с другой – помогает природе утилизировать все лишнее, восстанавливая таким образом экосистемы.
- Радиолиз – распад соединений при помощи воздействия на их молекулы ионизирующим излучением.
- Термолиз – повышение температуры для того, чтобы запустить реакцию разложения (примеры подобных процессов можно найти в пунктах 8-9).
- Сольволиз – обменное разложения между растворенным веществом и непосредственно самим растворителем. В зависимости от типа последнего, выделяются такие виды этого процесса: гидролиз (вода), алколиз (спирты), аммонолиз (амиак).
- Электролиз – разложение молекул с помощью воздействия на них электрического тока (пример в следующем пункте).
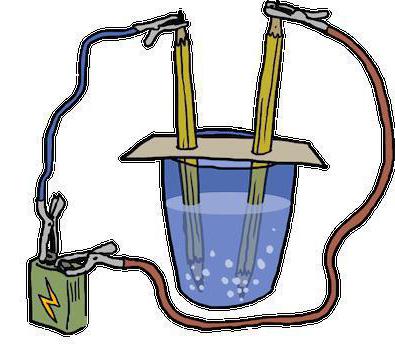
Расщепление Н2О
Разобравшись с теорией, касающейся реакции разложения, примеры практические ее проведения стоит рассмотреть. Поскольку Н2О сегодня является одним из наиболее доступных веществ для проведения химических опытов, стоит начать с нее.
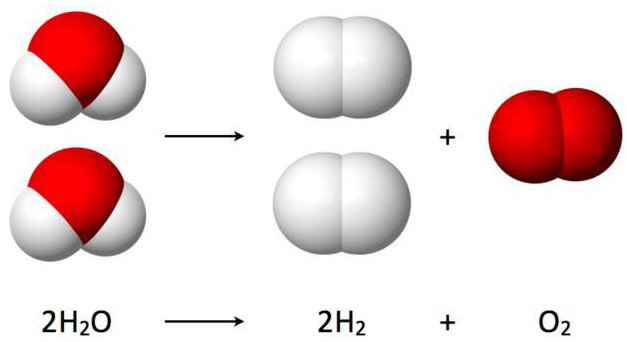
Данная реакция разложения воды именуется еще электролизом и выглядит таким образом: 2Н2О (электрический ток) → 2Н2↑ + О2↑.
Расшифровывается данное уравнение так: под воздействием на молекулы воды электрического тока, они расщепляют и образуют два газа – кислород и водород.Стоит отметить, что этот метод активно используется на подводных лодках для получения кислорода. В современном мире он заменил более дорогой способ получения этого жизненно важного вещества из пероксида натрия (Na2O2), с помощью его взаимодействия с углекислым газом: Na2O2 + CO2↑ → Na2CO3 + O2↑.
В перспективе реакция разложения воды может иметь огромное значение для будущего планеты. Поскольку таким образом можно добывать не только кислород, но и водород, использующийся как ракетное топливо. Разработки в этой области уже ведутся многие годы, однако основной проблемой является необходимость снизить количество энергозатрат на расщепление молекул воды.
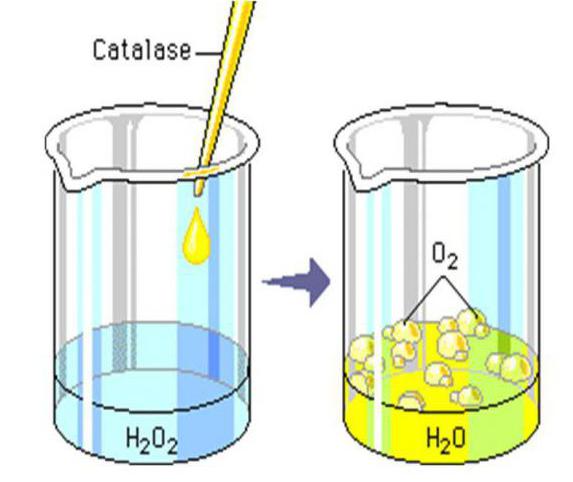
Расщепление Н2О2
Среди других примеров реакции разложения стоит обратить внимание на образование воды и кислорода из пероксида водорода (перекись).
Данный процесс также является термическим, поскольку для его начала, необходимо, чтобы исходное веществ было нагрето до температуры в 150 °C.
Именно по этой причине, перекись водорода (которую большинство использует для обработки ран) не превращается в воду, стоя в домашних аптечках.
Однако стоит помнить, что реакция разложения пероксида водорода может происходить и при обычной комнатной температуре, если вещество контактирует с такими соединениями, как каустическая сода (NaOH) или диоксид марганца (MnO2). Также в роли катализаторов могут выступать платина (Pt) и купрум (Cu).
Реакция термического разложения CaCO3
Еще одним интересным примером может служить расщепление карбоната кальция. Данный процесс можно записать с помощью такого уравнения: CaCO3 (t) → CaO + CO2↑.
Продуктом этой реакции буде негашеная известь (оксид кальция) и углекислый газ.
Представленный выше процесс активно используется в промышленности для получения углекислого газа. Подобные реакции производятся в специализированных шахтах, поскольку расщепление карбоната кальция происходит лишь при температуре от 900 °C.
Как расставлять коэффициенты в химических уравнениях
Содержание:
Все химические реакции, проходящие в окружающем мире можно описать при помощи специальных уравнений, представляющих собой химические формулы и математические знаки с коэффициентами. И от правильно расставленных коэффициентов в химических уравнениях порой зависит не много не мало, а то какой собственно и будет химическая реакция и будет ли она вообще. В нашей статье мы расскажем о том, как правильно расставлять коэффициенты в химии, чтобы химические уравнения были записаны верно.
Пример разбора простых реакций
Главное правило, которым следует руководствоваться при составлении химических уравнений – принцип сохранения энергии вещества, то есть, сколько есть атомов каждого химического элемента в левой части уравнения, столько должно быть и в правой части того же уравнения.
Для примера возьмем химическую реакцию взаимодействия кальция (Ca) с кислородом (O2). Но для начала объясним, почему вообще кислород (как и некоторые другие химических элементы) в химических уравнениях записывается с индексом «2». Дело в том, что одна молекула кислорода имеет 2 атома, поэтому его записывают как O2. В свою очередь, к примеру, одна молекула воды, состоящая из кислорода и водорода, имеет всем известную формулу H2O. Это означает, что каждая молекула воды состоит из двух атомов водорода и одного атома кислорода. Заметьте, что по своему усмотрению индексы в химических уравнениях и формулах менять нельзя, так как они изначально должны быть написаны правильно.
Теперь вернемся к нашему простому примеру реакции взаимодействия кальция и кислорода. Ее можно записать следующим образом:
О чем говорит эта запись? О том, что в результате химической реакции взаимодействия кальция с кислородом образуется оксид кальция, который записан формулой CaO. Но также обратите внимание, что в правой части оксид кальция мы записали с коэффициентом 2 – 2CaO. Это значит, что каждый из двух атомов кислорода сцепился со своим атомом кальция, но тогда происходит несоответствие – в правой стороне у нас два атома кальция, в то время как в левой только лишь один. А значит, чтобы запись была правильной в левой части мы должны перед кальцием поставить коэффициент 2:
Теперь мы можем проверить наше уравнение – с левой стороны у нас два атома кальция и с правой тоже два, а значит между обеими частями можно вполне справедливо поставить знак равенства:
Разберем еще один простой пример, из взаимодействия кислорода и водорода как мы знаем, рождается одно из самых ценным и необычных веществ во Вселенной (и это без преувеличения) – вода, основа жизни на нашей планете. Образование воды можно записать следующим уравнением:
Но где же здесь закралась ошибка? Давайте разберем: в левой части у нас два атома кислорода, а в правой только один. Значит перед формулой воды необходимо поставить коэффициент 2:
Умножение 2 молекул воды на 2 атома водорода даст нам 4 атома водорода с правой стороны, но ведь с левой стороны атомов водорода лишь два! Значить перед водородом в уравнении мы также должны поставить коэффициент 2 и теперь получим правильное химическое уравнение, где вместо стрелочки → можно уже смело поставить знак равенства.
Пример разбора сложной реакции
Теперь давайте разберем то, как проставлять коэффициенты в более сложных химических уравнениях:
Перед вами запись так званой реакции нейтрализации – взаимодействие кислоты и основания, в результате которого образуются соли и вода.
Что же мы имеем тут: с левой стороны у нас один атом натрия (Na), а с правой индекс говорит, что атомов натрия уже стало два. Значит логично, что химическую формулу основания гидроксида натрия NaOH надо умножить на 2. Или другими словами поставить перед ней коэффициент 2:
Количество серы в серной кислоте (H2SO4) и соли сульфате натрия (Na2SO4) у нас одинаковое, тут все хорошо, а вот с количеством кислорода и водорода опять несоответствие, с левой стороны кислорода 6, а с правой 5. Водорода с правой стороны 4, а с левой только 2, непорядок. Чтобы правильно записать это химическое уравнение надо сравнять количество кислорода и водорода в левой и правой части уравнения, к счастью тут сделать это просто, надо перед H2O поставить коэффициент 2.
Таким образом, количество всех химических элементов в правой и левой части уравнения у нас сравнялись, а значит, мы неспроста поставили знак равенства.
Для закрепления материала разберем еще один пример сложного уравнения.
Это уравнение отображает химическую реакцию гидроксида бария (Ba(OH)2) с азотной кислотой (HNO3) в результате которой образуется нитрат бария (Ba(NO3)2) и вода.
Пример этот нам интересен тем, что тут используются скобки. Они означают, что если множитель стоит за скобками, то каждый элемент умножается на него. Начнем же разбирать это уравнение, первое, что бросается в глаза, несоответствие азота N, слева он один, а вот справа, если принимать во внимание скобки, его уже два. Получим следующее:
Теперь у нас слева стало 4 атома водорода, а справа только 2. Значит, перед формулой воды также ставим коэффициент 2.
Теперь все элементы уравнены, и мы справедливо поставили знак равенства.
Видео
И чтобы окончательно закрепить материал, рекомендуем посмотреть это образовательное видео.
источники:http://fb.ru/article/330496/reaktsiya-razlojeniya-primeryi-i-uravnenie
http://www.poznavayka.org/himiya/kak-rasstavlyat-koefficzienty-v-himicheskih-uravneniyah/
Этот вид расщепления имеет подвид – пиролиз. От обычного термолиза он отличается тем, что помимо воздействия высокой температуры на молекулы вещества, также их лишают возможности взаимодействовать с кислородом (О2).