Диаграмма состояния сплавов с полиморфными превращениями компонентов и эвтектоидным превращением.
Диаграмма состояния сплавов, у которых высокотемпературные модификации компонентов γ обладают полной взаимной растворимостью, а низкотемпературные αF, βN – ограничены, приведена на рис. 2.2з.
По аналогии с линией эвтектического превращения DCE и эвтектической точкой C на рис. 2.2в линию СDE называют линией эвтектоидного превращения, а D – эвтектоидной точкой. Смесь кристаллов ограниченных растворов α (на основе низкотемпературной модификации полиморфного компонента А) и β (на основе низкотемпературной модификации полиморфного компонента В), которая образуется в твердом состоянии по реакции γD → αC + βE, получила название эвтектоида.
Сплавы, расположенные левее эвтектоидной точки D, называют доэвтектоидными, а сплавы, расположенные правее D, – заэвтектоидными.
2.6. Описание диаграммы состояния
Диаграммы состояния систем конкретных компонентов (например, «Железо – углерод», «Медь – алюминий» и др.) редко являются простейшими (типовыми) диаграммами. Они, как правило, являются сложными (комбинированными) диаграммами, в строении которых нужно уметь выделить простейшие (типовые) части их. На рис. 2.3 приведена сводная таблица так называемых геометрических образов различных превращений, т.е. показано расположение линий диаграмм, характерное для различных случаев взаимодействия компонентов и фаз.
В этом подразделе задания студент, изучив простейшие (типовые) диаграммы состояния (рис. 2.2) и ориентируясь по сводной таблице геометрических образов (рис. 2.3), должен дать общий анализ заданной диаграммы состояния, т. е. ответить на следующие вопросы:
· растворяются ли компоненты в жидком состоянии и как (ограниченно или неограниченно)?
· Растворяются компоненты в твердом состоянии, образуя ограниченные или неограниченные твердые растворы, или не растворяются, образуя смеси чистых компонентов, химических соединений и т.п.? Если образуются твердые растворы, то нужно их перечислить.
|  |  | ||
 |  |  | ||
| Полиморфные превращения | ||||
 |  | |||
 |  |
Рис. 2.3. Сводная таблица геометрических образов различных превращений
· 

· Перечислить все нонвариантные превращения, протекающие в заданной системе (эвтектические, эвтектоидные, перитектические, перитектоидные и др.), дать при этом словесное описание сути этих превращений, написать их уравнения, указать температуру и химические составы участвующих фаз.
2.7. построение кривой охлаждения заданного
сплава и Описание процесса кристаллизации
Сначала необходимо указать, до какой температуры сплав охлаждается, находясь в жидком состоянии (точка ликвидус), и на графике в координатах «Температура – Время» от любой точки, расположенной на оси ординат выше точки ликвидус, провести до нее круто падающую кривую. Это будет первый участок кривой охлаждения.
Затем для каждого температурного интервала, образованного критическими точками, а также для интервала под нижней критической точкой:
· описать процесс кристаллизации, который начинается при достижении сплавом данной критической точки;
· пользуясь правилом фаз, установить, идёт ли описываемый процесс в интервале температур или при постоянной температуре;
· на кривой охлаждения изобразить новый ее участок в рассматриваемом интервале температур, идущий под другим углом, нежели предыдущий, если процесс идёт при изменении температуры, или изобразить горизонтальную площадку, если процесс идёт при постоянной температуре;
· написать уравнение рассматриваемого процесса;
· описать структуру, которая сформировалась в сплаве к моменту окончания рассматриваемого процесса.
После рассмотрения последнего температурного интервала (под нижней критической точкой) ответ на этот пункт задания следует завершить описанием структуры сплава, сформировавшейся к моменту окончания последнего превращения.
Для правильного описания процесса кристаллизации заданного сплава надо, опираясь на знание типовых диаграмм и ориентируясь по таблице геометрических образов (рис. 2.3), правильно установить, каким фазовым превращениям соответствуют линии диаграммы, пересекаемые ординатой заданного сплава.
Применяя «правило фаз» (2.1) определить можно ли менять внешний
фактор, не нарушая равновесие фаз. При К = 2, Ф = 3, С = 0 – нонвариантная система и, следовательно, чтобы сохранить равновесие фаз, охлаждать сплав нельзя, процесс идёт при постоянной температуре (на кривой охлаждения – горизонтальная площадка) и при строго определенных (единственных) концентрациях фаз, участвующих в этом процессе.
Если число степеней свободы С = 1 (моновариантная система) или С = 2 (бивариантная система), то процесс идёт в интервале температур и на кривой охлаждения началу данного процесса соответствует точка перегиба (изменение наклона кривой).
Первичной кристаллизации (образования твёрдых фаз из жидкого состояния) соответствуют три типовые кривые охлаждения (рис. 2.4, 2.5, 2.6).
|
|
| ||||||
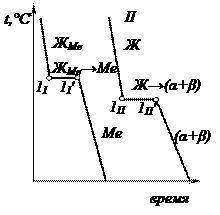
| Рис. 2.4. Кристаллизация при С = 0. I – чистые металлы: ЖМе→Ме. К = 1 (Ме), Ф = 2 (ЖМе, Ме), С = 0. II – сплавы, образующие смеси фаз: Ж→(α+β) К = 2 (А, В), Ф = 3 (Ж, α, β), С = 0. | Рис. 2.5. Кристаллизация при С = 1. Сплавы, образующие неограниченные твердые растворы: Ж→α. К = 2 (А, В), Ф = 2 (Ж, α), С = 1. | Рис. 2.6. Кристаллизация в два этапа (например, до- и заэвтектоидные сплавы). Ж→α. К = 2 (А, В), Ф = 2 (Ж, α), С = 1. Ж→(α+β) К = 2 (А, В), Ф = 3 (Ж, α, β), С = 0. |
Точки 1 соответствуют началу кристаллизации. Выше этих точек сплавы охлаждаются по физическим законам (без тепловых эффектов). Площадки 1I–1I‘, 1II–1II‘, 2IV–2IV‘ обусловлены выделением скрытой теплоты кристаллизации, которая уравновешивает отвод тепла от системы.
Охлаждение в интервалах 1III–2III и 1IV–2IV также сопровождается выделением теплоты, которой не хватает для сбалансирования отведенного от системы тепла. Поэтому в точках 1III и 1IV наблюдается перегиб в сторону замедления охлаждения. Точки 2 соответствуют окончанию процесса первичной кристаллизации.
Дальнейшее охлаждение чистых металлов идёт по физическим законам. Также охлаждаются сплавы, состоящие из компонентов, нерастворяющихся друг в друге в твердом состоянии. Большинство других сплавов по мере охлаждения претерпевают фазовую перекристаллизация, образуя смеси фаз или вторичные выделения.
Вопрос о возможности вторичных выделений решается легко. Если линии диаграммы, показывающие состав охлаждающихся твёрдых фаз, наклонны (состав их фаз изменяется с падением температуры), то в сплаве образуются вторичные выделения. Надо правильно решить вопрос о том, какие именно вторичные фазы выделяются. Вторичные выделения сопровождаются тепловым эффектом, поэтому на кривой охлаждения температуре начала выделения вторичных кристаллов соответствует перегиб.
Если линии диаграммы, показывающие состав охлаждающихся твёрдых фаз, вертикальны (состав фаз не изменяется с падением температуры), то вторичных выделений в сплаве не происходит.
При определении структуры сплава, сформировавшейся к моменту достижения конца данного температурного интервала, а также окончательной структуры сплава, образовавшейся после последнего превращения, нужно четко отличить структурный состав (структуру) сплава от фазового состава.
Фазами, как известно, называют однородные части системы, отделенные от других частей системы поверхностью раздела.
 |
Рис. 2.7. Диаграмма сплава с эвтектоидным превращением и таблица с указанием Под структурными составляющими понимают отдельные, обособленные части сплава, имеющие при рассмотрении под микроскопом однообразное строение с присущими им характерными особенностями. Структура характеризуется видом, формой, величиной, относительным количеством, распределением составляющих по объему или в плоскости шлифа. Структурная составляющая может состоять из одной, двух и более фаз. Формирование структуры прослеживается легче всего по превращениям, указанным на кривой охлаждения. Нужно следить за тем, какая (или какие) фаза участвует в фазовом превращении. Могут быть различные варианты. Например, двухфазный сплав, достигнув критической температуры, испытывает фазовое превращение. При этом фазы, взаимодействуя, расходуются полностью и образуется новая фаза. Возможен и другой путь. Одна фаза превращается в смесь фаз, а другая переходит в область низких температур как структурно свободная составляющая. Приведем пример, рассмотрев превращения, протекающие в сплаве, указанном на рис. 2.7. Рис. 2.8. Примерная структура сплава I при комнатной температуре В интервале 1000–600 °С сплав был однофазным. При охлаждении от 600 до 500 °С из γ-твёрдого раствора выделяются вторичные кристаллы компонента ВII. При 500 °С имеет место эвтектоидное превращение γ→(α+В). Вторичные кристаллы ВII в реакции участия не принимают. После завершения реакции они оказались на границе раздела эвтектоидных колоний (рис. 2.8). Таким образом, структура сплава при температуре ниже 500 °С состоит из вторичных кристаллов компонента и эвтектоида: ВII+(α+В). 2.8. Анализ состояния сплава при заданной температуре На ординате, соответствующей заданному (согласно варианту задания) сплаву, нанести точку, отвечающую указанной в таблице температуре. Обозначить ее любой буквой. Написать ответ на первую часть вопроса: из каких фаз состоит сплав при заданной температуре. Название фаз выписать из области диаграммы, в которую попадает горизонтальная линия (конода), соответствующая заданной в варианте температуре. Для определения количественного соотношения фаз необходимо провести горизонталь (коноду) до пересечения с ближайшими линиями диаграммы. Конечные точки этой горизонтали обозначить какими-либо буквами и спроектировать на ось концентраций для определения состава (содержания компонентов А и В в процентах). Для определения веса фаз на 1 килограмм сплава необходимо воспользоваться формулой (2.4). Длины отрезков не следует измерять линейкой. Необходимо воспользоваться осью концентраций, т. к. при нахождении составов фаз были спроектированы конечные точки коноды на эту ось и определены их абсциссы в соответствующем масштабе. ПриложениЯ п.1. Оформление титульного листа домашнего П.2. Пример выполнения домашнего задания «Анализ двойных диаграмм» Задание №10–Д 1. Общий анализ диаграммы состояния системы «Ti – W». 2. Для сплава, содержащего 40 % W: · описать процесс кристаллизации при очень медленном охлаждении и, пользуясь правилом фаз, построить кривую охлаждения с указанием фазовых превращений на всех участках кривой; · указать, из каких фаз будет состоять сплав при температуре 1200 °С, состав фаз и их количество (вес) на 1 килограмм сплава. 1. Общий анализ диаграммы. Титан является полиморфным металлом. При температурном интервале 1660–882 °С он имеет кристаллическую решетку ГПУ (Tiβ), при температуре ниже 882 °С титан образует кристаллы на основе решетки ОЦК (Tiα). Вольфрам не имеет полиморфных модификаций. Ниже температуры кристаллизации (3380 °С) кристаллы вольфрама имеют решетку ОЦК. Титан и вольфрам неограниченно растворяются в жидком состоянии, образуя неограниченный жидкий раствор Ж. В твёрдом состоянии они растворяются друг в друге ограниченно, образуя три ограниченных твёрдых раствора: α-твёрдый растворв α-модификации титана, β-твёрдый растворвольфрама в β-модификации титана и γ-твёрдый раствор титана в вольфраме. Химических соединений титан и вольфрам не образуют. В системе «Титан – вольфрам» протекают два нонвариантных превращения: перитектическое и эвтектоидное. При температуре 1880 °С протекает перитектическая реакция, заключающаяся в том, что жидкий раствор Ж, содержащий 25 % вольфрама, взаимодействует с ранее выпавшими из него кристаллами γ-твёрдого раствора, содержащего 92 % вольфрама, в результате чего образуется новая фаза – кристаллы β-твёрдого раствора, содержащие 50 % вольфрама: При температуре 715 °С протекает эвтектоидное превращение, при котором β-твёрдый раствор, содержащий 28 % вольфрама, распадается в смесь α-твёрдого раствора, содержащего 0,8 % вольфрама, и γ-твёрдого раствора, содержащего 96 % вольфрама: 2. Описание процесса кристаллизации сплава с 40 % вольфрама. При температурах выше 2350° сплав находится в жидком состоянии и состоит из одной фазы – жидкого раствора Ж. На этом участке охлаждения в сплаве не происходит никаких фазовых превращений, наблюдается простое физическое охлаждение жидкого раствора. Система бивариантна: При достижении температуры 2350 °С в сплаве начинается процесс первичной кристаллизации, который состоит в том, что из жидкого раствора будут выпадать первичные кристаллы γ-твёрдого раствора (Ж → γ). где При температуре 1880° в сплаве будет протекать перитектическое превращение: жидкий раствор будет взаимодействовать с кристаллами Это превращение нонвариантно: При охлаждении от 1880 °С до 1820 °С остаток жидкого раствора будет кристаллизоваться в β-твёрдый раствор. Превращение моновариантно: В интервале температур 1820 °С до 1500 °С ни каких фазовых превращений в сплаве не происходит, идёт простое физическое охлаждение ненасыщенного β-твёрдого раствора. Система бивариантна: При температуре 1500 °С β-твёрдый раствор достигнет предела насыщения и в связи с тем, что при дальнейшем понижении температуры растворимость вольфрама в титане понижается, β-твёрдый раствор становится пересыщенным и избыток вольфрама выделяется из него со вторичными кристаллами γ-твёрдого раствора ( Состав β-твёрдого раствора будет изменяться по линии сольвус от точки 4 к точке 5»’. В связи с понижением растворимости титана в вольфраме γ-твёрдого раствора будут выпадать вторичные кристаллы β-твёрдого раствора ( К моменту достижения сплавом температуры 715 °С его структура состоит из кристаллов β-твёрдого раствора, образовавшегося в результате перитектического превращения при 1860 °С, и тех кристаллов β-твёрдого раствора, в которые закристаллизовался остаток жидкого раствора в интервале 1880 °С – 1820 °С. Кроме того, в структуре сплава будут вторичные кристаллы γ— и β-твёрдых растворов, выпавшие в интервале 1500 °C –715 °C. При температуре 715 °С в сплаве будет протекать эвтектоидное превращение: β-твёрдый раствор будет распадаться в смесь кристаллов α— и γ-твёрдых растворов: Эвтектоидное превращение нонвариантно: Рис. Диаграмма состояния системы «Ti – W» и кривая охлаждения сплава с 40 % W. При дальнейшем охлаждении ниже 715 °С вследствие понижения растворимости вольфрама в титане из α-твёрдого раствора будут выпадать третичные кристаллы γ-твёрдого раствора и состав его будет изменяться по линии сольвус от точки 5′ до точки 6′ (см. рисунок), а вследствие понижения растворимости титана в вольфраме из γ-твёрдого раствора будут выпадать вторичные кристаллы α-твёрдого раствора. Ниже 715 °С сплав моновариантен: Так как после эвтектоидного превращения в сплаве нет структурно самостоятельных кристаллов α-твёрдого раствора, а есть лишь мелкие кристаллы α-твёрдого раствора, входящие в состав эвтектоида и при средних увеличениях невидимые в микроскоп, то выпадающие из них еще более мелкие третичные кристаллы γ-твёрдого раствора тем более не будут видны; они останутся внутри эвтектоида и сольются с эвтектоидными кристаллами γ-твёрдого раствора. Таким образом, окончательная структура сплава будет состоять из вторичных кристаллов γ-твёрдого раствора, эвтектоида 3. Определение состава и количества фаз на 1 килограмм сплава. При температуре 1200° сплав с 40 % вольфрама: · состоит из двух фаз: (β-твёрдого раствора и γ-твёрдого раствора; · β-твёрдый раствор содержит 34 % W и 66 % Ti; · γ-твёрдый раствор содержит 95 % W и 5 % Ti; · вес β-твёрдого раствора: · вес γ-твёрдого раствора: Для выработки навыка разбора процессов, происходящих при охлаждении конкретного сплава, необходимо обязательно выполнение следующих действий: строить кривую охлаждения разбираемого сплава; против участков кривой охлаждения схематично изображать состояние фаз (структуру) сплава; письменно объяснять процесс, происходящий в сплаве при рассматриваемых температурных условиях. Варианты заданий для домашней работы ЭвтектикаЭвтектика, англ. eutectic, eutecticum (от греческого слова «éutektos» — легко плавящийся) — смесь компонентов, которые плавятся при определённой, минимальной температуре. Литейный сплав может являться эвтектикой (эвтектический сплав). Эвтектику в системах «соль — вода» называют криогидратами, используют как охлаждающие смеси. Эвтектика в сплавах представляет собой тонкую смесь твёрдых веществ, которые начинают кристаллизоваться одновременно из расплавов при температуре менее tпл отдельных компонентов или любых других их смесей [1]. Примером эвтектики может служить, например, ледебурит в чёрных сплавах (Метастабильная система железо-цементит). Согласно [4] эвтектика — это жидкая система (раствор или расплав), которая при данном давлении находится в равновесии с твёрдыми фазами, число которых равно числу компонентов системы. Кристаллизация эвтектики, как и кристаллизация чистых веществ, происходит при постоянной температуре согласно правилу фаз. При этом образуется твёрдая эвтектика — механическая смесь твёрдых фаз того же состава. Таким образом твёрдая эвтектика — это продукт кристаллизации жидкой эвтектики. Температура плавления твёрдой эвтектики для такой системы ниже температуры плавления смеси этой системы любого другого состава. Свойство образовывать эвтектику характерно для металлических и неметаллических систем, в которых не ограничена взаимная растворимость компонентов в жидком состоянии, в то время, как в твёрдом состоянии растворимость ограничена или отсутствует. На диаграмме состояния двойной эвтектической системы, компоненты которой в твёрдом состоянии не растворяются друг в друге (рисунок), кривые TAE и TBE зависимости температур начала кристаллизации чистых компонентов А и В от состава системы пересекаются в точке Е, в которой жидкость L насыщена одновременно обоими компонентами (эвтектическая точка). Диаграмма с эвтектическим превращениемДиаграмма с эвтектикой или диаграмма с эвтектическим превращением относится к диаграммам состояния сплавов с ограниченной растворимостью компонентов в твёрдом состоянии (III рода). В таких сплавах оба компонента неограниченно растворимы в жидком состоянии, ограниченно растворимы в твёрдом состоянии и не образуют химических соединений. Фазы сплавов с эвтектическим превращением: жидкость Ж, твёрдые растворы α (раствор компонента A в B) и β (раствор компонента B в A). Этот тип диаграмм очень важен, так как часто представлен в составе сложных диаграмм (Пример: Fe-C). На диаграмме с эвтектикой может быть не одно, а два и больше эвтектических превращений. Например, в двухкомпонентных системах Железо-Гольмий и Железо-Диспрозий наблюдается три эвтектики, что и отражено на диаграммах этих систем. Температура эвтектикиТемпература кристаллизации эвтектики — эвтектическая точка. В эвтектической точке температуры ликвидус и солидус совпадают. Для чистых железоуглеродистых сплавов температура образования эвтектики (ледебурита) немного ниже 1145°C. Т.е. эвтектика начинает образовываться при переохлаждении сплава ниже температуры 1145°C. ЭвтектичностьЭвтектичность, степень эвтектичности — показатель, определяющий количество графита в структуре чугуна с учётом содержания в нём C, Si, P, Mn и S. Эвтектичность выражают символами Sэт или SсSэ=C/[4,23-0,312Si-0,33P+0,18(Mn-1,76S)], или в более простом виде Sэ=C/(4,3-0,3Si). Величина эвтектичности характеризует чугун как доэвтектический (Sэ 1). Эвтектичность определяет структуру чугуна и его важнейшие механические свойства. Автор: Корниенко А.Э. (ИЦМ) Лит.:
Конкурс «Я и моя профессия: металловед, технолог литейного производства». Узнать, участвовать >>> —> Структурные и фазовые превращения в сталях при нагреве и охлаждении.Диаграмма железо- углерод, имеющая техническое применение, включает содержание углерода от 0 до 6,67% (Рисунок ) . Содержание углерода 6,67% соответствует 100%-ной доле химического соединения Fe3C, называемого цементитом. Таким образом, диаграмма железо- углерод представляет часть диаграммы между чистым компонентом А (Fe) и соединением В (Fe3C) . Сплошные линии соответствуют метастабильной системе Fe- Fe3C, пунктирные линии изображают стабильную систему Fe — C. В области до 4,3% С различия граничных фазовых линий между метастабильной и стабильной системами незначительны. Однако при длительном температурном воздействии и при более высоком содержании углерода цементит имеет склонность к распаду на железо и графит. Графит и цементит могут, как часто наблюдается у чугуна, появляться рядом друг с другом. Диаграмма Fe-Fe3C является характерным примером сложной системы, содержащей три превращения: 1. Перетектическое превращение с перитектической точкой при 0,16%С и 1493 о С (точка J), в результате чего из расплава и первично выделенного -твердого раствора (ОЦК) образуется —твердый раствор (ГЦК) по реакции:. 2. Эвтектическая реакция между расплавом, g-твердым раствором и Fe3C при 4,3% С и 1147 о С по реакции (точка С).. Эвтектическая горизонталь простирается от 2,14 до 6,67% С, соответственно от 31 до 100% Fe3C. Это означает, что при содержании С о С уменьшается до 0,8% при 723 о С.С максимальной растворимостью углерода в g-твердом растворе при 2% связываются границы для стали ( 2,14%). 3. Эвтектоидное превращение — твердого раствора (аустенит) в при 0,8%С и 723 о С по реакции (точка S). Диаграмма состояния железо-углерод При содержании С>2,14% наряду с первично выделенным — твердым раствором остаточный расплав превращается в эвтектику , которая при 4,3%С образуется как чистая эвтектика и называется также ледебуритом. На диаграмме Fe- Fe3C левее точки Е’находятся стали, правее — чугуны. Как видно из диаграммы, стали не испытывают эвтектического превращения. При температурах ниже 723 о С все стали (в отожженном состоянии) состоят из двух фаз — ферритаи цементита.Феррит-это твердый раствор углерода в a-Feс ОЦК решеткой. Максимальная растворимость углерода в a-Fe составляет около 0,025% (точка Р) Цементит — это карбид железа Fe3C, содержащий 6,7%С. Микроструктура сталей По микроструктуре в отожженном состоянии различают: а) техническое железо, не испытывающее эвтектоидное превращение (до 0,025%С); б) доэвтектоидные стали (от 0,025 до 0,8%С); в) эвтектоидные стали (0,8 %С); г) заэвтектоидные стали (от 0,8 до 2,14%С). В отожженном техническом железе микроструктура состоит либо только из равноосных зерен феррита (до 0,006%С), либо из равноосных зерен феррита с пограничными выделениями третичного цементита. Третичный цементит образуется по границам зерен феррита вследствие уменьшения растворимости углерода в феррите при понижении температуры, и образует разорванную сетку, т.к. количество его невелико. В отожженных доэвтектоидных сталях две структурные составляющие: избыточный феррит, образующийся в результате полиморфного превращения g ® a, и эвтектоид — перлит, который возникает при эвтектоидном превращении: g08®a0.025+Fe3C. Избыточный феррит при большом его количестве выделяется в виде равноосных зерен (рисунок 22), при малом количестве — в виде сетки по границам зерен аустенита (рисунок 23). Перлит имеет характерное пластинчатое строение и состоит из отдельных зерен — колоний (рисунок 24). Количественное соотношение феррита и цементита в перлите не зависит от состава стали. В отожженных заэвтектоидных сталях структурные составляющие — перлит и цементит вторичный. Последний выделяется из аустенита перед эвтектоидной реакцией из-за уменьшения растворимости углерода при понижении температуры. Вторичный цементит выделяется по границам зерен аустенита, образуя сетку (рисунок 25), заполненную колониями перлита, которые образуются из аустенита при эвтектоидном превращении. Таким образом, по микроструктуре можно качественно отличить стали с разным содержанием углерода. В таблице 1 приведены данные о фазовых и структурных составляющих сталей. Таблица 1 — Фазовое состояние и микроструктура отожженных углеродистых сталей
Фазы углеродистой стали сильно отличаются механическими свойствами: феррит мягок и пластичен, цементит тверд и хрупок. Ясно, что механические свойства стали зависят от свойств фаз, однако существенное влияние оказывает и микроструктура. Свойства отдельных фаз и перлита можно сравнить в таблице 2. Эвтектоидные и заэвтектоидные стали со структурой перлита или перлита с вторичным цементитом обладают повышенной твердостью. Если же сталь подвергнуть специальному отжигу (сфероидизирующий отжиг), выделения вторичного цементита и цементит эвтектоида принимают глобулярную форму (см. рисунок 26), а твердость снижается.
Таблица 2 — Механические свойства структурных составляющих в углеродистых сталях источники: http://www.modificator.ru/terms/eutektos.html http://zdamsam.ru/a7244.html |







 ,
,  где
где  .
. ,
, , сопровождается выделением тепла и идёт в интервале температур. На кривой охлаждения при температуре 2350 °С будет наблюдаться перегиб. Выпадение γ-твёрдого раствора из жидкого раствора будет продолжаться до температуры 1880 °С, при этом состав жидкого раствора будет изменяться по отрезку линии ликвидус от точки 1 к точке 2′, а состав кристаллов γ-твёрдого раствора – по отрезку линии солидус от точки 1» к точке 2″. К моменту достижения сплавом температуры 1880 °С он состоит из первичных кристаллов γ-твёрдого раствора и жидкого раствора.
, сопровождается выделением тепла и идёт в интервале температур. На кривой охлаждения при температуре 2350 °С будет наблюдаться перегиб. Выпадение γ-твёрдого раствора из жидкого раствора будет продолжаться до температуры 1880 °С, при этом состав жидкого раствора будет изменяться по отрезку линии ликвидус от точки 1 к точке 2′, а состав кристаллов γ-твёрдого раствора – по отрезку линии солидус от точки 1» к точке 2″. К моменту достижения сплавом температуры 1880 °С он состоит из первичных кристаллов γ-твёрдого раствора и жидкого раствора. , где
, где  , поэтому идёт при постоянной температуре и указанных концентрациях фаз. На кривой охлаждения температуре 1880 °С будет соответствовать горизонтальная площадка. Поскольку в сплаве жидкого раствора больше, чем необходимо для перитектического превращения, сплав в момент окончания превращения (точка 2′ на кривой охлаждения – рисунок) будет состоять из кристаллов β-твёрдого раствора и остатка жидкого раствора.
, поэтому идёт при постоянной температуре и указанных концентрациях фаз. На кривой охлаждения температуре 1880 °С будет соответствовать горизонтальная площадка. Поскольку в сплаве жидкого раствора больше, чем необходимо для перитектического превращения, сплав в момент окончания превращения (точка 2′ на кривой охлаждения – рисунок) будет состоять из кристаллов β-твёрдого раствора и остатка жидкого раствора. , сопровождается выделением тепла и идёт в интервале температур, при этом состав жидкого раствора будет изменяться по линии ликвидус от точки 2′ до точки 3′ (см. рисунок), а состав кристаллов β-твёрдого раствора – по линии солидус от точки 2′» до точки 3. К моменту достижения температуры 1820° сплав состоит только из кристаллов β-твёрдого раствора.
, сопровождается выделением тепла и идёт в интервале температур, при этом состав жидкого раствора будет изменяться по линии ликвидус от точки 2′ до точки 3′ (см. рисунок), а состав кристаллов β-твёрдого раствора – по линии солидус от точки 2′» до точки 3. К моменту достижения температуры 1820° сплав состоит только из кристаллов β-твёрдого раствора. ,
,  ) и при температуре 1820 °С на кривой охлаждения будет перегиб.
) и при температуре 1820 °С на кривой охлаждения будет перегиб. ).
).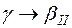 ). Состав γ-твёрдого раствора будет меняться по другой линии сольвус от точки 4» к точке 5″. Сплав моновариантен:
). Состав γ-твёрдого раствора будет меняться по другой линии сольвус от точки 4» к точке 5″. Сплав моновариантен:  где
где  , процессы идут в интервале температур, а на кривой охлаждения при 1500 °С будет перегиб.
, процессы идут в интервале температур, а на кривой охлаждения при 1500 °С будет перегиб. , идёт при постоянной температуре 715 °С и указанных концентрациях фаз и поэтому температуре 715 °С на кривой охлаждения будет соответствовать горизонтальная площадка. В момент окончания эв-тектоидного превращения (точка 5′ на кривой охлаждения – рисунок) структура сплава будет состоять из вторичных кристаллов γ-твёрдого раствора и эвтектоида
, идёт при постоянной температуре 715 °С и указанных концентрациях фаз и поэтому температуре 715 °С на кривой охлаждения будет соответствовать горизонтальная площадка. В момент окончания эв-тектоидного превращения (точка 5′ на кривой охлаждения – рисунок) структура сплава будет состоять из вторичных кристаллов γ-твёрдого раствора и эвтектоида 

 и состоит из двух фаз (α— и γ-твердые растворы). Описанные процессы (
и состоит из двух фаз (α— и γ-твердые растворы). Описанные процессы (  сопровождаются выделением тепла и идут в интервале температур.
сопровождаются выделением тепла и идут в интервале температур. и вторичных кристаллов α-твёрдого раствора:
и вторичных кристаллов α-твёрдого раствора: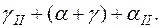
 ;
; .
.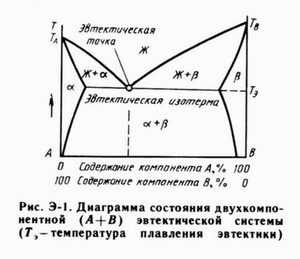

 Рисунок 21 — Схема микроструктуры технического железа: феррит и третичный цементит по границам зерен
Рисунок 21 — Схема микроструктуры технического железа: феррит и третичный цементит по границам зерен Рисунок 22 — Схема микроструктуры доэвтектоидной стали: зерна избыточного феррита и перлит
Рисунок 22 — Схема микроструктуры доэвтектоидной стали: зерна избыточного феррита и перлит Рисунок 23 — Схема микроструктуры перлита
Рисунок 23 — Схема микроструктуры перлита Рисунок 24 — Схема микроструктуры доэвтектоидной стали: сетка избыточного феррита и перлит
Рисунок 24 — Схема микроструктуры доэвтектоидной стали: сетка избыточного феррита и перлит Рисунок 25 — Схема микроструктуры заэвтектоидной стали: сетка вторичного цементита и перлит
Рисунок 25 — Схема микроструктуры заэвтектоидной стали: сетка вторичного цементита и перлит Рисунок 26 — Схема микроструктуры заэвтектоидной стали: феррит и зернистый цементит
Рисунок 26 — Схема микроструктуры заэвтектоидной стали: феррит и зернистый цементит