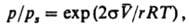Капиллярная конденсация
Капиллярная конденсация — сжижение пара в капиллярах, щелях или порах в твердых телах. Происходит при условии смачивания жидкостью поверхности конденсации и вследствие пониженного давления насыщенного пара р над вогнутым мениском по сравнению с давлением насыщенного пара рs над плоской поверхностью жидкости при той же температуре Т. Кол-во удерживаемой капиллярными силами жидкости зависит от радиуса кривизны r поверхности раздела жидкость — пар согласно уравнению Кельвина:
где s — поверхностное (межфазное) натяжение, V — молярный объем жидкости, R — газовая постоянная. Предельное количество жидкости достигается при р = ps, что отвечает плоской поверхности раздела (заполнение всех пор жидкостью) или поверхности катеноида. Капиллярной конденсации предшествует адсорбция пара на поверхности конденсации. Капиллярная конденсация начинается при таком значении равновесного количества адсорбировавшегося вещества, при котором образуется мениск жидкости с радиусом кривизны r0 более 2-3 диаметров молекулы. Согласно уравнению Кельвина, при этом p/ps / 0,2-0,3. В узких порах на величину r0 влияет наличие адсорбционных пленок, расхождение σ и V с табличными значениями, а также искажение формы мениска полем поверхностных сил. Для микропор (r0 1 нм) уравнение Кельвина неприменимо; поглощение пара микропорами аналогично растворению газа конденсированными телами. Сложность конфигурации порового пространства может быть причиной капиллярного гистерезиса, проявляющегося в том, что количество удерживаемой жидкости зависит не только от значения p/ps, но и от того, достигнуто ли данное состояние в ходе конденсации пара (кривая 1 на рис.) или же в ходе испарения жидкости (кривая 2).
Изотерма адсорбции в капиллярах и петля капиллярного гистерезиса. 1 и 2 — кривые конденсации пара и испарения жидкости соответственно.
Одно из этих состояний, а именно отвечающее большему массосодержанию (кривая 2), является метастабильным. Капиллярный гистерезис наблюдается обычно, если поры имеют форму бутылок или четок вследствие блокировки узкими перешейками жидкости, содержащейся в расширенной части пор, а также в случае цилиндрических пор, если образование конденсата происходит в результате утолщения и последующей смыкания адсорбционных пленок. Опорожнение таких пор начинается при более низком давлении пара, чем заполнение. Для расчета изотерм используют модельные системы — ансамбли цилиндрических или щелевых пор различных размеров, решеточные системы, а также упаковки из частиц правильной формы. Обычно уравнения используют для решения обратной задачи: определения размеров пор и их распределения по размерам на основании изотерм опорожнения пор, с привлечением модельных представлений о геометрии порового пространства. Капиллярная конденсация может наблюдаться не только в системах жидкость — пар, но и в заполняющих пористое тело бинарных жидких смесях вблизи критической точек смешения, а также в промерзающих пористых телах при наличии прослоек незамерзающей воды на внутренней поверхности пор. Капиллярную конденсацию используют для улавливания паров пористыми сорбентами. Большую роль капиллярная конденсация играет также в процессах сушки, удерживания влаги почвами, строительными и другими пористыми материалами. При p/ps
Какое уравнение лежит в основе теории капиллярной конденсации
Капиллярная конденсация обусловлена проявлением капиллярных сил, что связано со сродством адсорбата к адсорбенту. Основываясь на закономерностях капиллярных явлений, можно утверждать, что сродство должно быть достаточно для смачивания поверхности твердого тела жидкостью, появляющейся в результате конденсации в порах. Только в случае смачивания адсорбент будет втягивать в поры адсорбат, увеличивая тем самым адсорбцию. Чем меньше размер пор, тем сильнее капиллярное удерживание адсорбата. Если поверхность не смачивается, то наблюдается явление капиллярного выталкивания, адсорбция в этом случае минимальна и возможна только в крупных порах.
В адсорбентах с порами капиллярных размеров на стенках пор вначале образуется мономолекулярный, затем двойной и последующие слои адсорбата. Тем самым на стенке постепенно создается вогнутая поверхность жидкости, в которую превратился адсорбированный пар. Радиус кривизны поверхности постепенно уменьшается по мере утолщения слоя жидкости на стенках. Этот слой жидкости находится в равновесии с паром, заполняющим поровое пространство.
В случае плоской границы раздела фаз конденсация пара в жидкость при данной температуре происходит когда давление становится равным давлению насыщенного пара, то есть при P/P S = 1. Конденсация над вогнутой поверхностью в порах происходит при несколько меньшем давлении насыщенного пара, то есть при P/P S Давление насыщенного пара над искривленной поверхностью отличается от давления насыщенного пара над плоской поверхностью, что приводит к изменению химического потенциала над искривленной поверхностью и изменяет условия фазового равновесия в порах. Условием фазового равновесия является равенство химических потенциалов пара и жидкости:
где P давление насыщенного пара над искривленной поверхностью, PS — давление насыщенного пара над плоской поверхностью. Приращение химического потенциала за счет лапласова давления при изменении кривизны поверхности для однокомпонентной системы в изотермических условиях соответствует работе расширения:
После подстановок и необходимых преобразований получаем уравнение Томсона (Кельвина), связывающее давление P , при котором пар будет насыщенным по отношению к искривленной поверхности, c радиусом кривизны r :
На изотерме адсорбции этот участок проявляется в виде резкого подъема (изотермы IV и V типа), положение которого зависит от радиуса пор.
Размеры радиусов менисков подчиняются уравнению капиллярной конденсации Томсона (Кельвина) .
где р — давление пара над искривленным мениском;
рs — давление насыщенного пара над плоской поверхностью ;
s — поверхностное натяжение конденсированной жидкости;
r — радиус кривизны мениска.
σ — поверхностное натяжение жидкости, образов. при конденсации пара
R — газовая постоянная
Vm — молярный объем жидкости
Из уравнения видно, что при смачивании обеспечивается отрицательная кривизна мениска конденсата (вогнутый мениск), конденсация в порах наступает при давлении , которое меньше давления насыщенного пара , т.е. р/рs давление насыщения над поверхностью .
где φ — относительное давление пара, равное отношению давления пара на поверхности жидкости ρп к давлению насыщенного пара свободной жидкости ρ0 (давление над свободной поверхностью жидкости).
Если перепад давления Δρж определяется кривизной поверхности жидкости, то
Формула Томсона проверялась прямыми экспериментами. К. В. Чмутов опытами по капиллярной конденсации паров различных жидкостей в щели показал, что формула Томсона не применима к вычислению радиусов пор сорбентов.
Таким образом, значения радиусов цилиндрического капилляра, получаемые по последней формуле в зависимости от относительной упругости пара надо считать грубо ориентировочными.
Из табл. 1-3 видно, что при φ = 0,1 (давление насыщенного пара над мениском капилляра в 10 раз меньше давления насыщенного пара над плоской поверхностью) радиус капилляра равен 0,46•10-7 см. Для капилляра радиусом r = 1,07•10-5 см давление насыщенного пара практически не отличается от давления насыщенного пара над плоской поверхностью с точностью до 1 %.
Такой вывод послужил одной из причин, позволяющих считать капилляры с радиусом r>10-5 см макрокапиллярами в отличие от микрокапилляров, радиус которых r
1) Матвеев А.Н. Молекулярная физика: Учеб. Пособие для вузов. –М: Высшая школа,
1981.
2) Адсорбционные явления и поверхность (Рощина Т.М. , 1998), Химия. (Статья Соросовского образовательного журнала)
КАПИЛЛЯ́РНЫЕ ЯВЛЕ́НИЯ
В книжной версии
Том 13. Москва, 2009, стр. 17
Скопировать библиографическую ссылку:
КАПИЛЛЯ́РНЫЕ ЯВЛЕ́НИЯ, совокупность явлений, обусловленных поверхностным натяжением на границе раздела несмешивающихся сред (в системах жидкость – жидкость, жидкость – газ или пар) при наличии искривления поверхности. Частный случай поверхностных явлений .
http://www.sites.google.com/site/kolloidnaahimia/adsorbcia-svistat-vseh-na-poverhnost/uilam-tomson-kelvin/uravnenie-tomsona-kelvina
http://bigenc.ru/physics/text/2042928