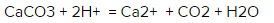Кальций: способы получения и химические свойства
Кальций Ca — это щелочноземельный металл, серебристо-белый, пластичный, достаточно твердый. Реакционноспособный. Сильный восстановитель.
Относительная молекулярная масса Mr = 40,078; относительная плотность для твердого и жидкого состояния d = 1,54; tпл = 842º C; tкип = 1495º C.
Способ получения
1. В результате электролиза жидкого хлорида кальция образуются кальций и хлор :
2. Хлорид кальция взаимодействует с алюминием при 600 — 700º С образуя кальций и хлорид алюминия:
3CaCl2 + 2Al = 3Ca + 2AlCl3
3. В результате разложения гидрида кальция при температуре выше 1000º С образуется кальций и водород:
4. Оксид кальция взаимодействует с алюминием при 1200º С и образует кальций и алюминат кальция:
4CaO + 2Al = 3Ca + Ca(AlO2)2
Качественная реакция
Кальций окрашивает пламя газовой горелки в коричнево-красный цвет.
Химические свойства
1. Кальций — сильный восстановитель . Поэтому он реагирует почти со всеми неметаллами :
1.1. Кальций взаимодействует с азотом при 200 — 450º С образуя нитрид кальция:
1.2. Кальций сгорает в кислороде (воздухе) при выше 300º С с образованием оксида кальция:
2Ca + O2 = 2CaO
1.3. Кальций активно реагирует при температуре 200 — 400º С с хлором, бромом и йодом . При этом образуются соответствующие соли :
1.4. С водородом кальций реагирует при температуре 500 — 700º C с образованием гидрида кальция:
1.5. В результате взаимодействия кальция и фтора при комнатной температуре образуется фторид кальция:
1.6. Кальций взаимодействует с серой при 150º С и образует сульфид кальция:
Ca + S = CaS
1.7. В результате реакции между кальцием и фосфором при 350 — 450º С образуется фосфид кальция:
1.8. Кальций взаимодействует с углеродом (графитом) при 550º С и образует карбид кальция:
Ca + 2C = CaC2
2. Кальций активно взаимодействует со сложными веществами:
2.1. Кальций при комнатной температуре реагирует с водой . Взаимодействие кальция с водой приводит к образованию гидроксида кальция и газа водорода:
2.2. Кальций взаимодействует с кислотами:
2.2.1. Кальций реагирует с разбавленной соляной кислотой, при этом образуются хлорид кальция и водород :
Ca + 2HCl = CaCl2 + H2 ↑
2.2.2. Реагируя с разбавленной азотной кислотой кальций образует нитрат кальция, оксид азота (I) и воду:
если азотную кислоту еще больше разбавить, то образуются нитрат кальция, нитрат аммония и вода:
2.3. Кальций вступает в реакцию с газом аммиаком при 600 — 650º С. В результате данной реакции образуется нитрид кальция и гидрид кальция:
если аммиак будет жидким, то в результате реакции в присутствии катализатора платины образуется амид кальция и водород:
Кальций це о три плюс аш хлор?
Химия | 5 — 9 классы
Кальций це о три плюс аш хлор.
СaCO3 + 2HCl — > CaCl2 + CO2 ↑ + H2O.
СаСО3 + 2HCl = CaCl2 + CO2↑ + H2O.
Осуществите следующие превращения кальций стрелка кальций O стрелка хлорид кальция стрелка аргентум хлор?
Осуществите следующие превращения кальций стрелка кальций O стрелка хлорид кальция стрелка аргентум хлор.
Помогите составить ионную связь атомов кальция и хлора?
Помогите составить ионную связь атомов кальция и хлора.
Запишите уравнения реакции : — фосфор + кальций ; — фосфор + кислород ; — кальций + азот ; — магний + хлор?
Запишите уравнения реакции : — фосфор + кальций ; — фосфор + кислород ; — кальций + азот ; — магний + хлор.
В каких процентах соотношениях нужно взять кальций хлор для получения хлорида кальция?
В каких процентах соотношениях нужно взять кальций хлор для получения хлорида кальция.
Феррум хлор плюс калий о аш?
Феррум хлор плюс калий о аш.
Купрум о аш дважды плюс аш хлор?
Купрум о аш дважды плюс аш хлор.
Охарактеризуйте хлор и кальций по плану на фото?
Охарактеризуйте хлор и кальций по плану на фото.
Дать характеристику хлору?
Дать характеристику хлору.
Так как показано на примере кальция.
Медь реагирует с цинкомхлоромкальцием азотом?
Медь реагирует с цинком
Толуол плюс три моль хлора?
Толуол плюс три моль хлора.
Если вам необходимо получить ответ на вопрос Кальций це о три плюс аш хлор?, относящийся к уровню подготовки учащихся 5 — 9 классов, вы открыли нужную страницу. В категории Химия вы также найдете ответы на похожие вопросы по интересующей теме, с помощью автоматического «умного» поиска. Если после ознакомления со всеми вариантами ответа у вас остались сомнения, или полученная информация не полностью освещает тематику, создайте свой вопрос с помощью кнопки, которая находится вверху страницы, или обсудите вопрос с посетителями этой страницы.
Решение : (А) Al / Al2(SO4)3 / / Fe2(SO4)3 / Fe (К) Уравнение электродных процессов : Al( — ) : Al — 3e = Al(3 + ) Fe( + ) : Fe(3 + ) + 3e = Fe Уравнение реакции : 2Al + Fe2(SO4)3 — — — >Al2(SO4)3 + 2Fe.
200 : 100 = 2 г — это 1% 2×12 = 24 г — уксусной кислоты 200 — 24 = 176 г — воды.
Решение см. В приложении. Желаю удачи.
Хех, это никто не знает ахахахах.
Поняла ошибку, сейчас напечатаю (внимание : во вложении нет решения, при разборе задачи не сверяйтесь с ним) Сумма АТОМОВ равна 3, 01 * 10 ^ 23, в таком случае составим уравнения : Nат(KBr) = 2 * Nмол(KBr) (так как в молекуле бродида калия только два..
1) сахар и сода : а) сходства — твердые, белого цвета, хорошо растворимы в воде. Б) различия — сахар сладкий, имеет низкую температуру плавления, его кристаллы крупнее, чем у соды и прозрачные. 2) вода и уксус : а) сходства — при обычных условиях б..
Алканами называют предельные углеводороды. Их общая формула : CnH2n + 2 1) CH4 — алкан, метан 2) C3H6 — алкЕн, пропен (пропилен) 3) C2H2 к алканам не относится 4) C4H16 к алканам не относится.
Т. к N2 — отсюда тройная связь. Хим. связь — ков. Неполярная(два одинаковых атома).
Какое ионное уравнение реакции CaCO3 + 2HCl?
Каким будет ионное уравнение реакции CaCO3 + 2HCl = CaCl2 + CO2 + H20?
Объясните как составить ионное уравнение этой реакции?
Как составить ионное уравнение реакции CaCO3 (карбоната кальция) и 2HCl (хлорной кислоты)?
Тип реакции: кислотно-основный.
В результате реакции карбонат кальция и 2 молекул хлорной кислоты, HCl нейтрализуется с образованием слабой неустойчивой кислоты H2CO3, которая не может оставаться в таком виде, потому распадается на углекислый газ CO2 и воду H2O.
Чтобы составить ионную реакцию, нужно сделать следующее:
- Проанализировать компоненты молекулярной реакции.
- Разложить на ионы газы, жидкости и растворы, а твердые вещества не трогать.
- Убрать с обоих сторон одинаковые ионы, записать конечный вид ионной реакции CaCO3 и 2HCl.
Итак, вот молекулярное уравнение:
Теперь нужно разобрать каждую составляющую этого уравнения, чтобы составить правильное ионное уравнение:
- CaCO3 не растворяется (ведь это обычный мел);
- HCl — кислота, растворяющаяся в воде;
- CaCl2 — хлорид кальция, растворяющийся в воде.
- H20 — это вода, в ионной реакции она не участвует;
- CO2 — газ, в данной ионной реакции он не участвует.
Теперь можно разложить составляющие на ионы (раскладывается только 2HCL и CaCl2):
CaCO3 (твердый элемент) + 2Cl- + 2H+ = Ca2+ + 2Cl- + CO2 + H2O
Что мы имеем? В обеих частях уравнения есть ионы хлора, потому их можно сократить. И вот что мы получаем в итоге:
Если вы любознательны и хотите знать больше, читайте также вопросы:
http://himia.my-dict.ru/q/7769624_kalcij-ce-o-tri-plus-as/
http://vovet.ru/q/kakoe-ionnoe-uravnenie-reakczii-caco3-2hcl-dt2.html