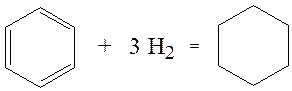Химические свойства аренов
Арены (ароматические углеводороды) – это непредельные (ненасыщенные) циклические углеводороды, молекулы которых содержат устойчивые циклические группы атомов (бензольные ядра) с замкнутой системой сопряженных связей.
Общая формула: CnH2n–6 при n ≥ 6.
Химические свойства аренов
Арены – непредельные углеводороды, молекулы которых содержат три двойных связи и цикл. Но из-за эффекта сопряжения свойства аренов отличаются от свойств других непредельных углеводородов.
Для ароматических углеводородов характерны реакции:
- присоединения,
- замещения,
- окисления (для гомологов бензола).
| Из-за наличия сопряженной π-электронной системы молекулы ароматических углеводородов вступают в реакции присоединения очень тяжело, только в жестких условиях — на свету или при сильном нагревании, как правило, по радикальному механизму |
| Бензольное кольцо представляет из себя скопление π-электронов, которое притягивает электрофилы. Поэтому для ароматических углеводородов характерны реакции электрофильного замещения атома водорода у бензольного кольца. |
Ароматическая система бензола устойчива к действию окислителей. Однако гомологи бензола окисляются под действием перманганата калия и других окислителей.
1. Реакции присоединения
Бензол присоединяет хлор на свету и водород при нагревании в присутствии катализатора.
1.1. Гидрирование
Бензол присоединяет водород при нагревании и под давлением в присутствии металлических катализаторов (Ni, Pt и др.).
При гидрировании бензола образуется циклогексан:
При гидрировании гомологов образуются производные циклоалканы. При нагревании толуола с водородом под давлением и в присутствии катализатора образуется метилциклогексан:
1.2. Хлорирование аренов
Присоединение хлора к бензолу протекает по радикальному механизму при высокой температуре, под действием ультрафиолетового излучения.
При хлорировании бензола на свету образуется 1,2,3,4,5,6-гексахлорциклогексан (гексахлоран).
Гексахлоран – пестицид, использовался для борьбы с вредными насекомыми. В настоящее время использование гексахлорана запрещено.
Гомологи бензола не присоединяют хлор. Если гомолог бензола реагирует с хлором или бромом на свету или при высокой температуре (300°C), то происходит замещение атомов водорода в боковом алкильном заместителе, а не в ароматическом кольце.
| Например, при хлорировании толуола на свету образуется бензилхлорид |
| Если у гомолога бензола боковая цепь содержит несколько атомов углерода – замещение происходит у атома, ближайшему к бензольному кольцу («альфа-положение»). |
| Например, этилбензол реагирует с хлором на свету |
2. Реакции замещения
| Реакции замещения у ароматических углеводородов протекают по ионному механизму (электрофильное замещение). При этом атом водорода замещается на другую группу (галоген, нитро, алкил и др.). |
2.1. Галогенирование
Бензол и его гомологи вступают в реакции замещения с галогенами (хлор, бром) в присутствии катализаторов (AlCl3, FeBr3).
При взаимодействии с хлором на катализаторе AlCl3 образуется хлорбензол:
Ароматические углеводороды взаимодействуют с бромом при нагревании и в присутствии катализатора – FeBr3 . Также в качестве катализатора можно использовать металлическое железо.
Бром реагирует с железом с образованием бромида железа (III), который катализирует процесс бромирования бензола:
| Гомологи бензола содержат алкильные заместители, которые обладают электронодонорным эффектом: из-за того, что электроотрицательность водорода меньше, чем углерода, электронная плотность связи С-Н смещена к углероду. На нём возникает избыток электронной плотности, который далее передается на бензольное кольцо. |
| Поэтому гомологи бензола легче вступают в реакции замещения в бензольном кольце. При этом гомологи бензола вступают в реакции замещения преимущественно в орто— и пара-положения |
| Например, при взаимодействии толуола с хлором образуется смесь продуктов, которая преимущественно состоит из орто-хлортолуола и пара-хлортолуола |
Мета-хлортолуол образуется в незначительном количестве.
При взаимодействии гомологов бензола с галогенами на свету или при высокой температуре (300 о С) происходит замещение водорода не в бензольном кольце, а в боковом углеводородном радикале.
| Если у гомолога бензола боковая цепь содержит несколько атомов углерода – замещение происходит у атома, ближайшему к бензольному кольцу («альфа-положение»). |
Например, при хлорировании этилбензола:
2.2. Нитрование
Бензол реагирует с концентрированной азотной кислотой в присутствии концентрированной серной кислоты (нитрующая смесь).
При этом образуется нитробензол:
| Серная кислота способствует образованию электрофила NO2 + : |
Толуол реагирует с концентрированной азотной кислотой в присутствии концентрированной серной кислоты.
В продуктах реакции мы указываем либо о-нитротолуол:
Нитрование толуола может протекать и с замещением трех атомов водорода. При этом образуется 2,4,6-тринитротолуол (тротил, тол):
2.3. Алкилирование ароматических углеводородов
- Арены взаимодействуют с галогеналканами в присутствии катализаторов (AlCl3, FeBr3 и др.) с образованием гомологов бензола.
| Например, бензол реагирует с хлорэтаном с образованием этилбензола |
- Ароматические углеводороды взаимодействуют с алкенами в присутствии хлорида алюминия, бромида железа (III), фосфорной кислоты и др.
| Например, бензол реагирует с этиленом с образованием этилбензола |
| Например, бензол реагирует с пропиленом с образованием изопропилбензола (кумола) |
- Алкилирование спиртами протекает в присутствии концентрированной серной кислоты.
| Например, бензол реагирует с этанолом с образованием этилбензола и воды |
2.4. Сульфирование ароматических углеводородов
Бензол реагирует при нагревании с концентрированной серной кислотой или раствором SO3 в серной кислоте (олеум) с образованием бензолсульфокислоты:
3. Окисление аренов
Бензол устойчив к действию даже сильных окислителей. Но гомологи бензола окисляются под действием сильных окислителей. Бензол и его гомологи горят.
3.1. Полное окисление – горение
При горении бензола и его гомологов образуются углекислый газ и вода. Реакция горения аренов сопровождается выделением большого количества теплоты.
Уравнение сгорания аренов в общем виде:
При горении ароматических углеводородов в недостатке кислорода может образоваться угарный газ СО или сажа С.
Бензол и его гомологи горят на воздухе коптящим пламенем. Бензол и его гомологи образуют с воздухом и кислородом взрывоопасные смеси.
3.2. О кисление гомологов бензола
Гомологи бензола легко окисляются перманганатом и дихроматом калия в кислой или нейтральной среде при нагревании.
При этом происходит окисление всех связей у атома углерода, соседнего с бензольным кольцом, кроме связи этого атома углерода с бензольным кольцом.
Толуол окисляется перманганатом калия в серной кислоте с образованием бензойной кислоты:
Если окисление толуола идёт в нейтральном растворе при нагревании, то образуется соль бензойной кислоты – бензоат калия:
Таким образом, толуол обесцвечивает подкисленный раствор перманганата калия при нагревании.
| При окислении других гомологов бензола всегда остаётся только один атом С в виде карбоксильной группы (одной или нескольких, если заместителей несколько), а все остальные атомы углерода радикала окисляются до углекислого газа или карбоновой кислоты. |
| Например, при окислении этилбензола перманганатом калия в серной кислоте образуются бензойная кислота и углекислый газ |
| Например, при окислении этилбензола перманганатом калия в нейтральной кислоте образуются соль бензойной кислоты и карбонат |
Более длинные радикалы окисляются до бензойной кислоты и карбоновой кислоты:
При окислении пропилбензола образуются бензойная и уксусная кислоты:
Изопропилбензол окисляется перманганатом калия в кислой среде до бензойной кислоты и углекислого газа:
4. Ориентирующее действие заместителей в бензольном кольце
Если в бензольном кольце имеются заместители, не только алкильные, но и содержащие другие атомы (гидроксил, аминогруппа, нитрогруппа и т.п.), то реакции замещения атомов водорода в ароматической системе протекают строго определенным образом, в соответствии с характером влияния заместителя на ароматическую π-систему.
| Заместители подразделяют на две группы в зависимости от их влияния на электронную плотность ароматической системы: электронодонорные (первого рода) и электроноакцепторные (второго рода). |
Типы заместителей в бензольном кольце
| Заместители первого рода | Заместители второго рода |
| Дальнейшее замещение происходит преимущественно в орто— и пара-положение | Дальнейшее замещение происходит преимущественно в мета-положение |
| Электронодонорные, повышают электронную плотность в бензольном кольце | Электроноакцепторные, снижают электронную плотность в сопряженной системе. |
|
|
| Например, толуол реагирует с хлором в присутствии катализатора с образованием смеси продуктов, в которой преимущественно содержатся орто-хлортолуол и пара-хлортолуол. Метильный радикал — заместитель первого рода. |
В уравнении реакции в качестве продукта записывается либо орто-толуол, либо пара-толуол.
| Например, при бромировании нитробензола в присутствии катализатора преимущественно образуется мета-хлортолуол. Нитро-группа — заместитель второго рода |

5. Особенности свойств стирола
Стирол (винилбензол, фенилэтилен) – это производное бензола, которое имеет в своем составе двойную связь в боковом заместителе.
Общая формула гомологического ряда стирола: CnH2n-8.
| Молекула стирола содержит заместитель с кратной связью у бензольного кольца, поэтому стирол проявляет все свойства, характерные для алкенов – вступает в реакции присоединения, окисления, полимеризации. |
Стирол присоединяет водород, кислород, галогены, галогеноводороды и воду в соответствии с правилом Марковникова.
| Например, при гидратации стирола образуется спирт: |
| Стирол присоединяет бром при обычных условиях, то есть обесцвечивает бромную воду |
При полимеризации стирола образуется полистирол:
Как и алкены, стирол окисляется водным раствором перманганата калия при обычных условиях. Обесцвечивание водного раствора перманганата калия — качественная реакция на стирол:
При жестком окислении стирола перманганатом калия в кислой среде (серная кислота) разрывается двойная связь и образуется бензойная кислота и углекислый газ:
При окислении стирола перманганатом калия в нейтральной среде при нагревании также разрывается двойная связь и образуется соль бензойной кислоты и карбонат:
Гидрирование бензола
Гидрирование бензола осуществляется в паровой фазе при давлении1,6-2,0 МПа (16-20 атм.), температуре125-250 о С на никельхромовом катализаторе в 2-х реакторах: трубчатом реакторе со съемом тепла кипящим конденсатом и в колонном реакторе адиабатического типа.
Реакция гидрирования бензола в циклогексан протекает по уравнению:
Гидрирование бензола проводится водородом из азотоводородной фракции, поступающей с производства аммиака, а также используется отбросной водород из отделения дегидрирования анола.
Давление в системе не более 2,0 МПа и мольное соотношение газ-бензол поддерживается за счет циркуляции водорода после гидрирования с помощью циркуляционного компрессора и подачи свежего водорода с давлением 2,0-2,4 МПа.
Молярное соотношение газ — бензол поддерживается равным 8:1 регулированием подачи бензола и циркуляционного водорода.
Для исключения проскока бензола концентрация водорода в циркуляционном газе поддерживается в пределах 20-30 % об. за счет сдувок части циркуляционного газа из системы. Кроме этого необходимо иметь определенную объемную скорость бензола на катализаторе. Максимальная объемная скорость бензола на никельхромовом катализаторе 1,5 л бензола на 1 л катализатора в час. При этом обеспечивается полное превращение бензола в циклогексан.
Однако, реакция гидрирования бензола по высоте слоя катализатора проходит неравномерно: не менее 90 % бензола превращается в циклогексан на 30 % от общего объема катализатора, т.е. при высокой объемной скорости.
Особенность процесса гидрирования бензола требует разбавления катализатора в 1-ом реакторе: в верхнем слое 1 : 8, в среднем 1: 2, нижнем –чистый катализатор. Во 2-ом реакторе колонного типа загружается около 40 % общего объема катализатора без разбавления.
Реакция гидрирования- процесс экзотермический, поэтому для поддержания температуры в пределах 125-250 о С необходим съем тепла. Тепло реакции в реакторе трубчатого типа снимается кипящим конденсатом, тепло реакции во 2-ом реакторе снимается рабочей смесью за счет увеличения ее теплосодержания.
При повышении температуры реакции выше 250 о С происходит изомеризация циклогексана в метилциклопентан.
К качеству бензола предъявляются высокие требования и оно должно соответствовать нормам по ГОСТ 9572-93, представленным в таблице 2
| Наименование | Норма для марок | |||
| высшей очистки | очищенный | для синтеза | ||
| второй | первый | |||
| 1. Внешний вид и цвет | Прозрачная жидкость не содержащая пос-торонних примесей и воды , не темнее раствора 0,003 г К2Сr2О7 в 1 дм 3 воды | |||
| 2. Плотность при 20 о С, г/см 3 | 0,878-0,880 | 0,878-0,880 | 0,878-0,880 | 0,878-0,880 |
| 3. Пределы перегонки 95 %, о С, не более (включая температуру кипения чистого бензола 80,1 о С) | — | — | 0,6 | 0,6 |
| 4. Температура кристаллизации, о С, не ниже | 5,40 | 5,40 | 5,35 | 5,30 |
| 5. Массовая доля основного вещества, %, не менее | 99,9 | 99,8 | 99,7 | 99,5 |
| 6. Массовая доля примесей, %, не более: н-гептана метилциклогексана + толуола метилциклогексана толуола | 0,01 0,05 0,02 — | 0,06 0,09 0,04 0,03 | 0,06 0,13 0,08 — | — — — — |
| 7. Окраска серной кислоты, номер образцовой шкалы, не более | 0,1 | 0,1 | 0,1 | 0,15 |
| 8. Массовая доля общей серы, %, не более | 0,00005 | 0,00010 | 0,00010 | 0,00015 |
| 9. Реакция водной вытяжки | нейтральная |
Прежде всего, жесткие нормы установлены по содержанию серы, н- гептана, метилциклогексана и толуола. При гидрировании бензола первые 2 примеси не подвергаются изменениям, а толуол превращается в метилциклогексан.
При окислении циклогексана н- гептан и метилциклогексан окисляются до гептанона –2, который имеет точку кипения, близкую к точке кипения , циклогексанона , поэтому его трудно отделить ректификацией.
Гептанон-2 на стадиях оксимирования и перегруппировки превращается в амиды кислот , что ухудшает качество капролактама.
Следует отметить, что никельхромовый катализатор очень чувствителен к серосодержащим примесям, которые являются контактными ядами. Наиболее сильным каталитическим ядом является тиофен. Его отравляющее действие в 5 раз выше, чем сероводорода и сероуглерода.
Серосодержащие соединения хемосорбируются поверхностью катализатора необратимо отравляя его, снижается активность катализатора и степень превращения бензола.
Для обеспечения длительной эксплуатации никельхромового катализатора при содержании в бензоле и в водороде серы более 1,5 ррм предусматривается форконтактная очистка бензола и водорода на медьсодержащих катализаторах или цинковым поглотителем.
Снижение активности никельхромового катализатора вызывает также наличие аммиака в водороде в количестве более 300 мг / м 3 .
Каталитическое гидрирование аренов
Для гидрирования ароматических систем нужны более суровые условия с применением катализаторов.
Применение платинового и никелевого катализатора: Гидрирование на никеле заканчивается формированием смеси цис- и транс-изомеров. Использование этих катализаторов оправдано при температуре 150 – 160 градусов. Вещества, которые негативно влияют на катализатор: тиофен и его гомологи.
Не нашли что искали?
Просто напиши и мы поможем
Для очистки ароматических углеводородов показано добавление серной кислоты высокой концентрации. Затем раствор встряхивают тиофен связывается с кислотой. После отмывания углеводородного слоя (вода/щелочь/вода), субстанцию обрабатывают хлористым кальцием процесс очистки заканчивается перегоном полученного продукта над натрием. По такой же схеме можно гидрировать нафталин.
Углеводороды, которые получены в результате гидрирования аренов используется в промышленности как растворители или горючее для ДВС. Использование никелевого катализатора имеет ряд условий: нагревание раствора выше 100 градусов, давление водорода 15 атмосфер. До начала реакции нафталин нужно очистить. Гидрирование над никелем производных бензола осуществляется также при высокой температуре и повышенном давлении. Над платиной гидрировать можно пиридин, пиррол и прочее.
Стереоселективность отсутствует при гидрировании на никеле Ренея. Гидрирование бензольного кольца протекает быстро и на первых стадиях его нельзя остановить.
В отличие от производных бензола, гидрирование конденсированных ароматических соединений протекает гораздо быстрее. Реакции последовательного гидрирования нафталина показаны на рисунке ниже.
Сложно разобраться самому?
Попробуй обратиться за помощью к преподавателям
Восстановление алюмогидридом лития. Алюмогидрид лития как правило используется в химии в виде раствора или суспензии в абсолютном эфире. Имеем дело с активным восстановителем. 1 моль этого неорганического соединения способен восстановить 4 моля альдегида.
Реакция восстановления хинонов к аренам показана ниже.
Сложные эфиры кислот поддаются восстановлению к альдегидам только при наличии алюмогидрида лития и соблюдение особого температурного режима.
Восстановление боргидридом натрия. Методика восстановления карбонильного соединения будет актуальна только при условии, что нам известно количество боргидрида. Восстановление боргидридом натрия протекает быстрее чем реакции восстановления гидразинов.
http://helpiks.org/6-85905.html
http://spravochnikvs.com/kataliticheskoe_gidrirovanie_arenov