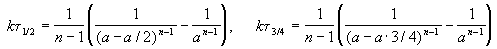Кинетическое уравнение реакции 2 го порядка
1. Основные понятия и постулаты химической кинетики
Химическая кинетика — раздел физической химии, изучающий скорости химических реакций. Основные задачи химической кинетики: 1) расчет скоростей реакций и определение кинетических кривых, т.е. зависимости концентраций реагирующих веществ от времени (прямая задача); 2) определение механизмов реакций по кинетическим кривым (обратная задача).
Скорость химической реакции описывает изменение концентраций реагирующих веществ в единицу времени. Для реакции
aA + bB + . 
скорость реакции определяется следующим образом:
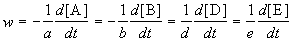
где квадратные скобки обозначают концентрацию вещества (обычно измеряется в моль/л), t — время; a, b, d, e — стехиометрические коэффициенты в уравнении реакции.
Скорость реакции зависит от природы реагирующих веществ, их концентрации, температуры и наличия катализатора. Зависимость скорости реакции от концентрации описывается основным постулатом химической кинетики — законом действующих масс:
Скорость химической реакции в каждый момент времени пропорциональна текущим концентрациям реагирующих веществ, возведенным в некоторые степени:
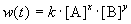
где k — константа скорости (не зависящая от концентрации); x, y — некоторые числа, которые называют порядком реакции по веществам A и B, соответственно. Эти числа в общем случае никак не связаны с коэффициентами a и b в уравнении реакции. Сумма показателей степеней x + y называется общим порядком реакции. Порядок реакции может быть положительным или отрицательным, целым или дробным.
Большинство химических реакций состоит из нескольких стадий, называемых элементарными реакциями. Под элементарной реакцией обычно понимают единичный акт образования или разрыва химической связи, протекающий через образование переходного комплекса. Число частиц, участвующих в элементарной реакции, называют молекулярностью реакции. Элементарные реакции бывают только трех типов: мономолекулярные (A 


ПРИМЕРЫ
Пример 1-1. Скорость образования NO в реакции 2NOBr(г) 
Решение. По определению, скорость реакции равна:
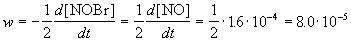
Из этого же определения следует, что скорость расходования NOBr равна скорости образования NO с обратным знаком:
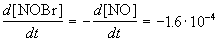
Пример 1-2. В реакции 2-го порядка A + B 
Решение. По закону действующих масс, в любой момент времени скорость реакции равна:
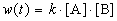
К моменту времени, когда [A] = 1.5 моль/л, прореагировало по 0.5 моль/л веществ A и B, поэтому [B] = 3 – 0.5 = 2.5 моль/л. Константа скорости равна:
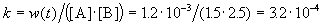
К моменту времени, когда [B] = 1.5 моль/л, прореагировало по 1.5 моль/л веществ A и B, поэтому [A] = 2 – 1.5 = 0.5 моль/л. Скорость реакции равна:
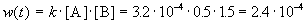
ЗАДАЧИ
1-1. Как выражается скорость реакции синтеза аммиака 1/2 N2 + 3/2 H2 = NH3 через концентрации азота и водорода? (ответ)
1-2. Как изменится скорость реакции синтеза аммиака 1/2 N2 + 3/2 H2 = NH3, если уравнение реакции записать в виде N2 + 3H2 = 2NH3? (ответ)
1-3. Чему равен порядок элементарных реакций: а) Сl + H2 = HCl + H; б) 2NO + Cl2 = 2NOCl? (ответ)
1-4. Какие из перечисленных величин могут принимать а) отрицательные; б) дробные значения: скорость реакции, порядок реакции, молекулярность реакции, константа скорости, стехиометрический коэффициент? (ответ)
1-5. Зависит ли скорость реакции от концентрации продуктов реакции? (ответ)
1-6. Во сколько раз увеличится скорость газофазной элементарной реакции A = 2D при увеличении давления в 3 раза?(ответ)
1-7. Определите порядок реакции, если константа скорости имеет размерность л 2 /(моль 2 . с). (ответ)
1-8. Константа скорости газовой реакции 2-го порядка при 25 о С равна 10 3 л/(моль . с). Чему равна эта константа, если кинетическое уравнение выражено через давление в атмосферах?(ответ)
1-9. Для газофазной реакции n-го порядка nA 
1-10. Константы скорости прямой и обратной реакции равны 2.2 и 3.8 л/(моль . с). По какому из перечисленных ниже механизмов могут протекать эти реакции: а) A + B = D; б) A + B = 2D; в) A = B + D; г) 2A = B.(ответ)
1-11. Реакция разложения 2HI 
1-12. Скорость реакции 2-го порядка A + B 
1-13. В реакции 2-го порядка A + B 
1-14. В реакции 2-го порядка A + B 
1-15. Скорость газофазной реакции описывается уравнением w = k . [A] 2 . [B]. При каком соотношении между концентрациями А и В начальная скорость реакции будет максимальна при фиксированном суммарном давлении? (ответ)
2. Кинетика простых реакций
В данном разделе мы составим на основе закона действующих масс и решим кинетические уравнения для необратимых реакций целого порядка.
Реакции 0-го порядка. Скорость этих реакций не зависит от концентрации:
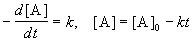
где [A] — концентрация исходного вещества. Нулевой порядок встречается в гетерогенных и фотохимических реакциях.
Реакции 1-го порядка. В реакциях типа A 
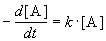
При решении кинетических уравнений часто используют следующие обозначения: начальная концентрация [A]0 = a, текущая концентрация [A] = a — x(t), где x(t) — концентрация прореагировавшего вещества A. В этих обозначениях кинетическое уравнение для реакции 1-го порядка и его решение имеют вид:
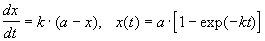
Решение кинетического уравнения записывают и в другом виде, удобном для анализа порядка реакции:
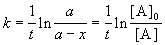
Время, за которое распадается половина вещества A, называют периодом полураспада t 1/2. Он определяется уравнением x(t 1/2) = a/2 и равен
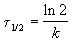
Реакции 2-го порядка. В реакциях типа A + B 
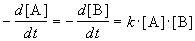
При решении этого уравнения различают два случая.
1) одинаковые начальные концентрации веществ A и B: a = b. Кинетическое уравнение имеет вид:
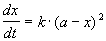
Решение этого уравнения записывают в различных формах:
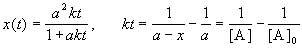
Период полураспада веществ A и B одинаков и равен:
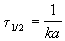
2) Начальные концентрации веществ A и B различны: a 
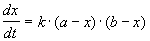
Решение этого уравнения можно записать следующим образом:
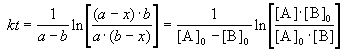
Периоды полураспада веществ A и B различны: 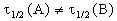
Реакции n-го порядка nA 
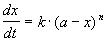
Решение кинетического уравнения:
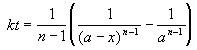
Период полураспада вещества A обратно пропорционален (n-1)-й степени начальной концентрации:
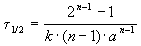
Пример 2-1. Период полураспада радиоактивного изотопа 14 C — 5730 лет. При археологических раскопках было найдено дерево, содержание 14 C в котором составляет 72% от нормального. Каков возраст дерева?
Решение. Радиоактивный распад — реакция 1-го порядка. Константа скорости равна:
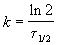
Время жизни дерева можно найти из решения кинетического уравнения с учетом того, что [A] = 0.72 . [A]0:
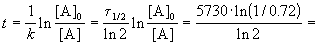
Пример 2-2. Установлено, что реакция 2-го порядка (один реагент) завершается на 75% за 92 мин при исходной концентрации реагента 0.24 М. Какое время потребуется, чтобы при тех же условиях концентрация реагента достигла 0.16 М?
Решение. Запишем два раза решение кинетического уравнения для реакции 2-го порядка с одним реагентом:
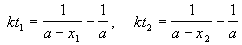
где, по условию, a = 0.24 M, t1 = 92 мин, x1 = 0.75 . 0.24 = 0.18 M, x2 = 0.24 — 0.16 = 0.08 M. Поделим одно уравнение на другое:
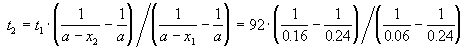
Пример 2-3. Для элементарной реакции nA 
и поделим одно выражение на другое. Постоянные величины k и a из обоих выражений сократятся, и мы получим:
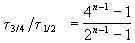
Этот результат можно обобщить, доказав, что отношение времен, за которые степень превращения составит a и b , зависит только от порядка реакции:
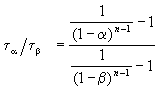
ЗАДАЧИ
2-1. Пользуясь решением кинетического уравнения, докажите, что для реакций 1-го порядка время t x, за которое степень превращения исходного вещества достигает x, не зависит от начальной концентрации. (ответ)
2-2. Реакция первого порядка протекает на 30% за 7 мин. Через какое время реакция завершится на 99%? (ответ)
2-3. Период полураспада радиоактивного изотопа 137 Cs, который попал в атмосферу в результате Чернобыльской аварии, — 29.7 лет. Через какое время количество этого изотопа составит менее 1% от исходного? (ответ)
2-4. Период полураспада радиоактивного изотопа 90 Sr, который попадает в атмосферу при ядерных испытаниях, — 28.1 лет. Предположим, что организм новорожденного ребенка поглотил 1.00 мг этого изотопа. Сколько стронция останется в организме через а) 18 лет, б) 70 лет, если считать, что он не выводится из организма?(ответ)
2-5. Константа скорости для реакции первого порядка SO2Cl2 = SO2 + Cl2 равна 2.2 . 10 -5 с -1 при 320 о С. Какой процент SO2Cl2 разложится при выдерживании его в течение 2 ч при этой температуре?(ответ)
2-6. Константа скорости реакции 1-го порядка
2N2O5(г) 
при 25 о С равна 3.38 . 10 -5 с -1 . Чему равен период полураспада N2O5? Чему будет равно давление в системе через а) 10 с, б) 10 мин, если начальное давление было равно 500 мм рт. ст. (ответ)
2-7. Реакцию первого порядка проводят с различными количествами исходного вещества. Пересекутся ли в одной точке на оси абсцисс касательные к начальным участкам кинетических кривых? Ответ поясните.(ответ)
2-8. Реакция первого порядка A 
2-9. Реакция второго порядка 2A 
2-10. Вещество A смешали с веществами B и C в равных концентрациях 1 моль/л. Через 1000 с осталось 50% вещества А. Сколько вещества А останется через 2000 с, если реакция имеет: а) нулевой, б) первый, в) второй, в) третий общий порядок?(ответ)
2-11. Какая из реакций — первого, второго или третьего порядка — закончится быстрее, если начальные концентрации веществ равны 1 моль/л и все константы скорости, выраженные через моль/л и с, равны 1? (ответ)
CH3CH2NO2 + OH — 
имеет второй порядок и константу скорости k = 39.1 л/(моль . мин) при 0 о С. Был приготовлен раствор, содержащий 0.004 М нитроэтана и 0.005 М NaOH. Через какое время прореагирует 90% нитроэтана? (ответ)
2-13. Константа скорости рекомбинации ионов H + и ФГ — (фенилглиоксинат) в молекулу НФГ при 298 К равна k = 10 11.59 л/(моль . с). Рассчитайте время, в течение которого реакция прошла на 99.999%, если исходные концентрации обоих ионов равны 0.001 моль/л. (ответ)
2-14. Скорость окисления бутанола-1 хлорноватистой кислотой не зависит от концентрации спирта и пропорциональна [HClO] 2 . За какое время реакция окисления при 298 К пройдет на 90%, если исходный раствор содержал 0.1 моль/л HClO и 1 моль/л спирта? Константа скорости реакции равна k = 24 л/(моль . мин). (ответ)
2-15. При определенной температуре 0.01 М раствор этилацетата омыляется 0.002 М раствором NaOH на 10% за 23 мин. Через сколько минут он будет омылен до такой же степени 0.005 М раствором KOH? Считайте, что данная реакция имеет второй порядок, а щелочи диссоциированы полностью.(ответ)
2-16. Реакция второго порядка A + B 
*2-17. Скорость автокаталитической реакции A 
*2-18. Автокаталитическая реакция A 
*2-19. Автокаталитическая реакция A 


Сервер создается при поддержке Российского фонда фундаментальных исследований
Не разрешается копирование материалов и размещение на других Web-сайтах
Вебдизайн: Copyright (C) И. Миняйлова и В. Миняйлов
Copyright (C) Химический факультет МГУ
Написать письмо редактору
Кинетика односторонних химических реакций второго порядка
Случай 1. Когда в элементарном акте реагируют две одинаковые частицы или когда концентрации исходных веществ А1 и А2 равны:
2А ®продукты или А1+А2 ®продукты.
Запишем выражение для скорости:
1) по закону действующих масс: v = k¢×C 2 ;
2) из определения скорости реакции: v = 
При выводе уравнения константы скорости химической реакции, приравняем полученные выражения, разделим переменные и проинтегрируем, учитывая что 
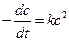
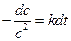
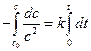
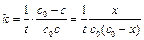
Размерность константы скорости реакции второго порядка – «время -1 ×концентрация -1 ». Например: л/(моль×с).
Зависимость концентрации от времени выражается уравнением
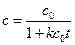
Кинетическое уравнение для реакции второго порядка, согласно уравнению (1.19) имеет вид:
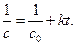
Откуда следует, что график в координатах 
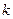
Период полупревращения для реакции второго порядка равен:
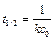
Как видно из этого уравнения, период полупревращения для реакции второго порядка обратно пропорционален начальной концентрации реагента.
Случай 2. Концентрации исходных веществ разные:
Пусть начальные и текущие концентрации веществ 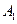
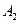

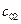
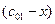
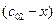

Запишем выражение для скорости:
1) по закону действующих масс
2) из определения скорости реакции
v = 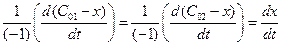
Для нахождения константы скорости химической реакции прировняем уравнения (4.37 и 4.38) друг другу, разделим переменные и проинтегрируем:

Как видно из уравнения (4.39), размерность константы скорости реакции второго порядка – «время -1 ×концентрация -1 ».
Дата добавления: 2016-01-09 ; просмотров: 1224 ; ЗАКАЗАТЬ НАПИСАНИЕ РАБОТЫ
Кинетические уравнения 1-, 2- и 0-го порядка
ТЕОРЕТИЧЕСКИЕ ОСНОВЫ РАБОТЫ
Скорость химической реакции определяется как изменение концентрации одного из реагирующих веществ или продуктов реакции в единицу времени. Среднюю скорость реакции в промежутке времени от t1 до t2 рассчитывают следующим образом:

где с1 и с2 – концентрация вещества в моменты времени t1 и t2 соответственно.
Знак плюс берется при расчете скорости по продукту реакции, в ходе реакции концентрация продукта возрастает, с2 > с1, Dс>0. Знак минус берется при расчете скорости по одному из исходных реагентов, концентрация его при протекании реакции убывает, с2 3 либо в моль/дм 3 (моль/л), время – в секундах, минутах, часах.
Скорость химической реакции зависит от природы реагирующих веществ, концентрации, температуры и присутствия в системе катализатора.
Для всякой химической реакции зависимость скорости реакции от концентраций реагирующих веществ выражается законом действующих масс: скорость химической реакции прямо пропорциональна произведению концентраций реагирующих веществ в соответствующих степенях

где ci – концентрация i-го реагента. Показатель степени при концентрации называется порядком реакции по i-му веществу. Сумма показателей степеней при концентрациях в законе действия равна суммарному порядку реакции. Для простых реакций показатель степени совпадает со стехиометрическим коэффициентом в уравнении реакции. Коэффициент пропорциональности k в законе действующих масс называется константой скорости. Величина k численно равна скорости химической реакции при концентрациях реагирующих веществ, равных единице. Константа скорости химической реакции является характеристикой каждой конкретной реакции, зависит от температуры и не зависит от концентраций.
Уравнения, связывающие скорость химической реакции с концентрациями, а также выражающие зависимость концентраций от времени, называются кинетическими уравнениями (см. таблицу 1).
Таблица 1
Кинетические уравнения 1-, 2- и 0-го порядка
| Порядок реакции | Выражение закона действующих масс | Единица измерения константы скорости | Кинетическое уравнение | Зависимость периода полураспад от начальной концентрации |
 | с -1 |  |  | |
 | л×моль -1 ×с -1 |  | 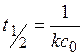 | |
 | моль×л -1 ×с -1 |  |  |
Для определения численного значения константы скорости необходимо тем или иным методом определить концентрацию реагирующего вещества в различные моменты времени и подставить эти значения в выражение для константы скорости (см. таблицу). Константу скорости можно также найти графически.
Изучаемая в данной работе реакция окисления иодид-ионов пероксидом водорода в водном растворе в кислой среде протекает по уравнению:
Механизм реакции сложный, включает несколько стадий. В целом в реакции участвуют три вида частиц, и в реакционной смеси могут изменяться концентрации всех этих частиц, влияя на скорость реакции. При избытке кислоты (ионов H + ) концентрация [H + ] может считаться постоянной. Концентрацию иодид-ионов [I – ] можно поддерживать постоянной. Для этого в ходе опыта к реакционной смеси периодически добавляют одинаковые количества тиосульфата натрия Na2S2O3. Тиосульфат реагирует с выделяющимся при реакции (1) иодом по уравнению
Таким образом, пероксид водорода расходуется в реакции, а концентрация иодид-ионов остается практически постоянной. Кинетическое уравнение реакции окисления v = k [H + ][I – ] n [H2O2] = kэксп [H2O2], где kэксп = k [H + ][I – ] n есть величина постоянная при соблюдении вышеуказанных условий, n – порядок реакции по I – . kэксп – экспериментально наблюдаемая константа скорости реакции первого порядка по пероксиду водорода.
Определить константу скорости реакции окисления иодид-ионов пероксидом водорода в кислой среде.
Ø раствор KI, 0,4 %-ный
Ø раствор крахмала 0,5 %-ный (индикатор)
Ø раствор молибдата аммония (NH4)2MoO4 (катализатор)
Ø Коническая колба на 250 мл
Ø Пипетки на 100 мл, 10 мл, 5 мл
Ø Бюретка 25 мл
1. В коническую колбу наливают мерной колбой 100 мл раствора KI и пипеткой 5 мл раствора H2SO4.
2. Бюретку заполняют раствором тиосульфата натрия. В течение опыта раствор тиосульфата в бюретку не добавляют!
3. В колбу с подкисленным раствором иодида из бюретки добавляют точно 1 мл раствора тиосульфата. Приливают 5 капель раствора крахмала.
4. В эту же колбу наливают пипеткой 10 мл пероксида водорода, тщательно перемешивают и ставят под бюретку с тиосульфатом.
5. В момент окрашивания реакционной смеси в синий цвет включают секундомер. Немедленно добавляют еще 1 мл тиосульфата и перемешивают, окраска раствора исчезает.
6. Отмечают момент следующего окрашивания раствора (секундомер не выключают!), сразу добавляют следующий мл раствора тиосульфата. Записывают время появления окрашивания по секундомеру.
7. Продолжают наблюдение, производят 6-7 таких отсчетов по секундомеру, соответствующих окрашиванию реакционной смеси, каждый раз приливая по 1 мл раствора тиосульфата.
Затем добавляют 3-5 капель раствора молибдата аммония в качестве катализатора. Реакция проходит до конца, т.е. весь пероксид водорода вступает в нее. Выделившийся при этом иод оттитровывают тиосульфатом до исчезновения окраски. Записывают окончательный (общий) объем тиосульфата V0. Общее количество Na2S2O3 эквивалентно начальному количеству H2O2.
По ходу опыта результаты измерений заносят в таблицу 2.
Условия проведения опыта: t = °C.
| Объем раствора Vt Na2S2O3, вступившего в реакцию к моменту времени t, мл | Момент появления окраски, t |  |
| По секундомеру | Перевод в секунды | |
| V0 |
Обработка результатов.
1. Рассчитывают константу скорости изучаемой реакции по формуле, приводят три значащих цифры.
2. Рассчитывают среднее значение К по данным таблицы и указывают его в выводе.
3. Строят график зависимости ln(V0-Vt) от времени и определяют по нему значение константы скорости. Указывают значение К в выводе.
Контрольные вопросы и задания.
1. Дайте определения следующим понятиям: химическая кинетика, скорость реакции, средняя и истинная скорость, порядок, молекулярность реакции. В каких единицах может измеряться скорость химической реакции?
2. Какие факторы влияют на скорость химической реакции, на значение константы скорости химической реакции?
3. Сформулируйте закон действия масс. Запишите его математическое выражение. Что называется общим порядком реакции, порядком реакции по веществу?
4. Запишите кинетическое уравнение реакции нулевого, первого, второго порядков. Как экспериментально можно определить константу скорости реакции первого порядка?
5. Что называется временем полупревращения (периодом полураспада)?
6. Какие уравнения описывают зависимость скорости реакции от температуры?
7. Дайте понятие энергии активации реакции.
8. Приведите химизм процесса, протекающего в данном опыте.
9. Какого порядка эта реакция и как это определить?
10. Взаимодействие оксида углерода (II) с хлором выражается уравнением:
концентрация оксида углерода (II) равно 0,3 моль/л, а хлора – 0,2 моль/л. как изменится скорость прямой реакции, если увеличить концентрацию оксида углерода (II) до 1,2 моль/л, а концентрацию хлора до 0,6 моль/л? считать, что это реакция второго порядка.
11. При помощи правила Вант-Гоффа вычислите, при какой температуре реакция закончится через 28 мин, если при 20 о С на это требуется 1,5 ч. температурный коэффициент скорости равен 2,5.
12. Для реакции C12H22O11 + H2O ↔ C6H12O6 + C6H12O6 константа скорости при температуре 298,2 к равна 0,765 л/(моль. мин), а при температуре 328,2 к — 35,5 л/(моль. мин). найдите энергию активации этой реакции и константу скорости при температуре 304,5 К.
13. Константа скорости рекомбинации ионов H + и ФГ — (фенилглиоксинат) в молекулу нфг при 298 К равна K = 1011.59 л/(моль. с). рассчитайте время, в течение которого реакция прошла на 70%, если исходные концентрации обоих ионов равны 0.001 моль/л.
http://helpiks.org/6-47008.html
http://allrefrs.ru/5-28618.html