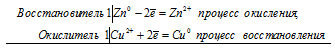metaldetector.com.ua
Часть I. Коррозия
Разрушения, вызванные коррозией металла, в технике напрямую связаны с потерей функциональности той или иной части устройства или всей системы. Помимо этого, во многих случаях коррозия приводит к ухудшению эстетических качеств объекта. Если говорить об исторических памятниках, то разрушения, вызванные коррозией, приводят главным образом к потере информации, поскольку важным носителем информации у находки является ее оригинальная поверхность. Для того чтобы выбрать метод расчистки и уменьшить риск потери этой оригинальной поверхности, а также приостановить дальнейшую коррозию находки, необходимо знать и понимать те процессы, которые происходят в металле.
В природе серебро редко встречается в чистом виде. Для получения металла из руды необходимо использовать определенные химические процессы. Будучи благородным металлом, серебро отличается относительно низкой реакционной способностью, но, находясь в неблагоприятных условиях, этот металл всегда стремится принять свою первичную форму: серебро корродирует.
Атмосферная коррозия
Природные серебряные руды часто содержат серу (аргентит, прустит, аргентоярозит); это свидетельствует, что серебро легко вступает с ней в реакцию. Так, на воздухе серебро образует очень тонкую невидимую пленку оксида. Но в связи с тем, что в воздухе, кроме кислорода и азота, почти всегда содержатся соединения серы (влияние индустрии, извержений вулканов и т. д.), светлая поверхность предмета преобразуется в темные (от светло-серого до черного) соединения. В комнатных условиях сульфидная патина образуется достаточно медленно и в какой-то степени пассивизирует поверхность металла. Но при высокой влажности этот процесс может развиваться очень быстро и приводить к образованию рыхлой патины, содержащей сульфиды.
Помимо того, что соединения серы находятся в воздухе, они также присутствуют во многих материалах, таких как бумага, картон, ткань, резина. В связи с этим предмет, начищенный до блеска и не покрытый защитным слоем, может со временем потемнеть, соприкасаясь с такими материалами или находясь с ними рядом.
Кроме соединений серы, на сохранность объекта сильно влияет хлор. Он содержится в воздухе, в водопроводной воде, в некоторых полимерных альбомах для монет, а также в человеческом поте.
Практически всегда предметы состоят не из чистого серебра, а из его сплава. Коррозия в этом случае протекает немного по-другому. Компоненты сплава оказывают большое влияние на сохранность предмета. Иногда они продлевают жизнь предмета, а в некоторых случаях могут значительно ее сократить. В сплаве разрушается, как правило, более «слабый» металл. Например, если в сплаве присутствует медь, то она реагирует первой.
Почвенная коррозия
Коррозионные процессы, происходящие в почве, значительно отличаются от атмосферной коррозии. В этом случае огромную роль играют такие факторы, как состав почвы, ее плотность, кислотность, влажность, наличие кислорода и других газов, а также состав сплава и техника изготовления самого объекта.
Существует множество видов коррозии. Описывать их все не имеет смысла, к тому же некоторые процессы еще не совсем понятны для науки. Но мне бы хотелось рассказать о некоторых важных и интересных, на мой взгляд, аспектах этой проблемы.
Интеркристаллическая коррозия
Серебро со временем становится хрупким вследствие интеркристаллической коррозией. Многие наверняка замечали, что поверхность корродированного предмета из серебра состоит как бы из маленьких крупинок. Это кристаллы сплава, образовавшиеся при остывании расплавленной массы. А так как температура плавления у различных компонентов разная, то и кристаллизация компонентов в сплаве происходит на разных стадиях охлаждения. Например, температура плавления серебра –963ºС, а меди –1083ºС. Упрощенно это можно представить так: при понижении температуры на поверхности каждой крупинки сначала застывает и концентрируется медь, а серебро застывает позже и концентрируется внутри самой крупинки. На самом деле процессы кристаллизации намного сложнее и зависят от множества факторов, но смысл остается тем же. Границы крупинок обогащены менее благородными металлами и примесями. Интеркристаллическая коррозия протекает именно по границам этих крупинок, в результате чего теряется связь между ними. Такая коррозия может заходить очень глубоко, и на первый взгляд она не видна. Порою весь предмет выглядит стабильно, блестит, но на самом деле вся структура металла нарушена. Крупинки металла связаны друг с другом тонкой невидимой пленкой, состоящей из продуктов коррозии. Опуская такой предмет в какой-либо чистящий раствор, мы значительно нарушаем эту связь кристаллов. В особенности пагубно на межкристаллической связи сказывается раствор аммиака или сода с аммиаком.
Контактная коррозия
Несколько слов следует сказать о контактной коррозии. Она возникает, если два различных металла соприкасаются друг с другом. Этот процесс хорошо заметен на бронзовых находках, имеющих серебрение. Так, выкапывая из земли медную ложку или какой-либо другой посеребренный предмет, мы часто видим, что поверхность серебра блестит и не имеет видимых следов коррозии. Но находящаяся под серебром медь или бронза частично корродирована. Продукты коррозии местами приподняли пленку серебра или полностью ее разрушили. Разрушение серебра в этом случае происходит механически и вызвано увеличенным объемом продуктов коррозии меди по сравнению с первоначальным металлом. Часто эти продукты покрывают всю поверхность серебрения и находятся как под ним, так и над ним. К расчистке таких предметов нужно подходить очень осторожно. Погружать такую находку в чистящий раствор не рекомендуется, а ее механическая расчистка без предварительного закрепления связана с риском потери серебрения.
Транскристаллическая коррозия
Еще один частый вид разрушений – так называемая транскристаллическая коррозия. Наблюдается она, как правило, у кованых и штампованных объектов (монет, колец, фибул и т. п.), а также у литых предметов, если отливка происходила неравномерно. Коррозия протекает сначала по самым «слабым» местам структуры металла. Так, при штамповке монеты, если материал недостаточно пластичен, в кристаллической решетке металла происходит сдвиг. В том месте, где он произошел, структура металла нарушается. Именно здесь и будет быстрее всего развиваться транскристаллическая коррозия. В таких случаях можно наблюдать отслаивание металла. Начинается оно с маленькой микротрещинки или с маленького, невидимого невооруженным глазом очага поверхностной коррозии. Когда этот очаг доходит до внутренних границ слоев, коррозия меняет свое направление и начинает протекать по плоскости сдвига. В таких местах наблюдаются сначала вздутия, а затем расслаивание поверхности. При расчистке подобных очагов нельзя сильно нажимать на них шабером или тереть их кисточками и щетками. Перед расчисткой такие места желательно закрепить. Еле заметный бугорок с оригинальной поверхностью всегда лучше, чем большой «кратер».
При штамповке или ковке металла образуются невидимые глазом трещины. Что-то подобное можно наблюдать и при плохой отливке. Если расплавленный металл при литье чуть-чуть остыл, хотя и не затвердел, то следующая порция расплавленного сырья уже не может смешаться с начальной. В результате между ними образуются границы, тоже своего рода трещины. Образовавшиеся в них темные продукты коррозии хорошо заметны, но, хотя они и портят внешний вид предмета, не старайтесь избавиться от них полностью, так как они могут уходить глубоко внутрь предмета.
Электрохимическая коррозия
Часто в сплаве серебра присутствует медь, в результате чего на поверхности находки можно наблюдать зеленые продукты коррозии. Если содержание меди в сплаве очень высоко, то вся поверхность объекта может быть покрыта зеленой коркой. Иногда из-за таких отложений даже не удается сразу определить металл, из которого изготовлен предмет. Сплавы, в особенности старые сплавы, далеко не гомогенны. Частицы металлов здесь чаще всего плохо перемешаны между собой и располагаются друг напротив друга. Иногда разнородные частицы группируются на различных участках предмета. В результате этого образуется своеобразный «гальванический элемент» и более «слабый» металл начинает разрушаться.
Сульфидная патина
В относительно редких случаях на поверхности предмета из серебра присутствует ровная темная сульфидная патина. Цвет ее варьирует от светло-серого до темного, почти черного. Но, хотя сульфидов в почве обычно более чем достаточно, такая патина образуется редко. Сернистое серебро плохо растворимо в Трилоне-Б и других комплексообразователях, а также в аммиаке. Иногда его ошибочно принимают за роговое серебро или налет, образовавший в результате воздействия высокой температуры. Но это не так. Темную ровную сульфидную патину ни в коем случае нельзя удалять: она в точности передает все детали предмета. Если ее удалить, то полностью теряются оригинальная поверхность и ее детали и открывается внутренняя зернистая структура металла.
Роговое серебро
Роговое серебро часто присутствует на археологических предметах. Водный раствор, содержащий хлориды, при доступе воздуха начинает воздействовать на серебро. В результате образуется хлорид серебра AgCl, так называемое роговое серебро – мягкое, аморфное вещество от светло-желтого до серо-свинцового цвета. Как правило, оно присутствует в паре с полухлористым серебром (Ag2Cl), которое немного тверже рогового серебра. Такая коррозия может преобразовать все металлическое ядро, и, если она зашла слишком глубоко, ее ни в коем случае нельзя полностью удалять.
Чрезвычайно редко на предмете встречается лишь один вид коррозии. Как правило, различные виды сочетаются друг с другом, что негативно сказывается на сохранности оригинальной поверхности и металла в целом. Умение различать виды коррозии необходимо не только для правильной оценки состояния металла и выбора наиболее подходящего метода его консервации (расчистки, закрепления), но и для определения начавшихся изменений и их возможной опасности при дальнейшем хранении предметов.
Процессы коррозии различных металлов. Интенсивность коррозии
Решение задач по химии на коррозию металлов
Задание 296
Цинковую и железную пластинки опустили в раствор сульфата меди. Составьте электронные и ионно-молекулярные уравнения реакций, происходящих на каждой из этих пластинок. Какие процессы будут проходить на пластинках, если наружные концы их соединить проводником?
Решение:
Если цинковую или медную пластинки опустить в раствор сульфата меди, то в обоих случаях будет наблюдаться выпадение осадка меди. Происходит вытеснение меди цинком и железом, потому что стандартные электродные потенциалы цинка (-0,763 В) и железа (-0,44 В) значительно электроотрицательнее, чем потенциал меди (+0,34 В). Поэтому цинк и железо будут окисляться, а ионы меди Cu 2+ — восстанавливаться до металлической меди:
а) Электрохимические процессы при реакции цинка и сульфата меди
Zn 0 + Сu 2+ = Zn 2+ + Cu 0
б) Электрохимические процессы при реакции железа и сульфата меди
Fe 0 + Сu 2+ = Fe 2+ + Cu 0
Если соединить цинковую и железную пластинки, опущенные в раствор сульфата меди (II) проводником, то будет наблюдаться растворение цинковой пластинки и осаждение меди на железной пластинке. Объясняется это тем, что цинк имеет более электроотрицательный стандартный электродный потенциал, чем железо, поэтому цинк будет окисляться. На железной пластинке будут восстанавливаться ионы меди, так как стандартный электродный потенциал меди имеет большее численное значение, чем потенциал железа.
Анодный процесс: Zn 0 -2 
Катодный процесс: Cu 2+ + 2 
Задание 297
Как влияет рН среды на скорость коррозии железа и цинка? Почему? Составьте электронные уравнения анодного и катодного процессов атмосферной коррозии этих металлов.
Решение:
Стандартные электродные потенциалы железа и цинка равны соответственно -0,44 В и -0,763 В. Потенциал, отвечающий электродному процесс:
2Н + + 2 
В нейтральной среде, равен приблизительно -0,41 В. Следовательно, ионы водорода, находящиеся в воде и в нейтральных водных средах, могут окислять только те металлы, потенциал которых меньше, чем -0,41 В, — это могут быть железо и цинк. Однако, эти металлы в нейтральных растворах, содержащих растворённый кислород, образуют защитную оксидную плёнку, препятствующую дальнейшему разрушению металла. Поэтому железо и цинк не могут быть окислены ионами водорода в нейтральных средах. Атмосферная коррозия – коррозия во влажном воздухе при комнатной температуре. Поверхность металла, находящегося во влажном воздухе, бывает покрыта плёнкой воды, содержащей различные газы, и в первую очередь – кислород. Скорость атмосферной коррозии зависит от рН среды. При понижении рН среды концентрация ионов водорода Н+ возрастает, что приводит к увеличению скорости коррозии металла, увеличивается восстановительный процесс на аноде:
2Н + + 2 
При повышении рН раствора уменьшается концентрация ионов водорода Н + и, соответственно, увеличивается концентрация ионов ОН-, что, согласно принципу Ле Шателье, смещает равновесие в системах: 2Н + + 2 

Электрохимические процессы, протекающие при контакте железа и цинка при контакте с водой с поглощением кислорода (атмосферная коррозия):
Анод: Zn 0 -2 
Катод: 1/2O2 + H2O + 2 
Анод: Zn 0 -2 
Катод: 1/2O2 + H2O + 2 
Задание 298
В раствор электролита, содержащего растворенный кислород, опустили цинковую пластинку и цинковую пластинку, частично покрытую медью. В каком случае процесс коррозии цинка проходит интенсивнее? Составьте электронные уравнения анодного и катодного процессов.
Решение:
а) Если цинковую пластинку опустить в раствор электролита, содержащего растворенный кислород, то будет наблюдаться коррозия цинка, характеризующаяся окислением его до ионов Zn 2+ :
Zn 0 -2 
Чрез некоторое время скорость реакции заметно замедляется, потому что чистый цинк окисляется кислородом, растворённым в воде, с образованием оксидной плёнки, которая, покрывая пластинку тонким слоем, пассивирует её. При этом протекает реакция:
Zn + 1/2 O2 = Zn 0
б) Если в раствор электролита опустить цинковую пластинку частично покрытую медью, процесс коррозии будет происходить значительно интенсивнее, так как образуется гальваническая пара Zn — Cu. Цинк имеет более электроотрицательный электродный потенциал (-0,763 В), чем медь (0,34 В), поэтому цинк является анодом, а медь – катодом.
Анодный процесс: Zn 0 -2 
Катодный процесс: в кислой среде: 2Н + + 2 

В нейтральной среде или в щелочной ионы цинка Zn 2+ с гидроксид-ионами ОН- образуют нерастворимое основание, то продуктом коррозии будет Zn(OH)2. В кислой среде ионы цинка Zn 2+ с ионами кислотного остатка будут образовывать соль и при этом выделяется газообразный водород. Происходит интенсивное разрушение цинковой пластинки частично покрытой медью.
Коррозия серебра на воздухе уравнение
8.2 ЭЛЕКТРОХИМИЧЕСКАЯ КОРРОЗИЯ
Причиной электрохимической коррозии * является возникновение на поверхности металла короткозамкнутых гальванических элементов *.
В тонком слое влаги, обычно покрывающем металл, растворяются кислород, углекислый, сернистый и другие газы, присутствующие в атмосферном воздухе. Это создает условия соприкосновения металла с электролитом *. Различные участки поверхности любого металла обладают разными потенциалами. Причинами этого могут быть наличие примесей в металле, различная обработка отдельных его участков, неодинаковые условия (окружающая среда), в которых находятся различные участки поверхности металла. При этом участки поверхности металла с более электроотрицательным потенциалом становятся анодами и растворяются.
Электрохимическая коррозия может развиваться в результате контакта различных металлов. В этом случае будет возникать не микр о- , а макрогальванопара , и коррозия называется контактной (см. детальную классификацию видов коррозии). Сочетания металлов, сильно отличающихся значениями электродных потенциалов *, в технике недопустимы (например, алюминий – медь). В случае коррозии, возникающей при контакте какого-либо металла со сплавом, последний имеет потенциал, соответствующий наиболее активному металлу, входящему в состав сплава. Например, при контакте латуни (сплав цинка и меди) с железом корродировать будет латунь за счет наличия в ней цинка.
Представим схематично работу короткозамкнутого гальванического элемента, возникающего на поверхности металла, подверженного коррозии в электролите * (рисунок 8.1). Анодный участок имеет более электроотрицательный потенциал, поэтому на нем идет процесс окисления металла. Образовавшиеся в процессе окислен ия ио ны переходят в электролит, а часть освободившихся при этом электронов может перемещаться к катодному участку (на рисунке 8.1 показано стрелками). Процесс коррозии будет продолжаться в том случае, если электроны, перешедшие на катодный участок, будут с него удаляться. Иначе произойдет поляризация электродов *, и работа коррозионного гальванического элемента прекратится.
Рисунок 8.1 – Схема электрохимической коррозии. Д – деполяризатор
Процесс отвода электронов с катодных участков называется деполяризацией. Вещества, при участии которых осуществляется деполяризация, называются деполяризаторами. На практике чаще всего приходится встречаться с двумя типами деполяризации: водородной и кислородной. Тип деполяризации (катодный процесс) зависит от реакции среды раствора электролита.
В кислой среде электрохимическая коррозия протекает с водородной деполяризацией. Рассмотрим коррозию железной пластинки с примесями меди во влажной хлористоводородной атмосфере Имеется в виду атмосфера с примесью газообразного HCl. . В этом случае железо будет анодом ( E ° = –0,44В), а медь – катодом ( E ° =+0,34В). На анодном участке будет происходить процесс окисления железа, а на катодном – процесс деполяризац ии ио нами водорода, которые присутствуют в электролите:
А: Fe – 2e → Fe 2+ – окисление
К: 2 H + + 2e → H2 ↑ – восстановление
Схема возникающего короткозамкнутого гальванического элемента выглядит следующим образом:
A (–) Fe | HCl | Cu (+) К
В нейтральной среде коррозия протекает с кислородной деполяризацией, т.е. роль деполяризатора выполняет кислород, растворенный в воде. Этот вид коррозии наиболее широко распространен в природе: он наблюдается при коррозии металлов в воде, почве и в незагрязненной промышленными газами атмосфере. Если коррозии во влажном воздухе подвергается железо с примесями меди, то электродные процессы можно записать в виде:
(А) Fe – 2e → Fe 2+ – окисление
(К) 2 H2O + O2 + 4e → 4 OH – – восстановление
У поверхности металла в электролите протекают следующие реакции:
Fe 2+ + 2 OH – → Fe( OH)2
Основная масса черных металлов разрушается вследствие процесса ржавления, в основе которого лежат вышеуказанные реакции.
Коррозия металла в результате неравномерного доступа кислорода . Случаи электрохимической коррозии, возникающей вследствие неравномерной аэрации кислородом различных участков металла, очень часто встречаются в промышленности и в подземных сооружениях. Примером может служить коррозия стальной сваи, закопанной в речное дно (рис 8.2).
Рисунок 8.2 – Коррозия в результате неравномерного доступа кислорода. Б – техническое сооружение; А – анодный участок; К – катодный участок.
Часть конструкции, находящаяся в воде, омывается растворенным в ней кислородом и, в случае возникновения условий для электрохимической коррозии, будет выполнять роль катода. Другая же часть конструкции, находящаяся в почве, будет анодом и подвергнется разрушению.
http://buzani.ru/zadachi/khimiya-shimanovich/955-korroziya-metallov-zadachi-229
http://www.chem-astu.ru/chair/study/genchem/r8_2.htm