Acetyl
Наведите курсор на ячейку элемента, чтобы получить его краткое описание.
Чтобы получить подробное описание элемента, кликните по его названию.
| H + | Li + | K + | Na + | NH4 + | Ba 2+ | Ca 2+ | Mg 2+ | Sr 2+ | Al 3+ | Cr 3+ | Fe 2+ | Fe 3+ | Ni 2+ | Co 2+ | Mn 2+ | Zn 2+ | Ag + | Hg 2+ | Pb 2+ | Sn 2+ | Cu 2+ | |
| OH — | Р | Р | Р | Р | Р | М | Н | М | Н | Н | Н | Н | Н | Н | Н | Н | — | — | Н | Н | Н | |
| F — | Р | М | Р | Р | Р | М | Н | Н | М | М | Н | Н | Н | Р | Р | Р | Р | Р | — | Н | Р | Р |
| Cl — | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Н | Р | М | Р | Р |
| Br — | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Н | М | М | Р | Р |
| I — | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | ? | Р | ? | Р | Р | Р | Р | Н | Н | Н | М | ? |
| S 2- | М | Р | Р | Р | Р | — | — | — | Н | — | — | Н | — | Н | Н | Н | Н | Н | Н | Н | Н | Н |
| HS — | Р | Р | Р | Р | Р | Р | Р | Р | Р | ? | ? | ? | ? | ? | Н | ? | ? | ? | ? | ? | ? | ? |
| SO3 2- | Р | Р | Р | Р | Р | Н | Н | М | Н | ? | — | Н | ? | Н | Н | ? | М | М | — | Н | ? | ? |
| HSO3 — | Р | ? | Р | Р | Р | Р | Р | Р | Р | ? | ? | ? | ? | ? | ? | ? | ? | ? | ? | ? | ? | ? |
| SO4 2- | Р | Р | Р | Р | Р | Н | М | Р | Н | Р | Р | Р | Р | Р | Р | Р | Р | М | — | Н | Р | Р |
| HSO4 — | Р | Р | Р | Р | Р | Р | Р | Р | — | ? | ? | ? | ? | ? | ? | ? | ? | ? | ? | Н | ? | ? |
| NO3 — | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | — | Р |
| NO2 — | Р | Р | Р | Р | Р | Р | Р | Р | Р | ? | ? | ? | ? | Р | М | ? | ? | М | ? | ? | ? | ? |
| PO4 3- | Р | Н | Р | Р | — | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н |
| CO3 2- | Р | Р | Р | Р | Р | Н | Н | Н | Н | ? | ? | Н | ? | Н | Н | Н | Н | Н | ? | Н | ? | Н |
| CH3COO — | Р | Р | Р | Р | Р | Р | Р | Р | Р | — | Р | Р | — | Р | Р | Р | Р | Р | Р | Р | — | Р |
| SiO3 2- | Н | Н | Р | Р | ? | Н | Н | Н | Н | ? | ? | Н | ? | ? | ? | Н | Н | ? | ? | Н | ? | ? |
| Растворимые (>1%) | Нерастворимые ( Спасибо! Ваша заявка отправлена, преподаватель свяжется с вами в ближайшее время. Вы можете также связаться с преподавателем напрямую: 8(906)72 3-11-5 2 Скопируйте эту ссылку, чтобы разместить результат запроса » » на другом сайте. Изображение вещества/реакции можно сохранить или скопировать, кликнув по нему правой кнопкой мыши. Если вы считаете, что результат запроса » » содержит ошибку, нажмите на кнопку «Отправить». Этим вы поможете сделать сайт лучше. К сожалению, регистрация на сайте пока недоступна. На сайте есть сноски двух типов: Подсказки — помогают вспомнить определения терминов или поясняют информацию, которая может быть сложна для начинающего. Дополнительная информация — такие сноски содержат примечания или уточнения, выходящие за рамки базовой школьной химии, нужны для углубленного изучения. Здесь вы можете выбрать параметры отображения органических соединений. Бромид меди (I)
Бромид меди (I) — неорганическое вещество с формулой CuBr, соединение меди и брома. Относится к классу бинарных соединений, может рассматриваться как соль одновалентной меди и бромоводородной кислоты. В чистом виде — белое кристаллическое вещество, примеси бромида меди (II) окрашивают его в зеленоватый цвет. Содержание
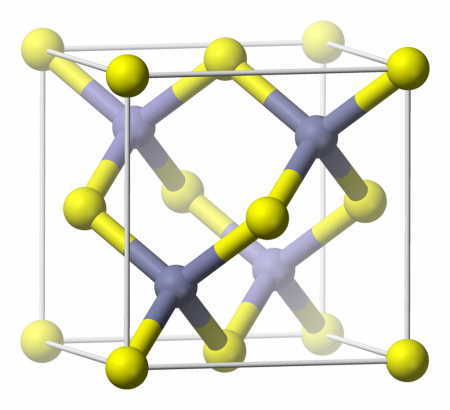
Физические свойстваВ чистом виде представляет собой бесцветные тетраэдрические микрокристаллы. Кристаллическая решётка типа сфалерита (кубическая сингония). Во влажном воздухе на свету медленно окисляется, приобретая зеленоватый цвет. Термически устойчив: плавится и кипит без разложения. Нерастворим в воде, этаноле, эфире. Не образует кристаллогидраты. Химические свойстваОбразование растворимых соединенийБромид меди (I) растворяется в горячей концентрированной серной кислоте: За счёт комплексообразования растворяется в концентрированных растворах бромоводородной кислоты, бромида калия, цианида калия, аммиака: CuBr + MBr ⟶ M[CuBr2], (M = H,K ) CuBr + 2KCN ⟶ K[Cu(CN)2] + KBr CuBr + 2(NH3 ⋅ H2O) ⟶ [Cu(NH3)2]Br + 2H2O Прочие реакцииПри кипячении водной суспензии бромида меди (I) происходит дисмутация последнего на бромид меди (II) и металлическую медь: Бромид меди(I) медленно окисляется на свету во влажном воздухе: Образует молекулярные аддукты с основаниями Льюиса, например с диметилсульфидом: ПолучениеБромид меди (I) можно получить одним из следующих способов. Термическим разложением бромида меди (II): Реакцией оксида меди (I) с разбавленной бромоводородной кислотой: Восстановлением растворимых солей двухвалентной меди диоксидом серы в присутствии растворимых бромидов, например: Пропусканием газообразного бромоводорода через суспензию металлической меди в эфире с последующим разложением образовавшегося дибромокупрата (I) водорода: 2Cu + 4HBr ⟶ 2H[CuBr2] + H2↑ H[CuBr2] ⟶ CuBr + HBr Восстановлением растворимых солей двухвалентной меди металлической медью в присутствии бромида калия с последующим разложением образовавшегося дибромокупрата (I) калия: ПрименениеБромид меди (I) применяется в органическом синтезе. Реакция взаимодействия меди и бромоводородаРеакция взаимодействия меди и бромоводородаУравнение реакции взаимодействия меди и бромоводорода: Реакция взаимодействия меди и бромоводорода. В результате реакции образуются дибромокупрат (I) водорода и водород. Для проведения реакции медь используется в виде суспензии. Реакция протекает при условии: в эфире и при нормальных условиях. Формула поиска по сайту: 2Cu + 4HBr → 2H[CuBr2] + H2. Реакция взаимодействия цинка и гидроксида натрияРеакция взаимодействия гидроксида цинка и гидроксида калияРеакция диспропорционирования сульфида галлия (II)Выбрать языкПопулярные записиПредупреждение.Все химические реакции и вся информация на сайте предназначены для использования исключительно в учебных целях — только для решения письменных, учебных задач. Мы не несем ответственность за проведение вами химических реакций. Химические реакции и информация на сайте источники: http://chem.ru/bromid-medi-i.html http://chemicalstudy.ru/reaktsiya-vzaimodejstviya-medi-i-bromovodoroda/ | |||||||||||||||||||||||||||||||||||||||||||||