Acetyl
Наведите курсор на ячейку элемента, чтобы получить его краткое описание.
Чтобы получить подробное описание элемента, кликните по его названию.
| H + | Li + | K + | Na + | NH4 + | Ba 2+ | Ca 2+ | Mg 2+ | Sr 2+ | Al 3+ | Cr 3+ | Fe 2+ | Fe 3+ | Ni 2+ | Co 2+ | Mn 2+ | Zn 2+ | Ag + | Hg 2+ | Pb 2+ | Sn 2+ | Cu 2+ | |
| OH — | Р | Р | Р | Р | Р | М | Н | М | Н | Н | Н | Н | Н | Н | Н | Н | — | — | Н | Н | Н | |
| F — | Р | М | Р | Р | Р | М | Н | Н | М | М | Н | Н | Н | Р | Р | Р | Р | Р | — | Н | Р | Р |
| Cl — | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Н | Р | М | Р | Р |
| Br — | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Н | М | М | Р | Р |
| I — | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | ? | Р | ? | Р | Р | Р | Р | Н | Н | Н | М | ? |
| S 2- | М | Р | Р | Р | Р | — | — | — | Н | — | — | Н | — | Н | Н | Н | Н | Н | Н | Н | Н | Н |
| HS — | Р | Р | Р | Р | Р | Р | Р | Р | Р | ? | ? | ? | ? | ? | Н | ? | ? | ? | ? | ? | ? | ? |
| SO3 2- | Р | Р | Р | Р | Р | Н | Н | М | Н | ? | — | Н | ? | Н | Н | ? | М | М | — | Н | ? | ? |
| HSO3 — | Р | ? | Р | Р | Р | Р | Р | Р | Р | ? | ? | ? | ? | ? | ? | ? | ? | ? | ? | ? | ? | ? |
| SO4 2- | Р | Р | Р | Р | Р | Н | М | Р | Н | Р | Р | Р | Р | Р | Р | Р | Р | М | — | Н | Р | Р |
| HSO4 — | Р | Р | Р | Р | Р | Р | Р | Р | — | ? | ? | ? | ? | ? | ? | ? | ? | ? | ? | Н | ? | ? |
| NO3 — | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | — | Р |
| NO2 — | Р | Р | Р | Р | Р | Р | Р | Р | Р | ? | ? | ? | ? | Р | М | ? | ? | М | ? | ? | ? | ? |
| PO4 3- | Р | Н | Р | Р | — | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н |
| CO3 2- | Р | Р | Р | Р | Р | Н | Н | Н | Н | ? | ? | Н | ? | Н | Н | Н | Н | Н | ? | Н | ? | Н |
| CH3COO — | Р | Р | Р | Р | Р | Р | Р | Р | Р | — | Р | Р | — | Р | Р | Р | Р | Р | Р | Р | — | Р |
| SiO3 2- | Н | Н | Р | Р | ? | Н | Н | Н | Н | ? | ? | Н | ? | ? | ? | Н | Н | ? | ? | Н | ? | ? |
| Растворимые (>1%) | Нерастворимые ( Спасибо! Ваша заявка отправлена, преподаватель свяжется с вами в ближайшее время. Вы можете также связаться с преподавателем напрямую: 8(906)72 3-11-5 2 Скопируйте эту ссылку, чтобы разместить результат запроса » » на другом сайте. Изображение вещества/реакции можно сохранить или скопировать, кликнув по нему правой кнопкой мыши. Если вы считаете, что результат запроса » » содержит ошибку, нажмите на кнопку «Отправить». Этим вы поможете сделать сайт лучше. К сожалению, регистрация на сайте пока недоступна. На сайте есть сноски двух типов: Подсказки — помогают вспомнить определения терминов или поясняют информацию, которая может быть сложна для начинающего. Дополнительная информация — такие сноски содержат примечания или уточнения, выходящие за рамки базовой школьной химии, нужны для углубленного изучения. Здесь вы можете выбрать параметры отображения органических соединений. АминыАмины — органические соединения, продукты замещения атомов водорода в аммиаке NH3 различными углеводородными радикалами. Функциональная группой аминов является аминогруппа — NH2. Классификация аминовПо числу углеводородных радикалов амины подразделяются на первичные, вторичные и третичные. Запомните, что основные свойства аминов выражены тем сильнее, чем больше электронной плотности присутствует на атоме азота. Однако, у третичных аминов три углеводородных радикала создают значительные затруднения для химических реакций. Таким образом, у третичных аминов основные свойства выражены слабее, чем у вторичных аминов. Основные свойства возрастают в ряду: третичные амины (слабые основные свойства) → первичные амины → вторичные амины (основные свойства хорошо выражены). Номенклатура и изомерия аминовНазвания аминов формируются путем добавления суффикса «амин» к названию соответствующего углеводородного радикала: метиламин, этиламин, пропиламин, изопропиламин, бутиламин и т.д. В случае если радикалов несколько, их перечисляют в алфавитном порядке. Общая формула предельных аминов CnH2n+3N. Атомы углерода находятся в sp3 гибридизации. Для аминов характерна структурная изомерия: углеродного скелета, положения функциональной группы и изомерия аминогруппы. Получение
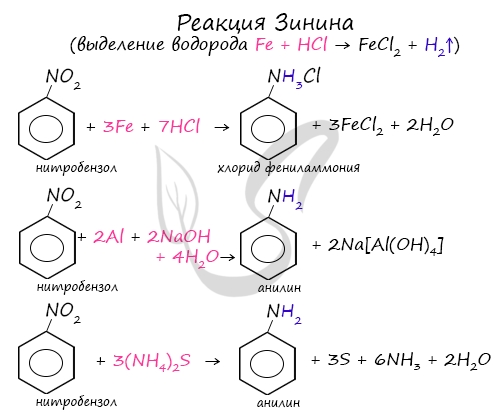
В основе этой реакции лежит замещение атома галогена в галогеналканах на аминогруппу, при этом образуются амин и соль аммония. При такой реакции нитрогруппа превращается в аминогруппу, образуется вода. Знаменитой является предложенная в 1842 году Н.Н. Зининым реакция получения аминов восстановления ароматических нитросоединений (анилина и других). Она возможна в нескольких вариантах, главное, чтобы в начале реакции выделился водород. Реакция сопровождается разрушением карбонильной группы и отщеплении ее от молекулы амида в виде воды. Этим способом в промышленности получают гексаметилендиамин, используемый в изготовлении волокна — нейлон. В промышленности амины получают реакцией аммиака со спиртами, в ходе которой происходит замещение гидроксогруппы на аминогруппу. В ходе реакции галогеналканов с аммиаком, аминами, становится возможным получение первичных, вторичных и третичных аминов. Химические свойства аминов
Как и аммиак, амины обладают основными свойствами, их растворы окрашивают лакмусовую бумажку в синий цвет. В реакции с водой амины образуют гидроксиды алкиламмония, которые аналогичны гидроксиду аммония. Анилин с водой не реагирует, так как является слабым основанием. Как основания, амины вступают в реакции с различными кислотами и образуют соли алкиламмония. Данная реакция помогает различить первичные, вторичные и третичные амины, которые по-разному с ней взаимодействуют. При конденсации первичных аминов с альдегидами и кетонами получают основания Шиффа, соединения, которые содержат фрагмент «N=C». Соли аминов легко разлагаются щелочами (растворимыми основаниями). В результате образуется исходный амин, соль кислоты и вода. При горении аминов азот чаще всего выделяется в молекулярном виде, так как для реакции азота с кислородом необходима очень высокая температура. Выделение углекислого газа и воды обыкновенно при горении органических веществ. © Беллевич Юрий Сергеевич 2018-2022 Данная статья написана Беллевичем Юрием Сергеевичем и является его интеллектуальной собственностью. Копирование, распространение (в том числе путем копирования на другие сайты и ресурсы в Интернете) или любое иное использование информации и объектов без предварительного согласия правообладателя преследуется по закону. Для получения материалов статьи и разрешения их использования, обратитесь, пожалуйста, к Беллевичу Юрию. Как будут реагировать с азотистой кислотой следующие амины : метиламин, диметиланилин, триэтиламин, анилин?Химия | 10 — 11 классы Как будут реагировать с азотистой кислотой следующие амины : метиламин, диметиланилин, триэтиламин, анилин? Написать уравнение реакции. CH3 — NH2 + HO — NO — > ; CH3 — OH + N2 + H2O (CH3)2 — NH + HO — NO — > ; (CH3)2 — N — N = O + H2O C6H5 — NH2 + HO — NO — > ; C6H5 — OH + N2 + H2O. Напишите уравнения реакций, с помощью которых можно осуществить следующие превращения : уксусная кислота→ аминоуксусная кислота→ метиламин?Напишите уравнения реакций, с помощью которых можно осуществить следующие превращения : уксусная кислота→ аминоуксусная кислота→ метиламин. Даны вещества : магний, гидроксид бария, соляная кислота, гидроксид меди, оксид кальция и вода ?Даны вещества : магний, гидроксид бария, соляная кислота, гидроксид меди, оксид кальция и вода . Какие из этих веществ будут реагировать между собой ? Написать уравнения реакций. Помогите?1. Бромоводород реагирует с : а)анилином, глицином , этанолом б)изопропиламином, анилином , формальдегидом в)гликоколом, муравьиной кислотой, изобутиленом г)метиламином , уксусной кислотой, метанолом. Какие объемы (при н?Какие объемы (при н. У. ) азота и оксида углерода (IV) образуются в результате полного сгорания : а) 12, 4 метиламина б) 0, 56 л метиламина (н. У) в) 1, 86 г анилина г) 2, 02 г триэтиламина. Запишите уравнение реакции анилина с соляной кислотой?Запишите уравнение реакции анилина с соляной кислотой. Как изменяется валентность азота в ходе этой реакции? Соляная кислота с массовой долей хлороводорода 20% прореагировала в одном случае с метиламином массой 8, 68г, а в другом — с анилином массой 26, 04г?Соляная кислота с массовой долей хлороводорода 20% прореагировала в одном случае с метиламином массой 8, 68г, а в другом — с анилином массой 26, 04г. В каком отношении по массе находятся растворы соляной кислоты , взятые для данных реакций с аминами? 5. Какие из следующих веществ могут реагировать между собой : этанол, гидроксид натрия, анилин, соляная кислота, уксусная кислота?5. Какие из следующих веществ могут реагировать между собой : этанол, гидроксид натрия, анилин, соляная кислота, уксусная кислота? Напишите уравнения соответствующих реакций. Даны следующие вещества : гидроксид кальция, соляная кислота, оксид серы(6), вода, оксид меди(2)?Даны следующие вещества : гидроксид кальция, соляная кислота, оксид серы(6), вода, оксид меди(2). Какие из них будут реагировать между собой? Напишите уравнения реакций. Составьте уравнение реакции толуол и азотистая кислота?Составьте уравнение реакции толуол и азотистая кислота. Написать реакции Метиламин + азотистая кислота Анилин + серная кислота?Написать реакции Метиламин + азотистая кислота Анилин + серная кислота. Перед вами страница с вопросом Как будут реагировать с азотистой кислотой следующие амины : метиламин, диметиланилин, триэтиламин, анилин?, который относится к категории Химия. Уровень сложности соответствует учебной программе для учащихся 10 — 11 классов. Здесь вы найдете не только правильный ответ, но и сможете ознакомиться с вариантами пользователей, а также обсудить тему и выбрать подходящую версию. Если среди найденных ответов не окажется варианта, полностью раскрывающего тему, воспользуйтесь «умным поиском», который откроет все похожие ответы, или создайте собственный вопрос, нажав кнопку в верхней части страницы. 1) СH3 — CH2 — CH2 — CH = CH2(пентен — 1) 2)СH3 — CH = CH — CH2 — CH3(пентен — 2) 3)СH3 — CH2 — C = CH2(2 — метилбутен — 1) I CH3 4) СH3 — CH = C — CH3(2 — метилбутен — 2) I CH3 5)СH3 — CH — CH = CH2(3 — метилбутен — 1) I CH3 6)Во вложении(циклопента.. BaCl₂ + AgNO₃ → Ba(NO₃)₂ + AgCl↓ Pb(NO₃)₂ + K₂S →KNO₃ + PbS↓ 3Ca(NO₃)₂ + 2H₃PO₄ →6HNO₃ + Ca₃(PO₄)₂↓ Ba(NO₃)₂ + Na₂SO₄ →2NaNO₃ + BaSO₄↓ Реакция протекает до конца, если 1. Образуется осадок 2. Выделяется газ 3. Образуется H₂O Стрелками указаны осад.. Я уже сегодня решал похожее задание S + O2 = SO2Найдем кол — во в — ва серы1)n = m / Mn(S) = 8г / 32г / моль = 0. 25 моль2)Vs = Vso2, значит, теперь просто подставим все в форумулу : m = n * MmSO2 = 0. 25моль * 64г / моль = 16 гОтвет : m(SO2) = 16г.. Mr(K2MnO4) = Ar(K) * 2 + Ar(Mn) + Ar(O) * 4 = 39 * 2 + 55 + 16 * 4 = 197 Mr — относительная молекулярная масса Ar — относительная атомная масса w — массовая доля w(K) = 39 * 2 / 197 = 0. 40 = 40% w(Mn) = 55 / 197 = 0. 28 = 28% w(O2) = 64 / 197 = 0. По ряду химических и физических свойств, специфичных исключительно для железа. Самая простая, известная всем качественная химическая реакция с высокой степенью достоверности указывающая на принадлежность металла к железу — это его ржавление. Это пр.. По ряду химических и физических свойств, специфичных исключительно для железа. Самая простая, известная всем качественная химическая реакция с высокой степенью достоверности указывающая на принадлежность металла к железу — это его ржавление. Это пр.. Третья реакция невозможна, т. К. степени окисленияAl разные, а должны быть одинаковые. 1) 4Аl + 6О2 = 2Аl2О3 2) 2Аl2О3 + 6HCl = 2AlCl3 + 3H2O 3) AlCl3 + 3NaOH = Al(OH)3 + 3NaCl 4) 2Al(OH)3 + 3H2SO4 = Al2(SO4)3 + 6H2O. Na₂CO₃ + H₂SO₄ = Na₂SO₄ + CO₂ + H₂O V(CO₂) / V₀ = m(Na₂CO₃) / M(Na₂CO₃) V(CO₂) = V₀m(Na₂CO₃) / M(Na₂CO₃) w = V'(CO₂)M(Na₂CO₃) / источники: http://studarium.ru/article/193 http://himia.my-dict.ru/q/1779723_kak-budut-reagirovat-s-azotistoj-kislotoj/ |