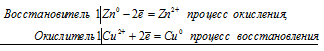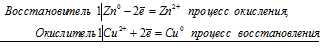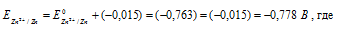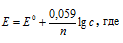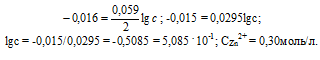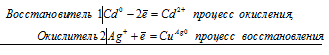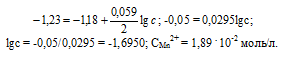Молекулярное уравнения с медным купоросом
1) Составьте молекулярное уравнение реакции серной кислоты с оксидом меди(II), о которой говорилось в тексте;
2) Укажите признак(и), который(-е) наблюдается(-ются) при протекании этой реакции.
Прочитайте следующий текст и выполните задания 5—7.
Сульфат меди(II) — важнейшая из солей меди. Кристаллогидрат сульфата меди(II) называют медным купоросом. В сельском хозяйстве медный купорос применяется как антисептик, фунгицид и медно-серное удобрение. В промышленности эту соль применяют в производстве ацетатного волокна, а также используют в качестве фиксатора окраски и консерванта. Сульфат меди(II) в промышленности получают различными способами, например растворением оксида меди(II)
в серной кислоте
Эта соль часто служит исходным сырьём для получения других соединений, например гидроксида меди(II)
Для водного раствора сульфата меди(II) возможна реакция с металлами активнее меди, например с цинком. Сульфат меди(II) является соединением с умеренной токсичностью. Однако работать с порошком или пудрой сульфата меди(II) следует осторожно, не допуская их пыления.
Сложные неорганические вещества можно классифицировать по четырём группам, как показано на схеме. В эту схему для каждой из четырёх групп впишите по одной химической формуле веществ из числа тех, о которых говорится в приведённом тексте.
| оксид | основание | кислота | соль |
Химические формулы запишите в таблицу в следующем формате: Al2(SO4)3.
1. — бинарное соединение, в котором один из атомов является кислородом, что говорит о его принадлежности к классу оксидов.
2. — является основанием, так как это основный гидроксид.
3. Кислота должна иметь ион водорода, примером может служить серная кислота
4. Соль состоит из иона металла и иона кислотного остатка, известным примером является сульфат меди (II)
Ответ: Оксид — основание —
кислота —
соль —
Составление электронных и молекулярных уравнений реакций. Уравнение Нернста (Nernst)
Решение задач по химии на составление электронных и молекулярных уравнений реакций окисления
Задание 241.
В два сосуда с голубым раствором медного купороса поместили в первый цинковую пластинку, а во второй серебряную. В каком сосуде цвет раствора постепенно пропадает? Почему? Составьте электронные и молекулярные уравнения соответствующей реакции.
Решение:
Стандартные электродные потенциалы цинка, меди и серебра соответственно равны -0,76 В, +0,34 В и +0,80 В. Исходя из того, что цинк имеет более электроотрицательный потенциал, чем медь, то между цинком и медным купоросом проходит реакция (цинк вытесняет медь из соли), и раствор соли при этом обесцвечивается, так как образуется бесцветный сульфат цинка:
Zn0 + Cu 2+ = Zn 2+ + Cu 0
Zn + CuSO4 = ZnSO4 + Cu
Серебро, имея более электроположительный потенциал, чем медь не способно вытеснять ионы меди из сульфата меди, поэтому раствор медного купороса, с опущенной в него серебряной пластинкой, не обесцвечивается.
Задание 242.
Увеличится, уменьшится или останется без изменения масса цинковой пластинки при взаимодействии ее с растворами: а) CuSO4; б) МgSO4; в) Рb(NO3)2? Почему? Составьте электронные и молекулярные уравнения соответствующих реакций.
Решение:
а) Стандартные электродные потенциалы цинка и меди соответственно равны -0,76 В и +0,34 В. Исходя из того, что цинк имеет более электроотрицательный потенциал, чем медь, то между цинком и медным купоросом проходит реакция (цинк вытесняет медь из соли), и раствор соли при этом обесцвечивается, так как образуется бесцветный сульфат цинка, а цинковая пластинка будет уменьшаться по массе:
Zn 0 + Cu 2+ = Zn 2+ + Cu 0
б) Так как стандартный электродный потенциал цинка (-0,76 В) больше, чем стандартный электродный потенциал магния (-2,36 В), то цинк не способен вытеснять магний из растворов его солей, поэтому цинковая пластинка останется без изменений.
в) Так как стандартный электродный потенциал цинка (-0,76 В) меньше, чем у свинца (-0,13 В), то металлический цинк будет обладать большими восстановительными способностями чем ионы Pb 2+ , и реакция будет протекать с растворением цинковой пластинки, т. е. её масса будет уменьшаться.
Zn 0 + Pb 2+ = Zn 2+ + Pb 0
Задание 243.
При какой концентрации ионов Zn 2+ (в моль/л) потенциал цинкового электрода будет на 0,015 В меньше его стандартного электродного потенциала? Ответ: 0,30 моль/л.
Решение:
Найдём значение электродного потенциала цинка в растворе его соли:
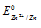
Электродный потенциал металла (Е) зависит от концентрации его ионов в растворе. Эта зависимость выражается уравнением Нернста:
Е 0 – стандартный электродный потенциал металла; n – число электронов, принимающих участие в процессе; с – концентрация ионов металла в растворе его соли (при точных вычислениях – активность). Так как уменьшение потенциала цинка равно 0,015 В, то используя уравнение Нернста, получим выражение для расчета концентрации ионов цинка в растворе:
Ответ: 0,30 моль/л.
Задание 244.
Увеличится, уменьшится или останется без изменения масса кадмиевой пластинки при взаимодействии ее с растворами:
а); AgNO3; б) ZnSO4; в) NiSO4? Почему? Составьте электронные и молекулярные уравнения соответствующих реакций.
Решение:
а) Стандартные электродные потенциалы кадмия и серебра соответственно равны -0,403 В и +0,80 В. Исходя из того, что кадмий имеет более электроотрицательный потенциал, чем серебро, то между кадмием и нитратом серебра проходит реакция (кадмий вытесняет серебро из соли), и кадмиевая пластинка при этом будет уменьшаться по массе.
Cd 0 + 2Ag + = Cd 2+ + 2Ag 0
б) Так как стандартный электродный потенциал кадмия (-0,403 В) больше, чем стандартный электродный потенциал цинка (-0,76 В), то кадмий не способен вытеснять цинк из растворов его солей, поэтому кадмиевая пластинка останется без изменений.
в) Так как стандартный электродный потенциал кадмия (-0,403 В) меньше, чем у никеля (-0,25 В), то металлический кадмий будет обладать большими восстановительными способностями чем ионы Ni 2+ , и реакция будет протекать с растворением кадмиевой пластинки, т. е. её масса будет уменьшаться.
Cd 0 + Ni 2+ = Cd 2+ + Ni 0
Задание 245.
Марганцевый электрод в растворе его соли имеет потенциал -1,23 В. Вычислите концентрацию ионов Мn 2+ (моль/л). Ответ. 1,89 . 10-2 моль/л.
Решение:
Электродный потенциал металла (Е) зависит от концентрации его ионов в растворе. Эта зависимость выражается уравнением Нернста:
Е 0 – стандартный электродный потенциал металла; n – число электронов, принимающих участие в процессе; с – концентрация ионов металла в растворе его соли (при точных вычислениях – активность). Так как уменьшение потенциала цинка равно 0,015 В, то используя уравнение Нернста, получим выражение для расчета концентрации ионов Mn 2+ в растворе:
Ответ. 1,89 . 10 -2 моль/л.
Подборка простых опытов с медным купоросом в домашних условиях
В прошлой статье я рассказывала про медный купорос, что это такое, где применяется и даже как некоторые им лечатся (вот только не знаю, вылечиваются ли?), а сегодня предлагаю поделать опыты с медным купоросом в домашних условиях.
Обо всех этих экспериментах я уже рассказывала в рубрике «Похимичим», так что сейчас, по сути, просто собираю их все вместе, так как они раскиданы по разным статьям.
В начале, как обычно предупреждаю о соблюдении правил техники безопасности!
Напоминаю, что практически все опыты (кроме одного) мы будем делать с раствором медного купороса. Чтобы его получить, растворите половину чайной ложки в стакане воды – этого вполне хватит на все сегодняшние эксперименты. Предлагаю начать с самого простого и похимичить гвоздем.
Опыт с медным купоросом и железным гвоздем
Все очень просто – в раствор купороса опускаете чистый (имеется ввиду без ржавчины и масла) железный гвоздь и ждете. Химическая реакция пройдет сама, без вашего дальнейшего участия. Первые результаты будут видны уже через несколько минут. Ну а самым терпеливым советую «забыть» про происходящее на пару недель. Будет очень интересно.
Подробнее читайте вот в этой статье.
Взаимодействие с аммиаком
В светло-голубой раствор капаем немного аммиака. Вуаля! Готов ярко-фиолетовый раствор аммиаката меди. Не забивайте голову названием, просто наслаждайтесь красивым зрелищем.
Взаимодействие с гидроксидом натрия
Добавляем немного гидроксида натрия. Получается красивый голубой осадок гидроксида меди. Не выливайте его, он нам пригодится в следующем опыте.
Красивые превращения глюкозы
Вам понадобится аптечный раствор чистой глюкозы. Приливаем ее к осадку, полученному в предыдущем опыте, и аккуратно нагреваем. Ярко-голубой осадок постепенно превратится сначала в желтый раствор, затем – в красный.
Делать все нужно достаточно внимательно и аккуратно, поэтому посмотрите, как я делала.
Опыты с яйцом
Денатурация (разрушение) белка
Берем сырое яйцо и отделяем белок от желтка. Белок помещаем в стакан, добавляем немного воды,перемешиваем и делим на две части, то есть на два эксперимента. К первой части приливаем немного медного купороса. После перемешивания получаем вот такую невразумительную массу:
Биуретовая реакция
Ко второй части белка добавляем немного гидроксида натрия, а потом – несколько капель купороса. Получаем ярко-фиолетовую окраску раствора.
Подробно об этих реакциях можно прочитать вот здесь.
Взаимодействие с поваренной солью
Разводим в стакане с водой немного обычной поваренной соли и смешиваем с раствором медного купороса. Любуемся изумрудно-зеленой окраской получившегося раствора.
Желающих продолжить этот опыт дальше отсылаю к статье «Цветные реакции». В ней вы найдете много интересного.
Забавный химический фокус
Он потребует от вас некоторых приготовлений (минут на пять), но оно того стоит. Нужна всего лишь старая сковородка и кристаллический (не раствор!) медный купорос. Будем с помощью воды превращать белое вещество в синее. Подробная инструкция здесь.
Морозные узоры на стекле
Хоть сейчас и лето, но вы легко можете создать на стекле самые настоящие морозные узоры.
Выращиваем химический сад
Еще один очень простой опыт. Единственное, что от вас потребуется, это, как и в случае с гвоздем, терпение. Ну и немного обычного канцелярского силикатного клея. Подробности в статье «Химические водоросли».
Непослушная пена
Ну и под занавес, эффектный опыт по получению пены. Его можно делать в двух вариантах – с медным купоросом либо с марганцовкой. По сути, процессы идут одинаковые и результат также практически одинаковый. Правда, придется побегать по аптекам в поисках гидроперита. Если вам улыбнется удача и вы его купите, то внимательно читайте вот эту статью и химичьте в свое удовольствие!
Вот и все на сегодня. Надеюсь, эта подборка домашних опытов с медным купоросом вам пригодится. Может, у вас есть какие-то идеи, что еще можно сделать? Пишите в комментариях, делитесь опытом.
Всем хорошего настроения!
P.S. Я совсем забыла про самый распространенный опыт — выращивание красивых синих кристаллов. Обещаю исправиться и в ближайшее время показать вам его
KidsChemistry теперь есть и в социальных сетях. Присоединяйтесь прямо сейчас! Google+ , В контакте , Одноклассники , Facebook , Twitter
http://buzani.ru/zadachi/khimiya-shimanovich/938-elektrodnye-potentsialy-metallov-zadaniya-241-245
http://kidschemistry.ru/prostye-opyty-s-mednym-kuporosom-v-domashnix-usloviyax.html