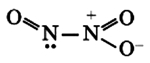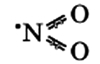Оксид азота I: строение и химические свойства
| Оксиды азота | Цвет | Фаза | Характер оксида |
| N2O Оксид азота (I), закись азота, «веселящий газ» | бесцветный | газ | несолеобразующий |
| NO Оксид азота (II), закись азота, «веселящий газ» | бесцветный | газ | несолеобразующий |
| N2O3 Оксид азота (III), азотистый ангидрид | синий | жидкость | кислотный |
| NO2 Оксид азота (IV), диоксид азота, «лисий хвост» | бурый | газ | кислотный (соответствуют две кислоты) |
| N2O5 Оксид азота (V), азотный ангидрид | бесцветный | твердый | кислотный |
Оксид азота (I) N2O, оксид диазота, закись азота, веселящий газ – это несолеобразующий оксид . Малые концентрации закиси азота вызывают лёгкое опьянение (отсюда название — «веселящий газ»). При вдыхании чистого газа быстро развиваются состояние опьянения и сонливость. Закись азота обладает слабой наркотической активностью, в связи с чем в медицине её применяют в больших концентрациях. В смеси с кислородом при правильном дозировании (до 80 % закиси азота) вызывает хирургический наркоз.
Строение молекулы оксида азота (I) нельзя описать методом валентных связей. Так как оксид азота (I) состоит из двух, так называемых резонансных структур, которые переходят одна в другую:
Общую формулу в таком случае можно задать, обозначая изменяющиеся связи в резонансных структурах пунктиром:
Получить оксид азота (I) в лаборатории можно разложением нитрата аммония:
Химические свойства оксида азота (I)
1. При нормальных условиях оксид азота (I) инертен. При нагревании проявляет свойства окислителя . Оксид азота (I) при нагревании окисляет водород, аммиак, металлы, сернистый газ и др. При этом азот восстанавливается в простое вещество.
N2O + Mg → N2 + MgO
Еще пример : оксид азота (I) окисляет углерод и фосфор при нагревании:
2. При взаимодействии с сильными окислителями N2O может проявлять свойства восстановителя.
Например , N2O окисляется раствором перманганата в серной кислоте:
3. Как несолеобразующий оксид, при обычных условиях с основаниями, основными оксидами, амфотерными оксидами, кислотными оксидами, кислотами и амфотерными гидроксидами оксид азота (I) не реагирует:
Химические свойства N2O
Читайте также:
|
| Тема или раздел темы | Стр. |
| Основные классы неорганических соединений | |
| Оксиды. Определение, примеры оксидов. | |
| Бинарные соединения, не являющиеся оксидами: пероксиды, надпероксиды и озониды. Фториды кислорода | |
| Классификация оксидов. | |
| Кислотные оксиды.Определение, перечень элементов, дающих кислотные оксиды | |
| Способы получения кислотных оксидов. | |
| Получение кислотных оксидов путём прямого синтеза из простых веществ | |
| Получение кислотных оксидов путём доокисления других оксидов до кислотных кислородом | |
| Получение кислотных оксидов путём доокисления других оксидов озоном | |
| Получение кислотных оксидов путём реакции димеризации | |
| Получение кислотных оксидов путём разложения веществ: кислот и солей | |
| Зависимость температуры разложения карбонатов от природы металлов | |
| Зависимость продуктов разложения нитратов от природы металлов | |
| Получение кислотных оксидов путём реакций обмена между кислотными оксидами и кислотами | |
| Получение кислотных оксидов путём реакций обмена между кислотными оксидами и солями | |
| Получение кислотных оксидов путём взаимодействия солей нестойких кислот с кислотами | |
| Получение кислотных оксидов в результате специфических реакций: контрпропорционирования, диспропорционирования, межмолекулярных ОВР | |
| Физические свойства кислотных оксидов | |
| Агрегатное состояние кислотных оксидов | |
| Растворимость кислотных оксидов | |
| Цвет кислотных оксидов | |
| Химические свойства кислотных оксидов | |
| Реакции кислотных оксидов с водой – получение кислот | |
| Реакции диспропорционирования при получении кислот из кислотных оксидов | |
| Реакции кислотных оксидов со щелочами в растворах и при сплавлении | |
| Реакции кислотных оксидов с нерастворимыми в воде основаниями и амфотерными гидроксидами | |
| Реакции кислотных оксидов с основными оксидами | |
| Реакции кислотных оксидов с амфотерными оксидами | |
| Реакции кислотных оксидов с некоторыми солями в растворе и при сплавлении | |
| Реакции кислотных оксидов с гидроксил и аммиак содержащими комплексами | |
| Участие кислотных оксидов в окислительно-восстановительных реакциях | |
| Обменные реакции кислотных оксидов с кислотами | |
| Реакции некоторых кислотных оксидов с кислотами. Образование олеума и пирофосфорной кислоты | |
| Реакции некоторых кислотных оксидов с органическими веществами: солями ацетилена и терминальных алкинов, фенолятами(реакция Кольбе-Шмитта), гетероциклическими соединениями: фураном и пирролом | |
| Основные оксиды.Определение. | |
| Перечень элементов, дающих основные оксиды | |
| Способы получения основных оксидов | |
| Получение основных оксидов прямым синтезом из простых веществ | |
| Получение основных оксидов из пероксидов путём сплавления с соотстветвующим металлом | |
| Получение основных оксидов из надпероксидов путём сплавления с соотстветвующим металлом | |
| Получение основных оксидов путём разложения нерастворимых в воде оснований | |
| Получение основных оксидов путём разложения солей | |
| Получение основных оксидов путём восстановления других оксидов углеродом (коксом), активными металлами или водородом | |
| Получение основных оксидов путём доокисления одних основных оксидов до других | |
| Получение основных оксидов путём реакций контрпропорционирования | |
| Физические свойства основных оксидов | |
| Температуры плавления и кипения основных оксидов | |
| Диспропорционирование некоторых основных оксидов при нагревании на металл и пероксид | |
| Разложение некоторых основных оксидов при нагревании на металл и кислород | |
| Цвет и запах основных оксидов | |
| Химические свойства основных оксидов | |
| Реакция некоторых основных оксидов с водой – получение гидроксидов | |
| Переведение основных оксидов, не реагирующих с водой, в гидроксиды последовательным действием кислоты и щёлочи | |
| Реакция основных оксидов с кислотами | |
| Реакция основных оксидов с кислотными оксидами | |
| Реакция основных оксидов с амфотерными оксидами и гидроксидами при сплавлении | |
| Реакция некоторых основных оксидов с жидким аммиаком | |
| Диспропорционирование некоторых основных оксидов при нагревании | |
| Окисление некоторых основных оксидов кислородом воздуха – получение оксидов других типов | |
| Восстановление некоторых основных оксидов под воздействием водорода, углерода (кокса) и более активных металлов | |
| Амфотерные оксиды. Определение. Перечень элементов, дающих амфотерные оксиды | |
| Доказательство ошибочности отнесения оксидов MgO, MnO, FeO, CoO, NiO, Ag2O, Cu2O и CuO к основным | |
| Способы получения амфотерных оксидов | |
| Получение амфотерных оксидов прямым синтезом из простых веществ | |
| Получение амфотерных оксидов путём разложения гидроксидов | |
| Получение амфотерных оксидов путём разложения солей | |
| Получение амфотерных оксидов путём разложения комплексных соединений | |
| Получение амфотерных оксидов путём доокисления основных оксидов кислородом | |
| Получение амфотерных оксидов путём разложения кислотных оксидов | |
| Получение одних амфотерных оксидов из других путём восстановления угарным газом | |
| Получение некоторых амфотерных оксидов путём окисления соответствующих им металлов сложными веществами при высоких температурах | |
| Получение некоторых амфотерных оксидов путём обжига минералов-сульфидов | |
| Физические свойства амфотерных оксидов | |
| Температуры плавления и кипения некоторых амфотерных оксидов. Таблица. | |
| Реакции разложения амфотерных оксидов на металл и кислород, которые происходят до достижения ими температуры плавления | |
| Реакции разложения амфотерных оксидов на другой оксид и кислород, которые происходят до достижения ими температуры плавления | |
| Цвет амфотерных оксидов.Их термохромные свойства | |
| Химические свойства амфотерных оксидов | |
| Реакция амфотерных оксидов с кислотами | |
| Реакция амфотерных оксидов с кислотными | |
| Реакция амфотерных оксидов со щелочами при сплавлении | |
| Реакция амфотерных оксидов со щелочами в их концентрированных водных растворах | |
| Реакция амфотерных оксидов с гидратом аммиака | |
| Практическое значение некоторыхкомплексных соединений | |
| Реакция амфотерных оксидов с основными оксидами при сплавлении или спекании | |
| Реакция одних амфотерных оксидов с другими при высоких температурах | |
| Реакции восстанавления амфотерных оксидов до соответствующих металлов угарным газом, более активными металлами, водородом, углеродом и цианидами щелочных металлов | |
| Реакции восстанавления амфотерных оксидов с соответствующими металлами до оксидов с более низкой степенью окисления металла – реакции контрпропорционирования | |
| Реакции окисления некоторых амфотерных оксидов кислородом в водной суспензии | |
| Реакции окисления некоторых амфотерных оксидов кислородом при высокой температуре | |
| Реакции окисления некоторых амфотерных оксидов сложными веществами: конц. азотной кислотой, нитратами и хлоратами в щелочной среде | |
| Участие некоторых амфотерных оксидов в сложных окислительно- восстановительных реакциях | |
| Участие большинства амфотерных оксидов в реакциях образования комплексных соединений | 15, |
| Амфотерные оксиды как катализаторы при проведении неорганических и органических реакций | |
| Несолеобразующие оксиды.Определение. Перечень несолеобразующих оксидов | |
| Оксид углерода (II) CO | |
| Электронное и пространственное строение оксида углерода (II) | |
| Прострпнственное строение комплексного соединения [Fe(CO)5], | |
| Физические свойства СО | |
| Токсические свойства СО | |
| Способы получения СО.Прямым синтезом из простых веществ | |
| Получение СО при взаимодействии паров воды с раскалённым углем (получение водяного газа): | |
| Получение СО при взаимодействии углекислого газа с раскаленным углем | |
| Образование СО при получении некоторых карбидов из соответствующих оксидов и угля при высоких температурах | |
| Образование СО при получении некоторых металлов из их карбонатов | |
| Образование СО при разложении муравьиной кислоты (лабораторный способ получения СО) | |
| Образование СО при разложении карбонильных комплексов | |
| Химические свойства СО | |
| Реакции СО с простыми вещестми: кислородом – горение на воздухе и окисление при комнатной температуре в присутствии катализатора – пиролюзита (MnO2) | |
| Реакции СО с водородом (реакция Сабатье и Сандерана) с получением метана и синтез метанола | |
| Реакция СО с хлором – получение фосгена | |
| Реакция СО с металлами – получение карбонилсодержащих комплексов | |
| Реакции СО с водяным паром – получение водорода | |
| Реакции СО с раствором щёлочи или гидрата аммиака под давлением | |
| Реакция СО с аммиаком при высокой температуре и наличии катализаторов | |
| Реакция СО с пентоксидом йода – полуколичественная реакция на содержание СО в газовых смесях. | |
| Реакции СО с пероксидами и надпероксидами натрия и калия. Использование их в изолирующих противогазах и в «фильтрующих» элементах, применяемых на подводных лодках и на космических обитаемых объектах | |
| Реакции СО, как восстановителя, с сильными окислителями в щелочной и нейтральной среде | |
| Реакции СО с органическими веществами: бензолом, ацетиленом и водородом, ацетиленом и водой и с ацетиленом и спиртами. Получение метилакрилата и полиметилакрилата | |
| Оксид азота(II) − NO | |
| Электронное и пространственное строение оксида азота (II). | |
| Физические свойства NO | |
| Способы получения NO | |
| Получение NO прямым синтезом из простых веществ в электрической дуге | |
| Получение NO сжиганием аммиака в присутствии катализаторов | |
| Получение NO сжиганием аминов в присутствии катализаторов | |
| Получение NO взаимодействием нитритов металлов с концентрированной серной кислотой | |
| Образование NO при разложении оксида азота (III): | |
| Образование NO при восстановлении нитритов в кислой среде | |
| Образование NO при восстановлении разбавленной азотной кислоты тяжёлыми металлами | |
| Образование NO при окислении «царской водкой» благородных металлов | |
| Образование NO при разложении хлорида нитрозила | |
| Образование NO при гидролизе трифторида азота | |
| Образование NO при восстановлении фторида или хлорида нитрозила красным фосфором, кремнием или металлами | 23, |
| Химические свойства оксида азота II – NO | |
| Разложениние NO на простые вещества при 700 О С | |
| Диспропорционирование NO при контакте с твёрдой щёлочью | |
| NO, как окислитель, по отношению к водороду, цинку в щелочной среде, сероводороду, оксиду серы (IV), углероду, фосфору, меди | |
| NO, как восстановитель, по отношению к кислороду, озону, хлорноватистой кислоте, оксиду хрома (III) | |
| Реакция замещения лигандов (СО) действием на карбонильные комплексы оксида NO | |
| Реакции соединения NO с галогенами и оксидом азота (IV) − NO2 | |
| Димеризация NO при отрицательных температурах | |
| Оксид азота (I) − N2O | |
| Физические свойства N2O: температуры плавления и кипения, качественная оценка растворимости | |
| Зависимость растворимости некоторых газов от их природы и температуры. Таблица | |
| Запах N2O и его наркотическое действие на человека. Проведение операций под N2O | |
| Способы получения N2O | |
| Получение N2O при взаимодействии щелочных и ряда щелочноземельных металлов с концентрированной азотной кислотой | |
| Получение N2O путём термического разложения нитрата аммония | |
| Получение N2O путём взаимодействия при нагревании смеси двух солей, в одной из которых есть ион аммония, а в другой нитрат-ион | |
| Электронное и пространственное строение N2O | |
| Химические свойства N2O | |
| N2O, как восстановитель, по отношению к кислотам – окислителям и сильным окислителям в кислой среде | |
| N2O, как окислитель, по отношению к водороду, углероду, сере, активным металлам | |
| N2O, как окислитель средней силы, по отношению к тяжёлым металлам и фосфору | |
| Горение сложных веществ в N2O | |
| Содержание |
Дата добавления: 2015-08-05 ; просмотров: 69 ; Нарушение авторских прав
Оксиды азота
Азот образует несколько оксидов:
- солеобразующие оксиды:
- N2O3 — оксид азота (III)
- NO2 — оксид азота (IV)
- N2O4 — димер оксида азота (IV)
- N2O5 — оксид азота (V)
- несолеобразующие оксиды:
- N2O — оксид азота (I)
- NO — оксид азота (II)
Все оксиды азота, за исключением N2O, являются ядовитыми веществами.
Оксид азота N2O (I)
Строение молекулы линейное:
N2O (I) — бесцветный газ со слабым запахом и сладковатым вкусом.
- растворяется в воде, но не реагирует с ней;
- разлагается при слабом нагревании:
2N2O → 2N2+O2 - реагирует с водородом со взрывом:
N2O+H2 → N2+H2O - получают разложением нитрата аммония:
NH4NO3 → N2O+2H2O - применяют в смеси с кислородом в качестве «веселящего газа», как средство общего наркоза в медицине, а также для получения азидов:
N2O+NaNH2 → NaN3+H2O
Оксид азота NO(II)
Молекула имеет вид:
Оксид азота NO(II) димеризуется (образуется новое вещество путём соединения двух структурных элементов) только при низких температурах.
- Бесцветный газ, без запаха.
- Малорастворим в воде.
- Легко окисляется на воздухе с образованием диоксида азота:
2NO+O2=2NO2. - Взаимодействует с другими окислителями (CrO3,Cl2, KMnO4).
- Реагирует с активными металлами, водородом:
K+NO=KNO
2NO+2H2=N2+2H2O
NO(II) содержится в выхлопных газах автомобилей с двигателями внутреннего сгорания — проходя через каталитический конвертор, состоящий из нагретых до высокой температуры керамических ячеек, оксиды азота восстанавливаются, а СО окисляется:
2NO+2CO → N2+2CO2
В природе NO(II) образуется во время грозы в результате взаимодействия азота с кислородом при высокой температуре:
N2+O2=2NO.
В промышленных целях NO(II) получают каталитическим окислением аммиака (в роли катализатора используется платина):
4N -3 H3+5O2 0 → 4N +2 O -2 +6H2O
В лабораторных условиях NO(II)получают действием разбавленной азотной кислотой на медь:
3Cu 0 +8HN +5 O3 = 3Cu +2 (NO3)2+2N -2 O↑+4H2O
Монооксид азота используют для получения азотной кислоты.
Оксид азота N2O3(III)
Связь N + -O — образована по донорно-акцепторному механизму.
Оксид азота N2O3(III) при н.у. является темно-синей жидкостью. При низких температурах (ниже -100°C) кристаллизуется.
Оксид азота N2O3(III) является кислотным оксидом, в значительной степени диссоциирует и реагирует со щелочами:
N2O3 ↔ NO2+NO
N2O3+2NaOH = 2NaNO2+H2O
Оксид азота N2O3(III) взаимодействует с водой с образованием азотистой кислоты:
N2O3+H2O = 2HNO2
Азотистая кислота является слабой кислотой, и существует только в водном растворе.
Соли азотистой кислоты — нитриты NaNO2, KNO2 являются устойчивыми соединениями, проявляя, как кислотные, так и восстановительные свойства, поскольку атом азота в них имеет «среднее» значение степени окисления (+3).
Оксид азота NO2(IV)
Связи N-O располагаются под углом друг к другу, при этом они носят промежуточный «полуторный» характер, при этом имеется еще и один неспаренный электрон, как и у NO (см. выше).
При н.у. оксид азота NO2(IV) является ядовитым газом (хорошо растворимым в воде) бурого цвета, с характерным запахом.
Оксид азота NO2(IV) — смешанный оксид, ему соответствуют две кислоты: азотистая и азотная, поэтому, реакция взаимодействия с водой имеет следующий вид:
2N +4 O2+H2O = HN +3 O2+HN +5 O3
При нагревании до 50°C неустойчивая азотистая кислота не образуется:
3NO2+H2O = 2HNO3+NO
На воздухе NO2 взаимодействует с водой с образованием только азотной кислоты:
4N +4 O2+O2 0 +2H2O ↔ 4HN +5 O3 -2
Оксид азота NO2(IV) взаимодействует с растворами щелочей с образованием воды и двух солей — нитрата и нитрита:
2N +4 O2+2NaOH = NaN +3 O2+NaN +5 O3+H2O
В избытке кислорода образуется только нитрат натрия:
4N +4 O2+4NaOH+O2 0 = 4NaN +5 O3 -2 +2H2O
При температуре ниже 22°C молекулы оксида азота NO2(IV) легко соединяются попарно (димеризуются), в результате чего образуется бесцветная жидкость, превращающаяся в кристаллы при дальнейшем охлаждении до температуры ниже -10,2°C.
В промышленных условиях оксид азота NO2(IV) получают путем окисления NO кислородом:
2NO+O2=2NO2
В лабораторных условиях оксид азота NO2(IV) получают окислением меди азотной кислотой (концентрированной), либо разложением нитрата свинца (меди):
Cu+4HNO3(конц) = Cu(NO3)2+2NO2↑+2H2O
2Pb(NO3)2 = 2PbO+4NO2↑+O2↑
Оксид азота NO2(IV) применяют в производстве азотной кислоты.
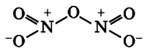
Оксид азота N2O5(V)
Связи N + -O — образуются по донорно-акцепторному механизму: атом азота отдает электрон, играя роль донора и приобретая положительный заряд, атом кислорода присоединяет электрон, выступая в роли акцептора и приобретая отрицательный заряд. Атомы азота проявляют степень окисления +5 (валентность 4).
Оксид азота N2O5(V) (азотный ангидрид, пентаоксид диазота) является кристаллическим веществом белого цвета, легко разлагающееся при нормальных условиях:
2N2O5 = 4NO2+O2
Оксид азота N2O5(V) является кислотным оксидом, который при растворении в воде образует азотную кислоту:
N2O5+H2O = 2HNO3
Оксиды азота N2O3 и N2O5 практического применения не имеют.
Другие соединения азота:
Если вам понравился сайт, будем благодарны за его популяризацию 🙂 Расскажите о нас друзьям на форуме, в блоге, сообществе. Это наша кнопочка:
Код кнопки: 
Политика конфиденциальности Об авторе
http://lektsii.com/2-127324.html
http://prosto-o-slognom.ru/chimia/504_oksid_azota_NO.html