Хлорид натрия: способы получения и химические свойства
Хлорид натрия NaCl — соль щелочного металла натрия и хлороводородной кислоты. Белое кристаллические вещество. Плавится и кипит без разложения. Умеренно растворяется в воде (гидролиза нет);
Относительная молекулярная масса Mr = 58,44; относительная плотность для ж. и тв. состояния d = 2,165; tпл = 800,8º C; tкип = 1465º C;
Способ получения
1. Хлорид натрия можно получить путем взаимодействия натрия и разбавленной хлороводородной кислоты, образуются хлорид натрия и газ водород:
2Na + 2HCl = 2NaCl + H2↑.
2. При комнатной температуре, в результате взаимодействия натрия и хлора, образуется хлорид натрия:
2Na + Cl2 = 2NaCl
3. Концентрированный раствор гидроксида натрия реагирует с концентрированным раствором хлорида аммония при кипении. При этом образуются хлорид натрия, газ аммиак и вода:
NaOH + NH4Cl = NaCl + NH3↑ + H2O
4. При взаимодействии с разбавленной и холодной хлороводородной кислотой пер окси д натрия образует хлорид натрия и пероксид водорода:
5. Разбавленная хлороводородная кислота реагирует с гидроксидом натрия . Взаимодействие хлороводородной кислоты с гидроксидом натрия приводит к образованию хлорида натрия и воды:
NaOH + HCl = NaCl + H2O
6. В результате взаимодействия сульфата натрия и хлорида бария образуется сульфат бария и хлорид натрия:
Качественная реакция
Качественная реакция на хлорид натрия — взаимодействие его с нитратом серебра, в результате реакции происходит образование белого творожного осадка:
1. При взаимодействии с нитратом серебра , хлорид натрия образует нитрат натрия и осадок хлорид серебра:
NaCl + AgNO3 = NaNO3 + AgCl↓
Химические свойства
1. Хлорид натрия вступает в реакцию со многими сложными веществами :
2.1. Хлорид натрия взаимодействует с кислотами :
2.1.1. Хлорид натрия в твердом состоянии при кипении реагирует с концентрированной серной кислотой с образованием сульфата натрия и газа хлороводорода:
а если температуру опустить до 50º С, то твердый хлорид натрия и концентрированная серная кислота образуют гидросульфат натрия и газ хлороводород:
2.2. Хлорид натрия способен вступать в реакцию обмена со многими солями :
2.2.1. Твердый хлорид натрия реагирует с концентрированной и горячей серной кислотой и твердым перманганатом калия . Взаимодействие хлорида натрия с перманганатом калия и серной кислотой приводит к образованию сульфата марганца, натрия, калия, газа хлора и воды:
2.2.2. Хлорид натрия взаимодействует с гидросульфатом натрия при температуре 450–800º C . При этом образуются сульфат натрия и хлороводородная кислота:
2.2.3. При взаимодействии холодного хлорида натрия с насыщенным нитритом серебра выделяются нитрат натрия и осадок хлорид серебра:
NaCl + AgNO2 = NaNO2 + AgCl↓
Ионные уравнения реакций
В качестве примера рассмотрим взаимодействие соляной кислоты и гидроксида натрия в водном растворе:
HCl + NaOH = NaCl + H2O.
Это уравнение написано в молекулярном виде. Молекулярное уравнение данного процесса не отражает реальных явлений, имеющих место при протекании такого взаимодействия, так как в приведенном примере все вещества, кроме воды, являются сильными электролитами и в растворе присутствуют не в виде молекул, а только в виде ионов:
Поэтому уравнение нейтрализации логичнее написать в ионном виде. При переходе от молекулярного к ионному (точнее: полному ионному) уравнению на ионы разбиваются только формулы сильных электролитов, хорошо растворимых в воде:
H + + Cl — + Na + + OH — = Na + + Cl — + H2O.
Полученное выражение можно сократить и получить сокращенное ионное уравнение:
Сокращенное ионное уравнение показывает, что данное взаимодействие сводится к реакции между ионами водорода и гидроксид-анионами с образованием молекул слабого электролита (воды).
Аналогичным образом следует рассматривать и другие процессы, протекающие в растворах с участием электролитов.
CO2 + 2Na + + 2OH — = 2Na + + CO 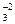
CO2 + 2OH — = CO 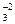
2Ag + + 2NO 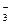
Тема 7. Равновесия в растворах, протолитическое равновесие,
Дата добавления: 2015-04-29 ; просмотров: 2004 ; ЗАКАЗАТЬ НАПИСАНИЕ РАБОТЫ
Напишите уравнения реакций :NaCl + HCl =Na2CO3 + HCl =?
Химия | 5 — 9 классы
Напишите уравнения реакций :
NaCl + HCl = нет реакции!
Реакция не идёт потому что кислоты реагируют с солями более слабых кислот.
Na2CO3 + 2HCl = H2O + CO2 + 2NaCl.
NaCl + HCl – реакция не идет
Na2CO3 + 2HCl = H2O + CO2 + 2NaCl.
Hcl — cl2 — fecl3 — nacl составьте уравнение реакции?
Hcl — cl2 — fecl3 — nacl составьте уравнение реакции.
Напишите уравнение реакции с помощью которых можно осуществить превращения Cl + HCl + NaCl + Cl?
Напишите уравнение реакции с помощью которых можно осуществить превращения Cl + HCl + NaCl + Cl.
Напишите уравнения возможных реакций гидроксида алюминия со следующими веществами : KOH, Li2O, NaCl, HCl, K2SO4?
Напишите уравнения возможных реакций гидроксида алюминия со следующими веществами : KOH, Li2O, NaCl, HCl, K2SO4.
Напишите уравнения реакций :NaCl + HCl =Na2CO3 + HCl =?
Напишите уравнения реакций :
Помогите пож?
Напишите уравнения реакций, которые осуществимы!
Помогите пожалуйстанапишите полные и сокращенные ионные уравнения1) CaCO3 и HCl2) NACl и HCl3) K2CO3 и H2SiO34) NaHCO3 и HCl?
напишите полные и сокращенные ионные уравнения
3) K2CO3 и H2SiO3
ПОМОГИТЕ СРОЧНО ДАЮ 10 БАЛЛОВданы схемы :Zn + HCl = Cu + HCl =Mg + H2SO4 = Au + H2SO4 =NaCl + HCl = H3PO4 + H2SO4 =Na2SO4 + HCl = Na2CO3 + HCl =Fe(OH)3 + HNO3 = NaCl + HNO3 = Напишите уравнение реакци?
ПОМОГИТЕ СРОЧНО ДАЮ 10 БАЛЛОВ
Zn + HCl = Cu + HCl =
Mg + H2SO4 = Au + H2SO4 =
NaCl + HCl = H3PO4 + H2SO4 =
Na2SO4 + HCl = Na2CO3 + HCl =
Fe(OH)3 + HNO3 = NaCl + HNO3 = Напишите уравнение реакций которые осуществимы.
30 БАЛЛОВ?
Составьте уравнения реакций по схеме H2 — H2O — H2S04 — HCL — NaCL.
Напишите уравнения реакций для осуществления превращений :Cl2 → HCl → CuCl2 → BaCl2 → NaCl → Cl2?
Напишите уравнения реакций для осуществления превращений :
Cl2 → HCl → CuCl2 → BaCl2 → NaCl → Cl2.
HCl + NaOH = NaCl + h2oнапишите полное и краткое ионное уравнение?
HCl + NaOH = NaCl + h2o
напишите полное и краткое ионное уравнение.
Вы находитесь на странице вопроса Напишите уравнения реакций :NaCl + HCl =Na2CO3 + HCl =? из категории Химия. Уровень сложности вопроса рассчитан на учащихся 5 — 9 классов. На странице можно узнать правильный ответ, сверить его со своим вариантом и обсудить возможные версии с другими пользователями сайта посредством обратной связи. Если ответ вызывает сомнения или покажется вам неполным, для проверки найдите ответы на аналогичные вопросы по теме в этой же категории, или создайте новый вопрос, используя ключевые слова: введите вопрос в поисковую строку, нажав кнопку в верхней части страницы.
M = 0, 2 * 250 = 50 250 — 160 50 — x x = 32 300 + 50 = 350 C% = 32 * 100 / 350 = 9, 14%.
MgCl2 + 2AgNO3 = Mg(NO3)2 + 2AgCl↓ Mg² + + 2Cl — + 2Ag + + 2NO3 — = Mg² + + 2NO3 — + 2AgCl↓ 2Ag + + 2Cl — = 2AgCl↓.
CaCO3 + 2HNO3 — — >Ca(NO3)2 + H2O + CO2↑.
Реакция идёт до образования газа СО2 : CaCO3 + HNO3 — — — — — > Ca(NO3)2 + H2O + CO2.
Сначала определяем в какой группе и периоде находится элемент Cr — 4 — й период, 6 — я группа. Периоды — количество энергетических электронов ; их будет 4 52 Cr ) ) ) ) 24 2 8 8 6 Почти у всех элементов на 1 — ом и на 2 — ом уровнях получается по 2 ..
Mg + S — > MgS Mg + H2O→Mg(OH)2 + H2 Mg + Cl2→MgCl2 JiOH + H2SO4 — не знаю Na + O2→Na2O Na2SO4 + KOH — не знаю.
Mg + S — > MgS Mg + 2H2O — > Mg(OH)2 + H2 (при высокой температуре) Mg + Cl2 — > MgCl2 2LiOH + H2SO4 — > Li2SO4 + 2H2O 4Na + O2 — > 2Na2O Na2SO4 + KOH — > реакция не идёт.
Mr(NaBr) = 23 + 80 = 103 Mr(Cu(NO3)2) = 64 + 14 * 2 + 16 * 6 = 188.
1)CH4 + Br2 — — — — (hv) — — — — >CH3Br 2)2CH3Br + Na — — — — — — — — — — >CH3 — CH3 + 2NaBr 3)CH3 — CH3 — — — — — — >CH2 = CH2 + H2 4)CH2 = CH2 — — — — >CH(тр. Связь)CH + H2 5)3CH(тр. Связь)CH — — — — >C6H6.
16, 7 г Пусть масса воды М, масса соли в растворе м. Тогда в первом случае 4% раствора имеем 0, 04 = м / (М + м), отсюда получаем, что м = М / 24. Поскольку м + М = 250 г. , то подставив сюда значение м получим для М : М = 240 г. , тогда м = 10 г..
http://helpiks.org/3-32166.html
http://himia.my-dict.ru/q/7409800_napisite-uravnenia-reakcij-nacl-hcl-na2co3/









