Ионные уравнения реакций
В качестве примера рассмотрим взаимодействие соляной кислоты и гидроксида натрия в водном растворе:
HCl + NaOH = NaCl + H2O.
Это уравнение написано в молекулярном виде. Молекулярное уравнение данного процесса не отражает реальных явлений, имеющих место при протекании такого взаимодействия, так как в приведенном примере все вещества, кроме воды, являются сильными электролитами и в растворе присутствуют не в виде молекул, а только в виде ионов:
Поэтому уравнение нейтрализации логичнее написать в ионном виде. При переходе от молекулярного к ионному (точнее: полному ионному) уравнению на ионы разбиваются только формулы сильных электролитов, хорошо растворимых в воде:
H + + Cl — + Na + + OH — = Na + + Cl — + H2O.
Полученное выражение можно сократить и получить сокращенное ионное уравнение:
Сокращенное ионное уравнение показывает, что данное взаимодействие сводится к реакции между ионами водорода и гидроксид-анионами с образованием молекул слабого электролита (воды).
Аналогичным образом следует рассматривать и другие процессы, протекающие в растворах с участием электролитов.
CO2 + 2Na + + 2OH — = 2Na + + CO 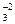
CO2 + 2OH — = CO 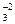
2Ag + + 2NO 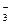
Тема 7. Равновесия в растворах, протолитическое равновесие,
Дата добавления: 2015-04-29 ; просмотров: 2008 ; ЗАКАЗАТЬ НАПИСАНИЕ РАБОТЫ
Реакция гидроксида натрия с соляной кислотой
Повесть о Ромео и Джульетте со счастливым финалом
Ни на одной карте мира вы не найдете страны под названием Химия. Но она существует, и жизнь в ней протекает не менее насыщенно (а иногда и более интересно), чем в любой другой стране. К примеру, самая известная история любви всех веков и народов там заканчивается очень счастливо. Но давайте по порядку, ведь нам предстоит очень многое: познакомиться с химическими Монтекки и Капулетти, выбрать лучшего свидетеля реакции гидроксида натрия и соляной кислоты, слетать в космос, посетить самый лучший ресторан мира, заглянуть на концерт ансамбля песни и пляски Черноморского флота и многое другое.
Для начала заглянем в химическую лабораторию.
Если здесь чтут технику безопасности, то щелочи и их растворы хранятся строго отдельно от кислот и их растворов. Это химические Монтекки и Капулетти: оба семейства агрессивны и находятся в непримиримой вражде. Если они столкнутся без присмотра Химика, жди беды! Да и ученого они не жалуют: так и норовят обжечь или отравить. Поэтому при общении с ними Химик защищается как может: работает в вытяжном шкафу, надевает халат, фартук, перчатки, спецобувь и даже очки или защитный щиток.
И надо же такому случиться, чтобы прекрасный юноша Гидроксид натрия из рода Щелочей влюбился в обворожительную девушку по имени Соляная Кислота из семейства Кислот! Чтобы понять полноту трагедии, давайте поближе познакомимся и узнаем характеры гидроксида натрия и соляной кислоты.
Гидроксид натрия
Химическая формула — NaOH. Является одной из самых распространенных щелочей, известен также как каустическая сода.
Физические свойства
Твердый белый или чуть желтоватый порошок. Гигроскопичен, разъедает многие материалы и органические вещества: бумагу, кожу и даже некоторые металлы, растворяется в воде, этиловом и метиловом спиртах.
Химические свойства
Это сильное химическое основание, взаимодействует с:
- кислотами;
- амфотерными оксидами;
- амфотерными гидроксидами;
- солями в растворе;
- неметаллами;
- галогенами;
- металлами;
- эфирами, амидами и алкилгалогенидами;
- многоатомными спиртами.
Области применения
Гидроксид натрия используется в самых различных отраслях:
- в химической промышленности;
- при нефтепереработке;
- в целлюлозно-бумажной промышленности;
- для устранения засора в трубах;
- в гражданской обороне (нейтрализующее вещество);
- в пищевой промышленности: для очистки овощей и фруктов от корочки; в производстве шоколада и какао; для размягчения маслин и окрашивания их в темный цвет;
- в косметологии (для удаления ороговевших участков кожи);
- в быту.
Теперь познакомимся поближе с соляной кислотой.
Соляная кислота
Химическая формула — HCl. Сильная минеральная одноосновная бескислородная кислота.
Физические свойства
Бесцветная прозрачная едкая жидкость, дымящаяся на воздухе. Максимальная концентрация при 200 °С равна 38%, плотность такого раствора — 1,19 г/см³. Если высококонцентрированная кислота вызывает сильные ожоги кожи, слизистых оболочек и глаз, а вот в концентрации около 0,5 % она присутствует в желудке человека.
Химические свойства
Это сильная кислота, взаимодействует с:
• металлами; • гидроксидами металлов; • оксидами металлов; • солями металлов; • сильными окислителями; • аммиаком.
Качественная реакция на соляную кислоту и ее соли – взаимодействие с нитратом серебра.
Область применения
Соляная кислота используется в:
- в гидрометаллургии и гальванопластике;
- в химической промышленности;
- в пищевой промышленности (пищевая добавка Е507);
- в медицине (при пониженной кислотности в желудке).
И вот решил Химик подружить два непримиримых рода и повенчать влюбленных: сделать всё, чтоб состоялась реакция гидроксида натрия с соляной кислотой. В свидетели с невестой-кислотой пошел индикатор Фенолфталеин. Как только сбудется реакция с гидроксидом, бесцветный индикатор от радости станет малиновым. Несмотря на то что агрессивными были гидроксид натрия и соляная кислота, какая реакция получилась хорошая!
Напишем уравнение этой реакции:
HCl + NaOH = NaCl + H₂O + Q
Соляная кислота и гидроксид натрия> взаимодействуют, в результате чего образуются соль и вода и выделяется тепло.
Как видим, в результате взаимодействия двух агрессивнейших соединений получилась поваренная соль и вода — безобиднейшие и даже полезные для человека соединения. Примирились-таки два враждующих рода и перестали быть злыми и опасными.
А чтобы оценить по достоинству продукты реакции, давайте сядем в ракету и устремимся в космос. Взгляните на нашу Землю со стороны. Не зря ее называют голубой планетой, ведь 71% ее поверхности занимают моря и океаны, то есть вода, один из продуктов нашей реакции. Хотя отметим, справедливости ради, что только 1% от этого количества пригоден к употреблению.
А теперь заглянем в самый лучший ресторан, какой — вы решите сами. Не ограничивайте себя в фантазиях, ведь в пределах нашей истории возможно всё! Давайте пройдем на кухню и спросим шеф-повара, без каких двух продуктов он не смог бы обойтись. И поверьте, он назовет не икру, трюфели или пармезан — он выберет соль и воду, поскольку без этих простых компонентов не приготовишь ни одно блюдо.
Наши продукты реакции входят в состав соединения, которое вы найдете и дома в супе или рассоле, и в морской воде. Об этом соединении поет ансамбль песни и пляски Черноморского флота «Эх! Соленая вода, ветер на просторе, полюбили навсегда голубое море!» А теперь присмотримся повнимательней и определим, какая же это реакция гидроксида натрия и соляной кислоты с точки зрения классификации химических реакций.
Определение вида химической реакции соляной кислоты с гидроксидом натрия.
1. По числу и состоянию исходных и образующихся веществ, это реакция обмена.
Другими словами, количество веществ, вступивших в реакцию, равно количеству веществ, получившихся в результате. Просто произошел обмен ионами. Чтобы увидеть это, напишем уравнение реакции в ионном виде:
H⁺ + Cl⁻ + Na⁺ + OH⁻ = Na⁺+Cl⁻ + H₂O
Следуя сюжету нашей повести, жених с невестой обменялись своим личным имуществом: бери, мол, мне для тебя ничего не жалко. Узнать больше об их «приданном» вы можете здесь.
2. По типу взаимодействующих веществ, это реакция нейтрализации:
3. По агрегатному состоянию веществ, эта реакция является гомогенной.
Вещества, вступающие в реакцию, находятся в одинаковом агрегатном состоянии — в растворе.
4. По направлению протекания реакции, она необратимая.
Реакция протекает до конца, то есть до полного расхода реагирующих веществ.
5. По тепловому эффекту — экзотермическая. Другими словами, церемония венчания прошла в теплой атмосфере. Реакция сопровождается тепловым эффектом, выделяется 57,3 кДж тепловой энергии.
6. Реакция не является окислительно-восстановительной: степени окисления атомов в ходе реакции не изменились.
H⁺Cl⁻ + Na⁺O₂⁻H⁺ = Na⁺Cl⁻ + H₂⁺ O₂⁻
Подведем итоги. У нашей любовной истории счастливый финал: любящие сердца из двух непримиримых семейств воссоединились.
Взаимодействовали агрессивные гидроксид натрия, соляная кислота, реакция же в результате дала нам очень полезные продукты, воспетые в искусстве.
Какая всё-таки замечательная наука − химия. Благодаря реакции кислоты со щелочью мы смогли изменить финал самой печальной трагедии и превратить ее в счастливый роман!
HCL+ NaOH
Ионное и молекулярное уравнения
Молекулярное: HCL + NaOH = NaCl + H2O
Полное ионное: H(+) + CL(-) + Na(+) + OH(-) = Na(+) + CL(-) + H2O
Сокращенное ионное: H(+) + OH(-) = H2O
Если ответ по предмету Химия отсутствует или он оказался неправильным, то попробуй воспользоваться поиском других ответов во всей базе сайта.
http://melscience.com/RU-ru/articles/reakciya-gidroksida-natriya-s-solyanoj-kislotoj/
http://zubrit.com/himiya/zu808559.html
