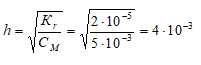Как правильно написать уравнения гидролиза и рассчитать константу и степень гидролиза соли
Молекулярная и ионная формы уравнений реакций гидролиза
Задача 21.
Напишите в молекулярной и ионной форме уравнения реакций гидролиза следующих солей: а) сульфида калия; б) сульфата меди (ⅠⅠ); в) совместного гидролиза хлорида алюминия и ацетата калия. Константа гидролиза соли.
Решение:
а) Гидролиз сульфида калия:
K2S + H2O = KHS + KOH — (молекулярная форма);
S 2– + HOH = HS – + OH – — (ионная форма).
б) Гидролиз сульфата меди (ⅠⅠ):
Cu 2+ + HOH = CuOH + + H + — (ионная форма).
в) Совместный гидролиз хлорида алюминия и ацетата калия:
AlCl3 + 3CH3COOK + 3H2O = Al(OH)3↓ + 3CH3COOH + 3KCl — (молекулярная форма);
Al 3+ + 3CH3COO – + 3HOH = Al(OH)3↓ + 3CH3COOH — (ионная форма).
Определение степени гидролиза и рН раствора цианида калия
Задача 22.
Определите степень гидролиза и pH раствора цианида калия с молярной концентрацией 0,005 моль/л.
Решение:
Цианид калия – соль, образованная сильным основанием КОН и слабой кислотой HCN, которая в водном растворе гидролизуется по аниону.
KCN + HOH ⇔ KOH + HCN
CN – + HOH ⇔ HCN + OH –
Таким образом, при гидролизе этой соли в растворе ее будет избыток ионов OH-, что придает раствору щелочную реакцию
(pH > 7 – среда щелочная).
Константа гидролиза соли, образованной слабой кислотой и сильным основанием определяется по формуле:
Kw = 1 . 10 -14 – ионное произведение воды.
KD(HCN) = 5 . 10 -10 – константа диссоциации циановодородной кислоты
Константа гидролиза цианида калия равна:
Kr(KCN) = Kw/KD(HCN) = (1 . 10 -14 )/(5 . 10 -10 ) = 2 . 10 -5 .
Находим степень гидролиза цианида калия, получим:
Рассчитаем молярную концентрацию ионов OH? в растворе, получим:
[OH – ] = h . СM(KCN) = (4 . 10 -3 ) . 0,005 = 2 . 10 -5 моль/л.
Находим гидроксильный показатель, получим:
рОН = — lg[OH – ] = – lg2 . 10 -5 = 5 — lg2 = 5 — 0,30 = 4,7.
Находим водородный показатель, получим
Гидролиз сульфида калия
K2S — соль образованная сильным основанием и слабой кислотой, поэтому реакция гидролиза протекает по аниону.
Первая стадия (ступень) гидролиза
Молекулярное уравнение
K2S + HOH ⇄ KHS + KOH
Полное ионное уравнение
2K + + S 2- + HOH ⇄ K + + HS — + K + + OH —
Сокращенное (краткое) ионное уравнение
S 2- + HOH ⇄ HS — + OH —
Вторая стадия (ступень) гидролиза
Молекулярное уравнение
KHS + HOH ⇄ H2S + KOH
Полное ионное уравнение
K + + HS — + HOH ⇄ H2S + K + + OH —
Сокращенное (краткое) ионное уравнение
HS — + HOH ⇄ H2S + OH —
Среда и pH раствора сульфида калия
В результате гидролиза образовались гидроксид-ионы (OH — ), поэтому раствор имеет щелочную среду (pH > 7).
Написать подробный Гидролиз солей. ХИМИЯ
Нужно молекулярную и ионную форму.
Сульфид K2S – соль, образованная сильным основанием КОН и слабой кислотой H2S, и в водном растворе подвергнется гидролизу по аниону.
K2S + НОН ↔ KOH + КНS – первая ступень гидролиза
S(2-) + HOH ↔ НS(-) + OH(-) (pH > 7 – среда щелочная)
При нормальных условиях процесс гидролиза сульфида калия K2S протекает по первой ступени и является обратимым процессом. В растворе устанавливается равновесие.
При нагревании процесс гидролиза сульфида калия идет по второй ступени. Гидролиз сульфида калия по второй ступени – необратимый процесс, протекающий с выделением сероводорода H2S, в растворе остается только гидроксид калия.
КНS + НОН → KOH + Н2S↑ — вторая ступень гидролиза
НS(-) + НОН → OH(-) + Н2S↑(pH > 7 – среда щелочная)
Суммарно
K2S + 2НОН → Н2S↑ + 2KOH
S(2-) + 2HOH → Н2S↑ + 2OH(-) (pH > 7 – среда щелочная)
Хлорид цинка ZnCl2 – соль, образованная слабым основанием Zn(OH)2 и сильной кислотой. Гидролиз протекает по катиону.
ZnCl2 + НОН ↔ ZnОНCl + НCl – первая ступень гидролиза
Zn(2+) + НОН ↔ ZnОН (+) + Н (+) (pH 7 – среда щелочная)
К2НРО4 + НОН ↔ KOH + КН2РО4 – вторая ступень гидролиза
НРО4(2-) + НОН ↔ Н2РО4(-) + OH(-) (pH > 7 – среда щелочная)
По третьей ступени гидролиз протекает при нагревании
КН2РО4 + НОН ↔ KOH + Н3РО4 – третья ступень гидролиза
Н2РО4(-)+ НОН ↔ Н3РО4 + OH(-) (pH > 7 – среда щелочная)
Суммарно
K3РО4 + 3НОН ↔ 3KOH + Н3РО4
РО4(3-) + 3HOH ↔ Н3РО4 + 3OH(-) (pH > 7 – среда щелочная)
http://chemer.ru/services/hydrolysis/salts/K2S
http://sprashivalka.com/tqa/q/23514498