Диссоциация воды
Химически чистая вода обладает хотя и ничтожной, но измеримой электропроводностью, так как вода в незначительной степени диссоциирует на ионы. Так при комнатной температуре лишь примерно одна из 10 8 молекул воды находится в диссоциированной форме. Процесс электролитической диссоциации воды возможен благодаря достаточно высокой полярности связей О-Н и наличию между молекулами воды системы водородных связей. Уравнение диссоциации воды записывается так:
где H3O + — катион гидроксония водорода.
Уравнение диссоциации воды можно записать в более простой форме:
Присутствие в воде ионов водорода и гидроксида придают ей специфические свойства амфолита, т.е. способность выполнять функции слабой кислоты и слабого основания. Константа диссоциации воды при температуре 22 0 С:
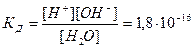
где [H + ] и [OH — ] – равновесные концентрации в г-ион/л соответственно катионов водорода и гидроксо-анионов, а [H2O] – равновесная концентрация воды в моль/л. Учитывая, что степень диссоциации воды чрезвычайно мала, равновесную концентрацию недиссоциированных молекул воды вполне можно приравнять к общему количеству воды, заключающемуся в 1 л ее:
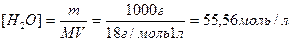
Теперь выражение (1) можно записать в следующем виде:
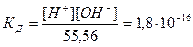
отсюда [H + ] [OH — ] = (1,8 10 -16 ) 55,56 = 10 -14 г-ион 2 /л 2 .
Произведение концентраций ионов водорода и гидроксо-ионов является константой не только для воды, но и для водных растворов солей, кислот и щелочей. Эта величина называется ионным произведением водыили константой воды. Следовательно: КН2О = [H + ][OH — ] = 10 -14 г-ион 2 /л 2 .
Для нейтральных сред [H + ] = [OH — ] = 10 -7 г-ион/л. В кислых средах [H + ] > [OH — ], а в щелочных [H + ] — ]. При этом в любых средах произведение концентраций ионов водорода и гидроксо-ионов при данной температуре остается постоянным и равным 10 -14 г-ион 2 /л 2 . Таким образом, пользуясь ионным произведением воды, любую реакцию среды (нейтральную, кислую или щелочную) можно количественно выразить при помощи концентрации водородных ионов.
1.2. Водородный показатель – рН
Для количественной характеристики реакции среды обычно приводят не концентрации водородных ионов, а применяют некоторый условный показатель, обозначаемый через рН и называемый водородным показателем.Он представляет собой отрицательный десятичный логарифм концентрации катионов водорода рН = — lg [H + ].
Для нейтральной среды рН = -lg 10 -7 = 7;
для кислотной — рН 7.
Аналогично вводится понятие гидроксильного показателя рОН = — lg [ОH — ].
Определение рН имеет колоссальное значение в технике и, в частности, в строительном деле. Обычно величину рН измеряют при помощи индикаторов — веществ, способных менять свою окраску в зависимости от концентрации ионов водорода. Индикаторами являются слабые кислоты и основания, молекулы и ионы которых окрашены в разный цвет (табл. 1).
| Индикаторы | Реакция среды раствора | ||
| Кислая рН 7 | |||
| Лакмус | Красный | Синий | Синий |
| Фенолфталеин | Бесцветный | Бесцветный | Малиновый |
| Метиловый оранжевый | Розовый | Оранжевый | Желтый |
Однако индикаторы дают не точное определение значения рН, поэтому современные измерения рН производятся при использовании электрохимических методов, точность которых составляет ±0,01 единицы рН.
Пример 1.Вычислить рН раствора, в котором концентрация ионов ОН — равна 1∙10 -9 моль/л.
Решение. Из соотношения рН + рОН = 14 находим, что рН = 14 – рОН. Так как рОН = — lg [ОH — ], то рН = 14 – (-lg 10 -9 ) = 5.
Электролитическая диссоциация
Электролитической диссоциацией называют процесс, в ходе которого молекулы растворенного вещества распадаются на ионы в результате взаимодействия с растворителем (воды). Диссоциация является обратимым процессом.
Диссоциация обуславливает ионную проводимость растворов электролитов. Чем больше молекул вещества распадается на ионы, тем лучше оно проводит электрический ток и является более сильным электролитом.
В общем виде процесс электролитической диссоциации можно представить так:
KA ⇄ K + (катион) + A — (анион)
Замечу, что сила кислоты определяется способностью отщеплять протон. Чем легче кислота его отщепляет, тем она сильнее.
У HF крайне затруднен процесс диссоциации из-за образования водородных связей между F (самым электроотрицательным элементом) одной молекулы и H другой молекулы.
Ступени диссоциации
Некоторые вещества диссоциируют на ионы не в одну стадию (как NaCl), а ступенчато. Это характерно для многоосновных кислот: H2SO4, H3PO4.
Посмотрите на ступенчатую диссоциацию ортофосфорной кислоты:
Важно заметить, что концентрация ионов на разных ступенях разная. На первых ступенях ионов всегда много, а до последних доходят не все молекулы. Поэтому в растворе ортофосфорной кислоты концентрация дигидрофосфат-анионов будет больше, чем фосфат-анионов.
Для серной кислоты диссоциация будет выглядеть так:
Для средних солей диссоциация чаще всего происходит в одну ступень:
Из одной молекулы ортофосфата натрия образовалось 4 иона.
Из одной молекулы сульфата калия образовалось 3 иона.
Электролиты и неэлектролиты
Химические вещества отличаются друг от друга по способности проводить электрический ток. Исходя из этой способности, вещества делятся на электролиты и неэлектролиты.
Электролиты — жидкие или твердые вещества, в которых присутствуют ионы, способные перемещаться и проводить электрический ток. Связи в их молекулах обычно ионные или ковалентные сильнополярные.
К ним относятся соли, сильные кислоты и щелочи (растворимые основания).
Степень диссоциации сильных электролитов составляет от 0,3 до 1, что означает 30-100% распад молекул, попавших в раствор, на ионы.
Неэлектролиты — вещества недиссоциирующие в растворах на ионы. В молекулах эти веществ связи ковалентные неполярные или слабополярные.
К неэлектролитам относятся многие органические вещества, слабые кислоты, нерастворимые в воде основания и гидроксид аммония.
Степень их диссоциации до 0 до 0.3, то есть в растворе неэлектролита на ионы распадается до 30% молекул. Они плохо или вообще не проводят электрический ток.
Молекулярное, полное и сокращенное ионные уравнения
Молекулярное уравнение представляет собой запись реакции с использованием молекул. Это те уравнения, к которым мы привыкли и которыми наиболее часто пользуемся. Примеры молекулярных уравнений:
Полные ионные уравнения записываются путем разложения молекул на ионы. Запомните, что нельзя раскладывать на ионы:
- Слабые электролиты (в их числе вода)
- Осадки
- Газы
Сокращенное ионное уравнение записывается путем сокращения одинаковых ионов из левой и правой части. Просто, как в математике — остается только то, что сократить нельзя.
© Беллевич Юрий Сергеевич 2018-2022
Данная статья написана Беллевичем Юрием Сергеевичем и является его интеллектуальной собственностью. Копирование, распространение (в том числе путем копирования на другие сайты и ресурсы в Интернете) или любое иное использование информации и объектов без предварительного согласия правообладателя преследуется по закону. Для получения материалов статьи и разрешения их использования, обратитесь, пожалуйста, к Беллевичу Юрию.
Блиц-опрос по теме Электролитическая диссоциация
Диссоциация воды. Водородный показатель. Среды водных растворов электролитов
Вода — слабый амфотерный электролит.
Уравнение ионизации воды с учетом гидратации ионов водорода Н + таково:
Без учета гидратации ионов Н + уравнение диссоциации воды имеет вид:
Как видно из второго уравнения, концентрации ионов водорода Н + и гидроксид-ионов ОН — в воде одинаковы. При 25 о С [Н + ] = [ОН — ] = 10 -7 моль/л.
Произведение концентраций ионов водорода и гидроксид-ионов называется ионным произведением воды (KH2O).
KH2O — величина постоянная, и при температуре 25 о С
В разбавленных водных растворах электролитов, как и в воде, произведение концентраций ионов водорода Н + и гидроксид-ионов ОН — — величина постоянная при данной температуре. Ионное произведение воды дает возможность для любого водного раствора вычислить концентрацию гидроксид-ионов ОН — , если известна концентрация ионов водорода Н + , и наоборот.
Среду любого водного раствора можно охарактеризовать концентрацией ионов водорода Н + или гидроксид-ионов ОН — .
В водных растворах различают три типа сред: нейтральную, щелочную и кислую.
Нейтральная среда — это среда, в которой концентрация ионов водорода равна концентрации гидроксид-ионов:
[Н + ] = [OH — ] = 10 -7 моль/л
Кислая среда — это среда, в которой концентрация ионов водорода больше концентрации гидроксид-ионов:
[Н + ] > [ОН — ], [H+] > 10 -7 моль/л
Щелочная среда — это среда, в которой концентрация ионов водорода меньше концентрации гидроксид-ионов:
[H + ] — ], [H + ] -7 моль/л
Для характеристики сред растворов удобно использовать так называемый водородный показатель рН (пэ-аш).
Водородным показателем рН называется отрицательный десятичный логарифм концентрации ионов водорода: рН = -lg[H + ].
Например, если [H + ] = 10 -3 моль/л, то pН = 3, среда раствора — кислая; если [Н + ] = 10 -12 моль/л, то pН = 12, среда раствора — щелочная:
Чем рН меньше 7, тем больше кислотность раствора. Чем рН больше 7, тем больше щелочность раствора.
Зависимость между концентрацией ионов Н + , величиной рН и средой раствора показана на следующей схеме:
Существуют различные методы измерения рН. Качественно характер среды водных растворов электролитов определяют с помощью индикаторов.
Индикаторами называются вещества, которые обратимо изменяют свой цвет в зависимости от среды растворов, т. е. рН раствора.
На практике применяют индикаторы лакмус, метиловый оранжевый (метилоранж) и фенолфталеин. Они изменяют свою окраску в малом интервале рН: лакмус — в интервале рН от 5,0 до 8,0; метилоранж — от 3,1 до 4,4 и фенолфталеин — от 8,2 до 10,0.
Изменение цвета индикаторов показано на схеме:
Заштрихованные области показывают интервал изменения окраски индикатора.

Кроме указанных выше индикаторов, применяют также универсальный индикатор, который можно использовать для приблизительного определения рН в широком интервале от 0 до 14.
Величина рН имеет большое значение в химических и биологических процессах, так как в зависимости от характера среды эти процессы могут протекать с разными скоростями и в разных направлениях.
Поэтому определение рН растворов очень важно в медицине, науке, технике, сельском хозяйстве. Изменение рН крови или желудочного сока является диагностическим тестом в медицине. Отклонения рН от нормальных, величин даже на 0,01 единицы свидетельствуют о патологических процессах в организме. Постоянство концентраций ионов водорода Н + является одной из важных констант внутренней среды живых организмов.
Так, при нормальной кислотности желудочный сок имеет рН 1,7; рН крови человека равен 7,4; слюны — 6,9. Каждый фермент функционирует при определенном значении рН: каталаза крови при рН 7 пепсин желудочного сока — при рН 1,5—2; и т. д.
http://studarium.ru/article/159
http://al-himik.ru/dissociacija-vody-vodorodnyj-pokazatel-sredy-vodnyh-rastvorov-jelektrolitov/













