Химия NeoChemistry — мы знаем о химии всё
 |  | |||||||||||||||||||||||||||||||||||||
| Задачи по химии (с решениями) | ||||||||||
|---|---|---|---|---|---|---|---|---|---|---|
|
| Химия общая | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|
|
| Химия неорганическая | |||||||||
|---|---|---|---|---|---|---|---|---|---|
|
Начальные концентрации реагирующих веществ были (моль/л): СNО =0,8; СО2 =0,6. Как изменится скорость реакции, если концентрацию кислорода увеличить до 0,9моль/л, а концентрацию оксида азота (II) – до 1,2 моль/л
Решение:
Зависимость скорости реакции от концентраций определяется законом действия масс: при постоянной температуре скорость химической реакции прямо пропорциональна произведению молярных концентраций реагирующих веществ.
V =К [NО]2[О2]
Обозначим скорость реакции до изменения концентраций V1, а после изменения концентраций V2
Тогда V1=К*0,82*0,6
V2 = К*1,22*0,9
изменение скорости (V2/V1) равно:
V2/V1 = (К*1,22*0,9)/ К*0,82*0,6 =1,44*0,9/0,64*0,6=3,4
Ответ: Скорость реакции возрастет в 4 раза.
$ AlexLat $
| 04.11.2013, 00:17 |
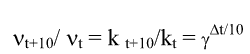
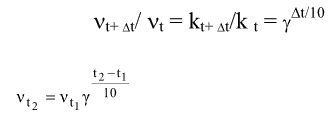 (4.2.3)
(4.2.3)
 Решебник по химии за 11 класс (О.С. Габриелян, 2007 год),
Решебник по химии за 11 класс (О.С. Габриелян, 2007 год),