Напишите уравнения электролитической диссоциации: а) гидроксида кальция; б) хлорида меди(ii); в) серной кислоты; г) сульфата железа(iii); д) нитрата калия
Ваш ответ
решение вопроса
Похожие вопросы
- Все категории
- экономические 43,296
- гуманитарные 33,622
- юридические 17,900
- школьный раздел 607,211
- разное 16,830
Популярное на сайте:
Как быстро выучить стихотворение наизусть? Запоминание стихов является стандартным заданием во многих школах.
Как научится читать по диагонали? Скорость чтения зависит от скорости восприятия каждого отдельного слова в тексте.
Как быстро и эффективно исправить почерк? Люди часто предполагают, что каллиграфия и почерк являются синонимами, но это не так.
Как научится говорить грамотно и правильно? Общение на хорошем, уверенном и естественном русском языке является достижимой целью.
Гидролиз хлорида меди. Расчет концентрации ионов кальция
Страницы работы
Содержание работы
1. Какая из перечисленных солей подвергается гидролизу: CuCl2, Na2SO4, Са(NОз)2? Рассчитать рН раствора, если концентрация этой соли равна 0.5 моль/л, а константа диссоциации основания равна Кь2 = 2.19 * 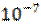
Сульфат натрия Na2SO4 и нитрат кальция Са(NОз)2 – соли сильных оснований и сильных кислот, поэтому гидролизу не подвергаются.
Гидролизоваться будет хлорид меди (2) CuCl2 – соль слабого основания (Cu(OH)2) и сильной кислоты (HCl). Гидролиз протекает по катиону, преимущественно по I ступени. Среда кислая.
Диссоциация хлорида меди (2):
Гидролиз хлорида меди по первой ступени:
Cu 2+ + H2O ↔ CuOH + + H +
Для солей, гидролизующихся по катиону, константа гидролиза Кг равна:
Кг = Kw/Kb, где Kw = 10 -14 – ионное произведение воды, Кb – константа диссоциации основания.
Т.к. гидролиз хлорида меди (2) протекает преимущественно по первой ступени, то для расчёта используем константу гидролиза по первой ступени, которая равна: Кг(1) = Kw/Kb(2)
Итак, рН для данного раствора равен:
2. Определите рН 0.1 М раствора плавиковой кислоты (HF), константа диссоциации которой равна Ка = 6.67*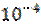
Плавиковая кислота – слабый электролит. Для слабых кислот концентрация водородных ионов в растворе рассчитывается по формуле:
рН = — lg[H + ] = — lg 8,17*10 -3 = 2,09
3. В какую сторону сместится равновесие реакции 2СО + O2 2СO2 а) при увеличении температуры (∆Н ; .
Диссоциация карбоната кальция:
Согласно уравнению диссоциации соли,
[Ca 2+ ] = √ПР = √(4,4*10 -9 ) = 6,63*10 -5 (моль/л)
Переведём концентрацию ионов кальция в г/л:
С = М*МВ = 6,63*10 -5 моль/л * 40 г/моль = 2,652*10 -3 г/л
(С – концентрация, выраженная в граммах растворённого вещества на литр раствора, М – молярная концентрация раствора, МВ – молярная масса катиона кальция)
Напишите уравнение диссоциации хлорида меди
Вопрос по химии:
Напишите пожалуйста ответ. Напишите уравнения электролитической диссоциации: а)гидроксид кальция;б)хлорида меди(2);в) серной кислоты;г)сульфата железа(3);д)нитрата калия.
Трудности с пониманием предмета? Готовишься к экзаменам, ОГЭ или ЕГЭ?
Воспользуйся формой подбора репетитора и занимайся онлайн. Пробный урок — бесплатно!
Ответы и объяснения 2
Ca(OH)2 ⇔Ca(2+) + 2OH(-)
CuCl2 ⇔Cu(2+) + 2Cl(-)
H2SO4 ⇔2H(+) + SO4(2-)
Fe2(SO4)3 ⇔2Fe(3+) + 3SO4(2-)
KNO3 ⇔K(+) + NO3(-)
А) Ca(OH)₂ → Ca²⁺ + 2OH⁻
б) CuCl₂ → Cu²⁺ + 2Cl⁻
в) H₂SO₄ → 2H⁺ + SO₄²⁻
г) Fe₂(SO₄)₃ → 2Fe³⁺ + 3SO₄²⁻
д) KNO₃ → K⁺ + NO₃⁻
Знаете ответ? Поделитесь им!
Как написать хороший ответ?
Чтобы добавить хороший ответ необходимо:
- Отвечать достоверно на те вопросы, на которые знаете правильный ответ;
- Писать подробно, чтобы ответ был исчерпывающий и не побуждал на дополнительные вопросы к нему;
- Писать без грамматических, орфографических и пунктуационных ошибок.
Этого делать не стоит:
- Копировать ответы со сторонних ресурсов. Хорошо ценятся уникальные и личные объяснения;
- Отвечать не по сути: «Подумай сам(а)», «Легкотня», «Не знаю» и так далее;
- Использовать мат — это неуважительно по отношению к пользователям;
- Писать в ВЕРХНЕМ РЕГИСТРЕ.
Есть сомнения?
Не нашли подходящего ответа на вопрос или ответ отсутствует? Воспользуйтесь поиском по сайту, чтобы найти все ответы на похожие вопросы в разделе Химия.
Трудности с домашними заданиями? Не стесняйтесь попросить о помощи — смело задавайте вопросы!
Химия — одна из важнейших и обширных областей естествознания, наука о веществах, их составе и строении, их свойствах, зависящих от состава и строения, их превращениях, ведущих к изменению состава — химических реакциях, а также о законах и закономерностях, которым эти превращения подчиняются.
http://vunivere.ru/work59419
http://online-otvet.ru/himia/5cea7cc696f4e19a290ca305

