Составьте ионно-молекулярные и молекулярные уравнения гидролиза солей: нитрат меди (II), сульфид калия
Решение:
Нитрат меди (II) Cu(NO3)2– соль слабого двухкислотного основания и сильной кислоты. Катионы слабого основания Cu 2+ связывают гидроксид ионы из воды. Гидролиз такой соли идет по катиону:
Сокращенное ионно-молекулярное уравнение гидролиза:
Cu 2+ + H2O 
полное ионно-молекулярное уравнение:
Cu 2+ + 2NO3 — + H2O 
Cu(NO3)2+ H2O 
В растворе накапливаются катионы водорода, которые создают кислую реакцию среды (pH 2– связывают ионы водорода из воды, образуя анионы кислой соли HS – . Соль гидролизуется по аниону.
Сокращенное ионно-молекулярное уравнение:
S 2– + H2O 
полное ионно-молекулярное уравнение:
2К + + S 2– + H2O 
К2S + H2O 
Появление избыточного количества ионов OH – обусловливает щелочную реакцию среды (pH > 7).
22. Какие из солей Al2(SO4)3, K2S, Pb(NO3)2, KCl подвергаются гидролизу? Составьте ионно-молекулярные и молекулярные уравнения гидролиза соответствующих солей.
Решение:
Сульфат алюминия Al2(SO4)3– соль слабого трехкислотного основания и сильной кислоты. Гидролиз такой соли идет по катиону слабого основания с образованием катионов основной соли AlOH 2+ .
Сокращенное ионно-молекулярное уравнение гидролиза:
Al 3+ + H2O 
полное ионно-молекулярное уравнение:
2Al 3+ + 3SO4 2- + 2H2O 
Al2(SO4)3 + 2H2O 
В растворе накапливаются катионы водорода, которые создают кислую реакцию среды (pH 2– связывают ионы водорода из воды, образуя анионы кислой соли HS – . Соль гидролизуется по аниону.
Сокращенное ионно-молекулярное уравнение:
S 2– + H2O 
полное ионно-молекулярное уравнение:
2К + + S 2– + H2O 
К2S + H2O 
Появление избыточного количества ионов OH – обусловливает щелочную реакцию среды (pH > 7).
Нитрат свинца (II) Pb(NO3)2– соль слабого двухкислотного основания и сильной кислоты. Катионы слабого основания Pb 2+ связывают гидроксид ионы из воды. Гидролиз такой соли идет по катиону:
Сокращенное ионно-молекулярное уравнение гидролиза:
Pb 2+ + H2O 
полное ионно-молекулярное уравнение:
Pb 2+ + 2NO3 — + H2O 
Pb(NO3)2+ H2O 
В растворе накапливаются катионы водорода, которые создают кислую реакцию среды (pH + и анионы Cl – . Катионы K + не могут связывать анионы OH – , так как KOH – сильный электролит. Анионы Cl – не могут связывать катионы Н + , так как НCl – сильный электролит. Таким образом, можно сделать вывод, что хлорид калия не гидролизуется. Равновесие между ионами и молекулами воды не нарушается, и раствор остается нейтральным, рН равен 7.
Как изменится цвет лакмуса в растворах солей: хлорида натрия, карбоната натрия, хлорида меди (II)? Составьте ионно-молекулярные и молекулярные уравнения гидролиза солей.
Решение:
Хлорид натрия NaCl —соль сильной кислоты и сильного основания. При растворении в воде хлорид натрия диссоциирует на ионы Na + и анионы Cl – . Катионы Na + не могут связывать анионы OH – , так как NaOH – сильный электролит. Анионы Cl – не могут связывать катионы Н + , так как НCl – сильный электролит. Таким образом, можно сделать вывод, что хлорид натрия не гидролизуется. Равновесие между ионами и молекулами воды не нарушается, и раствор остается нейтральным, рН равен 7. Цвет лакмуса не изменяется.
Карбонат натрия Na2CO3 – соль двухосновной слабой кислоты и сильного основания. Анионы слабой кислоты CO3 2– связывают ионы водорода из воды, образуя анионы кислой соли HCO3 — . Соль гидролизуется по аниону.
Сокращенное ионно-молекулярное уравнение:
CO3 2– + H2O 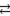
полное ионно-молекулярное уравнение:
2Na + + CO3 2– + H2O 
Na2CO3 + H2O 
Появление избыточного количества ионов OH – обусловливает щелочную реакцию среды (pH > 7). Цвет лакмуса меняется с фиолетового на синий.
Хлорид меди (II) CuCl2– соль слабого двукислотного основания и сильной кислоты. Гидролиз такой соли идет по катиону слабого основания с образованием катионов основной соли CoOH + .
Сокращенное ионно-молекулярное уравнение гидролиза:
Cu 2+ + H2O 
полное ионно-молекулярное уравнение:
Cu 2+ + 2Cl — + H2O 
CuCl2+ 2H2O 
В растворе накапливаются катионы водорода, которые создают кислую реакцию среды (pH
Гидролиз нитрата меди (II)
Cu(NO3)2 — соль образованная слабым основанием и сильной кислотой, поэтому реакция гидролиза протекает по катиону.
Первая стадия (ступень) гидролиза
Полное ионное уравнение
Cu 2+ + 2NO3 — + HOH ⇄ CuOH + + NO3 — + H + + NO3 —
Сокращенное (краткое) ионное уравнение
Cu 2+ + HOH ⇄ CuOH + + H +
Вторая стадия (ступень) гидролиза
Полное ионное уравнение
CuOH + + NO3 — + HOH ⇄ Cu(OH)2 + H + + NO3 —
Сокращенное (краткое) ионное уравнение
CuOH + + HOH ⇄ Cu(OH)2 + H +
Среда и pH раствора нитрата меди (II)
В результате гидролиза образовались ионы водорода (H + ), поэтому раствор имеет кислую среду (pH
Составить схему гидролиза нитрата меди?
Химия | 10 — 11 классы
Составить схему гидролиза нитрата меди.
Cu(NO3)2 + HOH ⇄ CuOHNO3 + HNO3 молекулярное уровнения
Cu2 + + 2NO3 — + HOH ⇄ CuOH + + NO3 — + H + + NO3 — ионое уровнение
Cu2 + + HOH ⇄ CuOH + + H + краткое ионое уравнение.
ШОКОЛАД?
Напишите уравнения гидролиза солей : карбоната калия, хлорида меди(II) нитрата свинца(II), фосфата натрия.
Укажите, какие из перечисленных солей подвергаются гидролизу при растворении в воде : карбонат натрия, хлорид калия, нитрат меди(II)?
Укажите, какие из перечисленных солей подвергаются гидролизу при растворении в воде : карбонат натрия, хлорид калия, нитрат меди(II).
Укажите, какие из перечисленных солей подвергаются гидролизу при растворении в воде : карбонат натрия, хлорид калия, нитрат меди(II)?
Укажите, какие из перечисленных солей подвергаются гидролизу при растворении в воде : карбонат натрия, хлорид калия, нитрат меди(II).
Напишите уравнения гидролиза солей : карбоната калия, хлорида меди(II) нитрата свинца(II), фосфата натрия?
Напишите уравнения гидролиза солей : карбоната калия, хлорида меди(II) нитрата свинца(II), фосфата натрия.
Пожалуйста напишите уравнения гидролизу солей : карбоната калия, хлорида меди (2), нитрата свинка (2), фосфата натрия?
Пожалуйста напишите уравнения гидролизу солей : карбоната калия, хлорида меди (2), нитрата свинка (2), фосфата натрия.
Составьте схему электролиза водного раствора нитрата меди (II)?
Составьте схему электролиза водного раствора нитрата меди (II).
Запишите молекулярное и ионные уравнения гидролиза и укажите окраску лакмуса в растворе : нитрата меди(||)?
Запишите молекулярное и ионные уравнения гидролиза и укажите окраску лакмуса в растворе : нитрата меди(||).
Напишите уравнение реакций гидролиза сульфата меди и нитрата магния?
Напишите уравнение реакций гидролиза сульфата меди и нитрата магния.
Химики помогите : ) Нужно составить молекулярные уравнения химических реакций, позволяющих осуществить превращения по схеме : гидроксид меди(2)⇒нитрат гидроксидмеди(2)⇒нитрат меди(2)⇒гидроксид меди(2)?
Химики помогите : ) Нужно составить молекулярные уравнения химических реакций, позволяющих осуществить превращения по схеме : гидроксид меди(2)⇒нитрат гидроксидмеди(2)⇒нитрат меди(2)⇒гидроксид меди(2)⇒оксид меди(2)⇒хлорид меди(2).
Написать гидролиз соли — нитрат меди (II)?
Написать гидролиз соли — нитрат меди (II).
Перед вами страница с вопросом Составить схему гидролиза нитрата меди?, который относится к категории Химия. Уровень сложности соответствует учебной программе для учащихся 10 — 11 классов. Здесь вы найдете не только правильный ответ, но и сможете ознакомиться с вариантами пользователей, а также обсудить тему и выбрать подходящую версию. Если среди найденных ответов не окажется варианта, полностью раскрывающего тему, воспользуйтесь «умным поиском», который откроет все похожие ответы, или создайте собственный вопрос, нажав кнопку в верхней части страницы.
Структурная формула во вложении.
Если элемент стоит один (простое вещество, например Cl), то его степень окисления = 0 — — — — — — — — — — — По таблице можно найти только для первой колонки : Если элемент стоит в первой колонке элементов, то его степень окисления такая же, как у вод..
Степень окисления атомов ВНЕ химического соединения равна нулю. Например, O2 ( кислород) если он не находится в соединении, то его степень окисления будет равна нулю. НО у некоторых элементов есть их постоянная степень окисления. Например, вода. ..
А) 2HCl + Ca — CaCl2 + H2 2HCl + ZnO — ZnCl2 + H2O б) 3HCl + Cr(OH)3 — CrCl3 + 3H2O 2HCl + Na2S — 2NaCl + H2S в) 2HCl + MgCO3 — H2O + CO2 ↑ + MgCl2 2AlCl3 + 3Pb(NO3)2 — 2Al(NO3)3 + 3PbCl2.
Найдем относительную молекулярную массу бихромата аммония : Mr((NH4)2Cr2O7) = 2Ar(N) + 8Ar(H) + 2Ar(Cr) + 7Ar(O) Mr((NH4)2Cr2O7) = 2 * 14 + 8 * 1 + 2 * 52 + 7 * 16 = 28 + 8 + 104 + 112 = 252 w(Cr) = 2Ar(Cr) / Mr((NH4)2Cr2O7) * 100% w(Cr) = 104 / 252 ..
1) N, P, As вниз по группе увеличивается радиус атома элемента.
N = 0. 4 (моль) M(MgCO3) = 24 + 12 + 3 * 16 = 84 (г / моль) m = n * M = 0. 4 * 84 = 33. 6 (г) N = 8. 7 * 10 ^ 23 (молекул) n = N / Na, где Na — число Авагадро = 6. 02 * 10 ^ 23 (молекул / моль) n = 8. 7 * 10 ^ 23 / 6. 02 * 10 ^ 23 = 1. 45 (мо..
Al(OH)3 Al(OH)3 + 3HNO3 = Al(NO3)3 + 3H2O Al(OH)3 + NaOH = Na[Al(OH)4].
1) 3 2) 4 Вот такие пироги.
СuCl2 + 2NaOH = Cu(OH)2 + 2NaCl реакция обмена 3FeO + 2Al = Al2O3 + 3Fe реакция замещения.
http://chemer.ru/services/hydrolysis/salts/Cu(NO3)2
http://himia.my-dict.ru/q/2464143_sostavit-shemu-gidroliza-nitrata-medi/









