Please wait.
We are checking your browser. gomolog.ru
Why do I have to complete a CAPTCHA?
Completing the CAPTCHA proves you are a human and gives you temporary access to the web property.
What can I do to prevent this in the future?
If you are on a personal connection, like at home, you can run an anti-virus scan on your device to make sure it is not infected with malware.
If you are at an office or shared network, you can ask the network administrator to run a scan across the network looking for misconfigured or infected devices.
Another way to prevent getting this page in the future is to use Privacy Pass. You may need to download version 2.0 now from the Chrome Web Store.
Cloudflare Ray ID: 6e099d4dfeb9716f • Your IP : 85.95.188.35 • Performance & security by Cloudflare
Полимеризация акрилонитрила
На способность акрилонитрила к полимеризации впервые обратил внимание ван-дер-Бург. Позднее это свойство было изучено рядом авторов.
Абсолютно чистый акрилонитрил является устойчивым соединением. Он не изменяется даже при длительном нагревании до температуры 150—160° и не окисляется кислородом воздуха. С этим свойством связано то обстоятельство, что присутствие воздуха продлевает индукционный период полимеризации, инициированной перекисью. Не совсем чистый мономер полимеризуется уже в процессе хранения, а еще быстрее при нагревании. Быстрая полимеризация происходит либо под влиянием ультрафиолетового света, особенно в присутствии α-диоксосоединений, например диацетила, либо под влиянием соединений, которые разлагаются на радикалы по неполярному механизму. Из таких соединений в качестве инициаторов полимеризации были использованы полиалкилированные дифенилэтаны, неорганические и органические перекиси, N-нитрозоацетанилид и его производные, азоизобутиронитрил, фтороборат п-бромбензолдиазония и диазоаминобензол. Лучше всего изучена полимеризация, вызываемая перекисью дибензоила. Если эту реакцию проводят без разбавителя, то ее скорость зависит главным образом от количества катализатора и от температуры. С ростом температуры скорость полимеризации возрастает. При концентрации перекиси дибензоила 1% и температуре 30° полимеризация почти не протекает; при температуре 100° реакция заканчивается за 20 мин. Индукционный период весьма мал, однако интенсивность полимеризации резко падает по мере расхода инициатора. При полимеризации больших количеств остается до 40% непрореагировавшего мономера. При концентрации свыше 1% перекись дибензоила вызывает необычайно бурную полимеризацию, часто оканчивающуюся взрывом. В процессе полимеризации, инициированной перекисью дибензоила, всегда выделяется цианистый водород, образующийся, очевидно, в результате побочной реакции:
Если полимеризацию проводят в растворе, то индукционный период удлиняется и процесс протекает более гладко. Менее активными инициаторами являются перекись тетралина и диазоаминобензол. При использовании последнего скорость полимеризации гораздо меньше, но проходит она также более гладко, поскольку концентрация радикалов, образующихся неполярным разложением, хотя и ниже, но она поддерживается на постоянном уровне.
Механизм полимеризации акрилонитрила и строение полимера недостаточно ясны, хотя полиакрилонитрилу обычно и приписывают структуру:
Это следует из того, что при окислении полиакрилонитрила в полиакриловую кислоту путем нагревания с концентрированной щелочью количество выделяющегося аммиака, как правило, бывает меньше расчетного (94—95% от теоретического); по-видимому, какое-то количество нитрильных групп принимает участие в образовании линейной макромолекулы полимера.
Полимеризацию можно вызвать не только свободными радикалами, но также и основаниями, а лучше всего металлорганическими соединениями, например реактивами Гриньяра. Такая анионоидная полимеризация акрилонитрила ведет к образованию полимера с количественным выходом даже при температуре –10°. В противоположность этому акрилонитрил нельзя полимеризовать, действуя металлическим натрием даже при температуре 90°.
В результате полимеризации акрилонитрила, проводимой как в мономере, так и в обычных органических растворителях, всегда получают нерастворимый полимер независимо от условий. Полиакрилонитрил образует вязкие растворы только при растворении в диметилформамиде, тетраметилдиамиде щавелевой кислоты, 1,2-дицианэтане, диметилцианамиде и в растворах некоторых солей, особенно бромистого лития, роданистого натрия или хлористого цинка. Эти растворы применяют при производстве синтетического волокна, получившего название «орлон». Полиакрилонитрил представляет собой бесцветную или слегка желтоватую аморфную массу, легко растирающуюся в порошок. Средняя степень полимеризации составляет минимум 270, молекулярный вес обычных полимеров колеблется в широком интервале от 15 000 до 250 000. Полимер не термопластичен, при температуре 300—350° он частично превращается, не деполимеризуясь, с образованием летучих точно не идентифицированных основных соединений. При щелочном и кислом гидролизе полимер превращается в полиакриловую кислоту. По описанным свойствам полиакрилонитрил диаметрально противоположен полиметакрилонитрилу (см. ниже).
На практике полимеризацию проводят в растворе или, чаще всего, в водной эмульсии в присутствии эмульгаторов. Точно таким же образом получают смешанные полимеры акрилонитрила с мономерами, например со стиролом и его замещенными, с хлористым винилом, с винилацетатом, с эфирами акриловой кислоты и главным образом с бутадиеном. Акрилонитрил придает смешанным полимерам высокую стойкость по отношению к органическим жидкостям, особенно к бензину, маслам и др. Вследствие этого сополимеры акрилонитрила имеют большее значение, нежели сам полиакрилонитрил. Из них наиболее известным и самым распространенным является смешанный полимер акрилонитрила с бутадиеном под названием «пербунан» или «буна-Н». Сополимер с хлористым винилом известен под названием «винилон».
Химия, Биология, подготовка к ГИА и ЕГЭ
Что же такое полимеризация?
и связанные с ними процессы, ведь, оказывается, почти весь наш мир — полимерный.
Автор статьи — Саид Лутфуллин
Полимеризация – это реакция образования высокомолекулярного соединения из низкомолекулярного. Высокомолекулярное соединение (полимер) – это вещество с большой молекулярной массой, состоящее из многократно повторяющихся сегментов (структурных звеньев), связанных между собой.
Где мы в повседневной жизни можем встретить полимеры?
Везде. Куда бы вы ни поглядели. Полимеры глубоко связались с нашей жизнью, собственно и образовали ее.
Ткани (как синтетические, так и натуральные), пластмассы, резина образованны полимерами. Кроме того, мы сами – тоже состоим из полимеров.
Вспомним определение жизни по Энгельсу:
«Жизнь есть способ существования белковых тел…».
Белки – это природные биополимеры, так же к биополимерам относятся нуклеиновые кислоты и полисахариды.
Какие вещества могут вступать в реакцию полимеризации?
Ответ простой: вещества, содержащие кратные (двойные, тройные) связи.
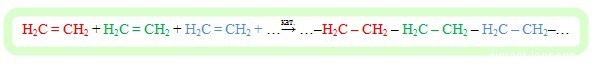
Давайте рассмотрим первое уравнение полимеризации — схему реакции образования полиэтилена (из него делают пакеты, бутылки, упаковочную пленку и многое другое):
Как мы видим, π-связь рвется, и атомы углерода одной молекулы связываются с атомами углерода соседних молекул. Так образуется длинная цепь полимера. Так как длина полимера может достигать нескольких сотен структурных звеньев, точное число которых, предсказать невозможно, так как в разных молекулах она различная и чтобы не записывать целиком эту цепь, реакцию полимеризации записывают следующим образом:
Где, n – число структурных звеньев в молекуле.
Исходное низкомолекулярное вещество, вступающее в реакцию полимеризации, называется мономер.
Не следует путать структурное звено с мономером.
Мономер и структурное звено имеют одинаковый качественный и количественный состав, но разное химическое строение (отличаются друг от друга количеством кратных связей).
Уравнения полимеризации:
Реакции получения наиболее часто встречающихся полимеров:
- Образование изопренового каучука (природный каучук тоже изопреновый, но строго цис- строения) из 2-метилбутадиена-1,3 (изопрена):
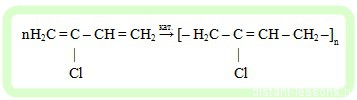
- Образование хлорпренового каучука (синтетический каучук) из 2-хлорбутадиена-1,3 (хлорпрена):
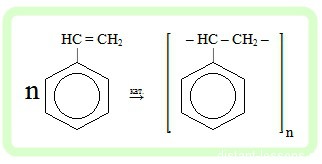
- Образование полистирола (пластмасса) из винилбензола (стирола):
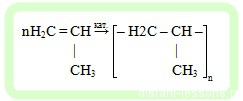
- Образование полипропилена из пропена (пропилена):
Каучуки – это группа полимеров, объединенные общими качествами (эластичность, электроизоляция и т.д.), сырье для производства резины. Раньше для этого использовали натуральный каучук из сока так называемых каучуконосных растений. Позже стали изготавливать искусственные каучуки.
В СССР в 1926 году был объявлен конкурс на лучший способ получения синтетического каучука. Конкурс выиграл Лебедев С.В.
Его метод заключался в следующем:
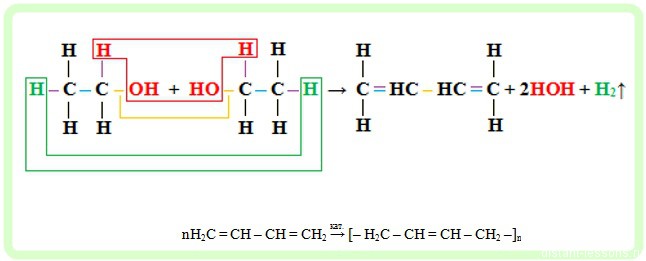
из этилового спирта производили бутадиен-1,3. Этиловый спирт получали брожением из растительного сырья, которого в СССР было предостаточно, это делало производство дешевле. Бутадиен-1,3 после полимеризации образовывал синтетический каучук:
Чтобы превратить каучук в резину, его подвергают вулканизации.
Вулканизация – это процесс сшивания нитей полимера-каучука в единую сеть, вследствие чего улучшается эластичность, прочность, устойчивость к органическим растворителям .
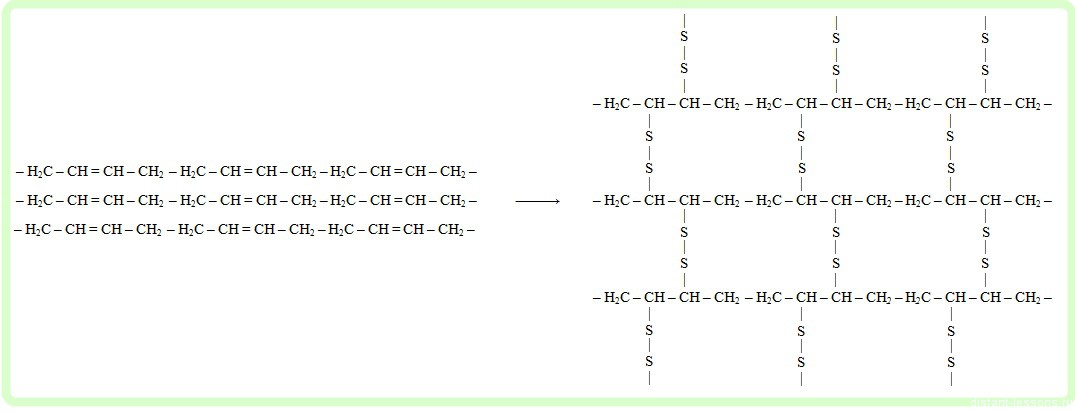
На схеме ни же показан процесс вулканизации бутадиеновго каучука, путем образования между молекулами полимера дисульфидных мостиков:
Следует отличать реакции полимеризации от реакций поликонденсации.
Реакция поликонденсации – это реакця образования высокомолекулярного соединения из низкомолекулярного, при которой выделяется побочный продукт (вода, аммиак, слороводород и др.)
Способность вещества вступать в реакцию поликонденсации обучлавливается у него наличием покрайней мере двух разных функциональных групп .
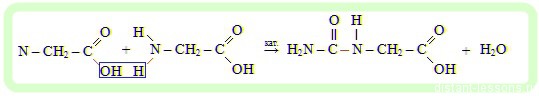
Рассмотрим на примере аминокислот:
Две аминокислоты соединились друг с другом, образовав пептидную связь, с выделением побочного продукта – воды. Если процесс продолжить – присоединять к этой цепи остатки аминокислот – по получим белок. Способность аминокислот вступать в реакцию поликонденсации обуславливает наличие в их строение двух функциональных групп: карбоксильной и аминогруппы. В результате реакции поликонденсации помимо полипептидов (белков), образуются нуклеиновые кислоты и полисахариды.
В погоне за качеством продукции, человек научился создавать такие стойкие полимеры, что они не разлагаются несколько тысяч лет. А иногда при разложении выделяют в окружающую среду опасные вещества. Это большая экологическая проблема. Сейчас открываются пункты переработки пластмасс.
Если мы все вместе будет сдавать туда пластмассовые отходы, то внесем огромный вклад в сохранение нашего общего дома – планеты Земля и ее природы.
http://www.zomber.ru/himiya-monomerov/213_polimerizaciya_akrilonitrila.php
http://distant-lessons.ru/uravneniya-polimerizacii.html