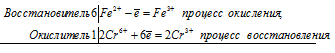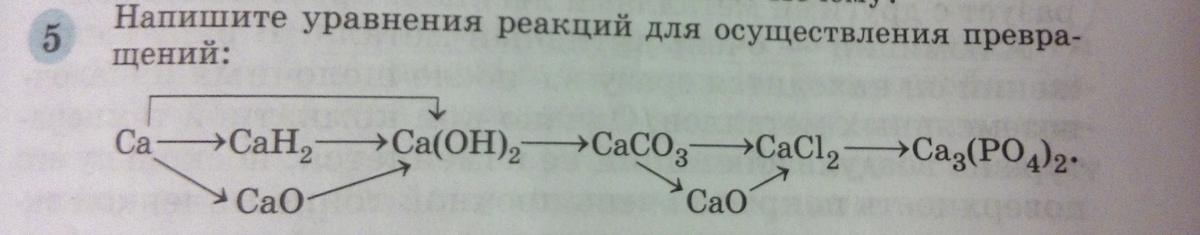5 Напишите уравнения реакций для осуществления превра-щений: Уравнение последней реакции запишите также в ионной форме

задача №5
к главе «Глава 1. Металлы. § 12(12). Бериллий, магний и щелочноземельные металлы».
Выделите её мышкой и нажмите CTRL + ENTER
Большое спасибо всем, кто помогает делать сайт лучше! =)
Нажмите на значок глаза возле рекламного блока, и блоки станут менее заметны. Работает до перезагрузки страницы.
Составление уравнений реакций, которые надо провести для осуществления превращений
Задание 392
Составьте уравнения реакций, которые надо провести для осуществления следующих превращений:
Cu → Cu(NO3)2 → Cu(OH)2 → CuCl2 → [Cu(NH3)4]Cl2
Решение:
а) 3Сu + 8HNO3 (разб.) = 3Сu(NO3)2 + 2NO↑ + 4H2O;
б) Сu(NO3)2 + 2NaOH = Cu(OH)2↓ + 2NaNO3;
в) Cu(OH)2 + 2HCl = CuCl2 + 2H2O;
г) CuCl2 + 4NH3 = [Cu(NH3)4]Cl2
Задание 394
Составьте уравнения реакций, которые надо провести для осуществления следующих превращений:
Ag → AgNO3 → AgCl → [Ag(NH3)2]Cl → AgCl
Решение:
Задание 416
Составьте уравнения реакций, которые надо провести для осуществления превращений:
Na2Cr2O7 → Na2CrO4 → Na2Cr2O7 → СгС13 → Сг(ОН)3
Уравнение окислительно-восстановительной реакции напишите на основании электронных уравнений.
Решение:
Уравнения реакций, которые надо провести для осуществления превращений:
Na2Cr2O7 → Na2CrO4 → Na2Cr2O7 → СгС13 → Сг(ОН
Под действием щёлочи дихромат-ионы Cr2O7 2- переходят в хромат-ионы CrO4. При подкислении растворов хроматов ионы CrO4 2- переходят в Cr2O7 2- .
в) Кислые растворы хроматов и дихроматов обладают окислительными свойствами. При их восстановлении жёлтая окраска хроматов или оранжевая дихроматов переходят в зеленную окраску, обусловленную присутствием ионов Cr 3+ .
6Fe 2+ + 2Cr 6+ = 6Fe 3+ + 2Cr 3+
г) При действии на соль CrCl3 раствором щёлочи выпадает осадок Сг(ОН)3:
Задание 427
Составьте уравнения реакций, которые надо провести для осуществления превращений:
Ni → N i(NO3)2 → Ni(OH)2 → Ni(ОН)3 → NiCl2
Уравнения окислительно-восстановительных реакций напишите на основании электронных уравнений.
Решение:
Уравнения реакций, которые надо провести для осуществления превращений:
а) Ni → N i(NO 3 ) 2 =
Напишите уравнения реакций для осуществления превращений?
Химия | 5 — 9 классы
Напишите уравнения реакций для осуществления превращений.
Ca + 2H2O = Ca(OH)2(в осадок) + H2(газ)
СaH2 + 2H2O = Ca(OH)2(осадок) + 2H2(газ)
CaO + H2O = Ca(OH)2(осадок)
Ca(OH)2 + CO2 = CaCO3 + H2O
CaCO3 = (под температурой) = CaO + CO2(газ)
СaCO3 + HCl = CO2(газ) + H2O + CaCL2
CaO + 2HCl = CaCl2 + H2O
3CaCl2 + 2H3PO4 + Ca3(PO4)2(осадок) + 6HCl.
Напишите уравнения реакции для осуществления превращений?
Напишите уравнения реакции для осуществления превращений.
Напишите уравнения реакций, которые надо провести для осуществления следующих превращений : AL2O3 — — AL — — ALCL3 Al2S3?
Напишите уравнения реакций, которые надо провести для осуществления следующих превращений : AL2O3 — — AL — — ALCL3 Al2S3.
ПОМОГИТЕЕЕЕ напишите уравнения реакций, которые надо провести для осуществления следующих превращений Al2O3← Al⇒AlCl3 Al→Al2S3?
ПОМОГИТЕЕЕЕ напишите уравнения реакций, которые надо провести для осуществления следующих превращений Al2O3← Al⇒AlCl3 Al→Al2S3.
12. составьте уравнения реакций, не обходимых для осуществления превращений Si — SiO2 — Na2SiO3 — H2SiO3 13?
12. составьте уравнения реакций, не обходимых для осуществления превращений Si — SiO2 — Na2SiO3 — H2SiO3 13.
Составьте уравнения реакций, не обходимых для осуществления превращений H2SiO3 — SiO2 — SiF4 14.
Составьте уравнения реакций, не обходимых для осуществления превращений K2CO3 — K2SiO3 — H2SiO3 — SiO2.
Напишите уравнение реакции для осуществления приведенных ниже превращений : Na — > ; NaOH — > ; Na2SO4 — > ; NaNO3?
Напишите уравнение реакции для осуществления приведенных ниже превращений : Na — > ; NaOH — > ; Na2SO4 — > ; NaNO3.
Напишите уравнение реакций которые надо провести для осуществления превращений : уксусный альдегид — этанол — этилен — ацетилен — ацетальдегид?
Напишите уравнение реакций которые надо провести для осуществления превращений : уксусный альдегид — этанол — этилен — ацетилен — ацетальдегид.
Напишите уравнения реакций которые надо провести для осуществления следующих превращений : метан — метанол — формальдегид — фенолформальдегидная смола?
Напишите уравнения реакций которые надо провести для осуществления следующих превращений : метан — метанол — формальдегид — фенолформальдегидная смола.
Напишите уравнения реакций для осуществления следущих превращений : 1)крахмал — глюкоза — этиловый спирт 2)глюкоза — глюконоая кислота?
Напишите уравнения реакций для осуществления следущих превращений : 1)крахмал — глюкоза — этиловый спирт 2)глюкоза — глюконоая кислота.
Напишите уравнения реакций для осуществления превращений : СН3Cl → С2Н6→ С2Н5Br→ С2Н5ОН→ СН3 — СОH → СН3 — СОH?
Напишите уравнения реакций для осуществления превращений : СН3Cl → С2Н6→ С2Н5Br→ С2Н5ОН→ СН3 — СОH → СН3 — СОH.
Здравствуйте, помогите, пожалуйста :Напишите уравнения реакций, которые необходимо провести для осуществления следующих превращений :вот, ход моих решений?
Здравствуйте, помогите, пожалуйста :
Напишите уравнения реакций, которые необходимо провести для осуществления следующих превращений :
вот, ход моих решений.
На этой странице находится вопрос Напишите уравнения реакций для осуществления превращений?, относящийся к категории Химия. По уровню сложности данный вопрос соответствует знаниям учащихся 5 — 9 классов. Здесь вы найдете правильный ответ, сможете обсудить и сверить свой вариант ответа с мнениями пользователями сайта. С помощью автоматического поиска на этой же странице можно найти похожие вопросы и ответы на них в категории Химия. Если ответы вызывают сомнение, сформулируйте вопрос иначе. Для этого нажмите кнопку вверху.
В электрохимическом ряду напряжений металлов алюминий предшествует железу. В гальванопаре алюминий — железо происходит ускоренная коррозия алюминия : (анод Al, + ) Al⁰ — 3e = Al³⁺ в зависимости от химического состава пресной или морской воды на като..
1)CaCO3 = CaO + CO2 CaO + H2O = Ca(OH)2 Ca(OH)2 + K2CO3 = CaCO3 + 2KOH CaCO3 + 2HNO3 = Ca(NO3)2 + H2CO3 2) 4P + 5O2 = 2P2O5 P2O5 + 3H2O = 2H3PO4 2H3PO4 + 3CaCO3 = Ca3(PO4)2 + 3H2CO3 Ca3(PO4)2 + 6HNO3 = 2H3PO4 + 3Ca(NO3)2.
А) Na > Li Б) Li > Be В) Mg > Al Г) K в группе сверху вниз и в периоде справа налево увеличиваются Металлические свойства.
4) 2 Al + 3S = Al2S3 На 2 моль Al надо 3 моль S На х моль Al — 0. 3 моль S Значит n(Al) = (2•0. 3) / 3 = 0. 2 моль Количество моль Al2S3 по уравнению видно : в три раза меньше, чем серы : 0. 3 / 3 = 0. 1 моль 3) количество вещества серы в три ра..
1. BaSO4 (выпадает в осадок) + 2HCl 2. Fe(NO3)3 + 3AgCl (выпадает в осадок) 3. 2NaOH + BaCO3 (выпадает в осадок).
Сложно не всем понятна легко допустить ошибку огромное кол — во вычислений имеет долю опасности.
Смеси : — Бензин ; — Кровь ; — Зола. Чистые вещества : — Соль ; — Золото.
Cu(OH)2 = CuO + H2O M(Cu(OH)2) = 98г / моль M(CuO) = 80г / моль n(Cu(OH)2) = 196 / 98 = 2моль nCu(OH)2 : nCuO = 1 : 1 n(CuO) = 2моль m(CuO) = 2 * 80 = 160г CuO + H2 = Cu + H2O n(CuO) = 2моль nCuO : nH2 = 1 : 1 n(H2) = 2моль V(H2) = 2 * 22, 4 = 44, 8л..
Гидроксид меди(основание) азотная кислота (кислоты) оксид фосфора 5 класс оксиды гидроксиды алюминия 3 основание оксид плюмбума (оксид).
То, где есть группа ОН – это основания, или гидрооксиды (меди, алюминия), второе – азотная кислота, третье оксид фосфора, последнее – оксид свинца.
http://buzani.ru/zadachi/khimiya-shimanovich/998-skhemy-prevrashchenij-zadaniya-392-394-416-427
http://himia.my-dict.ru/q/2862285_napisite-uravnenia-reakcij-dla-osusestvlenia-prevrasenij/