Номенклатура жиров
Общее название жиров – триацилглицерины (триглицериды).
Существует несколько способов назвать молекулу жира.
Например, жир, образованный тремя остатками стеариновой кислоты, будет иметь следующие названия:
Физические свойства жиров
Жиры растворимы в органических растворителях и нерастворимы в воде. С водой жиры не смешиваются.
| Животные жиры — предельные | Растительные жиры (масла) — непредельные |
| Твёрдые, образованы предельными кислотами – стеариновой и пальмитиновой. Все животные жиры, кроме рыбьего – твёрдые. | Жидкие, образованы непредельными кислотами – олеиновой, линолевой и другими. Все растительные жиры, кроме пальмового масла – жидкие. |
Химические свойства жиров
1. Гидролиз (омыление) жиров
Жиры подвергаются гидролизу в кислой или щелочной среде или под действием ферментов.
1.1. Кислотный гидролиз
Под действием кислот жиры гидролизуются до глицерина и карбоновых кислот, которых входили в молекулу жира.
| Например, при гидролизе тристеарата глицерина в кислой среде образуется стеариновая кислота и глицерин |
1.2. Щелочной гидролиз — омыление жиров
При щелочном гидролизе жиров образуется глицерин и соли карбоновых кислот, входивших в состав жира.
| Например, при гидролизе тристеарата глицерина гидроксидом натрия образуется стеарат натрия . |
2. Гидрирование (гидрогенизация) ненасыщенных жиров
Гидрогенизация жиров — это процесс присоединения водорода к остаткам непредельных кислот, входящих в состав жира.
При этом остатки непредельных кислот переходят в остатки предельных, жидкие растительные жиры превращаются в твёрдые (маргарин).
| Например, триолеат глицерина при гидрировании превращается в тристеарат глицерина: |
| Количественной характеристикой степени ненасыщенности жиров служит йодное число, показывающее, какая масса йода может присоединиться по двойным связям к 100 г жира. |
3. Мыло и синтетические моющие средства
При щелочном гидролизе жиров образуются мыла – соли высших жирных кислот.
Стеарат натрия – твёрдое мыло.
Стеарат калия – жидкое мыло.
Моющая способность мыла зависит от жесткости воды. Оно хорошо мылится и стирает в мягкой воде, плохо стирает в жёсткой воде и совсем не стирает в морской воде, так как содержащие в ней ионы Ca 2+ и Mg 2+ дают с высшими кислотами нерастворимые в воде соли.
| Например, тристеарат глицерина взаимодействует с сульфатом кальция |
Поэтому наряду с мылом используют синтетические моющие средства.
Их производят из других веществ, например из алкилсульфатов — солей сложных эфиров высших спиртов и серной кислоты.
Спирт реагирует с серной кислотой с образованием алкилсульфата .
Далее алкилсульфат гидролизуется щелочью:
Эти соли содержат в молекуле от 12 до 14 углеродных атомов и обладают очень хорошими моющими свойствами. Кальциевые и магниевые соли этих веществ растворимы в воде, а потому такие мыла моют и в жесткой воде. Алкилсульфаты содержатся во многих стиральных порошках.
Гидролиз триацилглицеринов
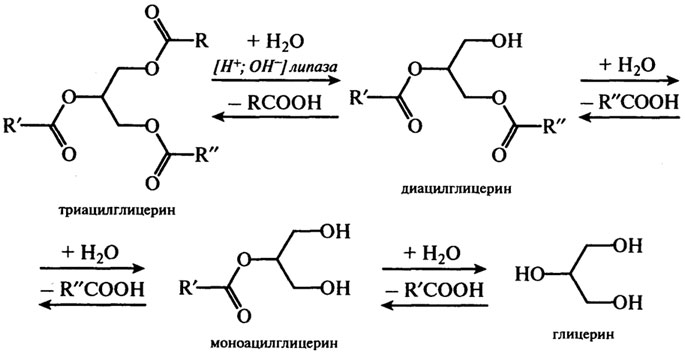
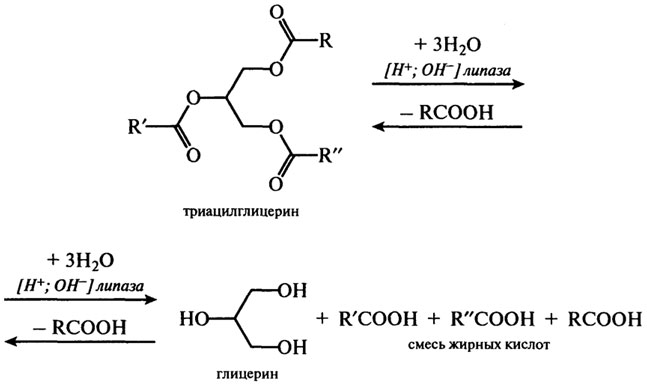
Под влиянием щелочей, кислот, фермента липазы триацилглицерины гидролизуются с образованием ди–, затем моноацилглицеринов и, в конечном счете, жирных кислот и глицерина.
Результаты гидролиза выражаются схемой:
В присутствии кислотных катализаторов (сульфокислоты, H2SO4) процесс ведут при 100°C в избытке воды. В отсутствие катализаторов расщепление проводят при температуре 220–225°C под давлением 2–2,5 MПa («безреактивное» расщепление). Гидролиз концентрированными водными растворами гидроксида натрия (омыление) является основой процесса получения («варки») мыла. На скорость гидролиза ацилглицерина влияют строение и положение ацилов, температура, катализаторы. С ростом длины углеродной цепи, увеличением ненасыщенности (при той же длине углеродной цепи) ацилов скорость гидролиза снижается. Гидролиз ацилглицеринов под действием липазы протекает ступенчато. При этом наблюдается определенная селективность: на первой стадии образуются 1,2–диацилглицерины, на второй – 2–мо–ноацилглицерины. Скорость гидролиза моноацилглицеринов выше, чем триацилглицеринов; диацилглицерины занимают промежуточное положение.
Гидролиз триацилглицеринов широко применяется в технике для получения жирных кислот, глицерина, моно– и диацилглицеринов.
Гидролитический распад жиров, липидов зерна, муки, крупы и других жиросодержащих пищевых продуктов является одной из причин ухудшения их качества, в конечном счете – порчи. Особенно ускоряется этот процесс при повышении влажности хранящихся продуктов, температуры, активности липазы. Скорость и глубину гидролиза масел и жиров (в том числе содержащихся в пищевом сырье и в готовых продуктах)
можно охарактеризовать с помощью кислотного числа. Кислотное число – это количество миллиграммов едкого калия, необходимое для нейтрализации свободных жирных кислот, содержащихся в 1 г масла или жира. Кислотное число для ряда пищевых продуктов нормируется стандартами и является одним из показателей, характеризующих их качество.
199 :: 200 :: 201 :: Содержание
201 :: 202 :: 203 :: Содержание
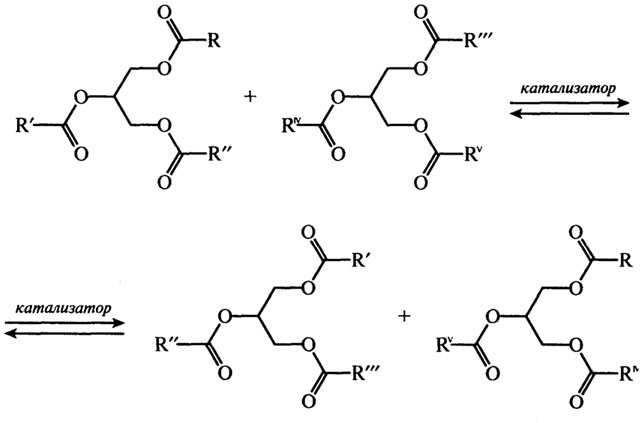
Переэтерификация
Большое практическое значение имеет группа реакций, при которых идет обмен ацильных групп (ацильная миграция), приводящий к образованию молекул новых ацилглицеринов. Триацилглицерины при температуре 80–9O°C в присутствии катализаторов (метилат и этилат натрия, натрий и калий, алюмосиликаты) способны обмениваться ацилами (переэтерификация). При этом ацильная миграция происходит как внутри молекулы ацилглицерина (внутримолекулярная Переэтерификация), так и между различными молекулами ацилглицеринов (межмолекулярная переэтерификация).
При переэтерификации с участием химических катализаторов состав жирных кислот жира не меняется, происходит их статистическое распределение в смеси триглицеридов, что приводит к изменению физико–химических свойств жировых смесей в результате изменения молекулярного состава. Увеличение числа ацил–глицериновых компонентов в жире
приводит к снижению температуры плавления и твердости жира, повышению его пластичности.
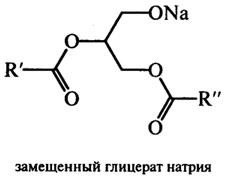
Истинным катализатором переэтерификации является глицерат натрия, образующийся при взаимодействии алкоголята натрия с триацилглицерином (или щелочи с глицерином).
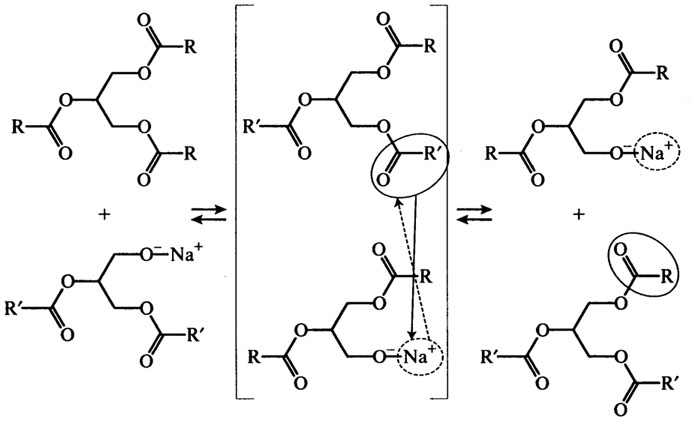
Механизм реакции переэтерификации заключается во взаимодействии карбонильной группы >C=0 сложного эфира со спиртовыми группами:
Образовавшийся глицерат взаимодействует с новой молекулой триацилглицерина. Скорость переэтерификации зависит от ацилглицеринового и жирнокислотного состава жира, количества и активности катализатора, температуры.
Переэтерификация высокоплавких животных и растительных жиров с жидкими растительными маслами позволяет получить пищевые пластичные жиры с высоким содержанием линолевой кислоты при отсутствии транс–изомеров жирных кислот. Готовые переэтерифицированные жиры, предназначенные в качестве компонентов маргариновой продукции, имеют следующие показатели: температура плавления 25–35°C; твердость (при 15°C) 30– 130г/м; массовая доля твердых триглицеридов (при 20°C) 6–20%. Переэтерифицированные жиры специального назначения применяются в хлебопечении, при производстве
аналогов молочного жира, кондитерского жира, комбинированных жиров и т. д.
Гидролиз жира
Лабораторная работа № 6
Свойства липидов
Опыт 1. Эмульгирование жира.
Принцип метода. При взбалтывании жира с водой, раствором желчи, белка, мыла, соды образуется эмульсия. Вода с жиром дает нестойкую, а остальные растворы стойкую эмульсию.
Это обусловлено тем, что поверхностно – активные частицы желчных кислот, белка, мыла обволакивают капельки жира и препятствуют их слиянию. Эмульгирование жира содой обусловлено образованием мыла в результате взаимодействия углекислого натрия с присутствующими в жире свободными жирными кислотами.
Порядок выполнения работы.
В 4 пробирки наливают по 1 мл: в первую – дистиллированной воды, во вторую – 1% раствора яичного белка, в третью – 1% раствора мыла, в четвертую – 1% раствора углекислого натрия Na 2 CO 3 •10H 2 O. В каждую пробирку добавляют по 2 капли растительного масла и тщательно взбалтывают.
Результаты работы заносят в таблицу:
| Вода+растительное масло | Белок+растительное масло | Мыло+растительное масло | Сода+растительное масло |
| Степень эмульгирования жира |
Примечание: Степень эмульгирования выражают знаком плюс (+),
Отсутствие эмульгирования выражают знаком минус (–).
Опыт 3. Гидролиз жира и открытие в гидролизате его составных частей.
Гидролиз жира.
В широкую пробирку пипеткой налейте 20 капель подсолнечного масла и мерным цилиндром 2 − 3 мл 1%-ного спиртового раствора KOH. Пробирку поместите в кипящую водяную баню на 15 − 20 минут до образования однородного раствора. Напишите уравнение реакции гидролиза триглицерида.
жир глицерин стеарат калия
К гидролизату мерным цилиндром прилейте 6 − 8 мл воды, взболтайте и используйте для открытия глицерина и жирных кислот.
Принцип метода. Качественная реакция на определение наличия глицецерина в растворах проводится с раствором сульфата меди (II) и раствором гидроксида натрия. Таким образом, происходит получение глицерата меди – комплексного соединения сине-василькового цвета.
Химический эксперимент проводится так: к раствору сульфата меди (II) приливается раствор гидроксида натрия. Раствор окрашивается в синий цвет – это выпал осадок гидроксида меди (II). Далее добавляется несколько мл гидролизата или глицерина и раствор перемешивается. Наблюдается растворение осадка – образуется комплексное соединение цвета индиго — глицерат меди. Получение его записывается в уравнении:
глицерин глицерат меди
При взаимодействии серной или соляной кислоты с гидролизатом или мылом выделяются свободные жирные кислоты, которые всплывают на поверхность жидкости. Реакция идет по следующему уравнению:
http://helpiks.org/5-109277.html
http://mydocx.ru/10-2097.html