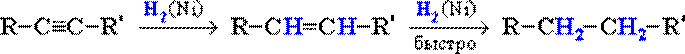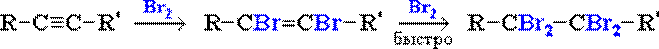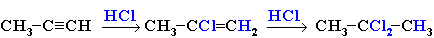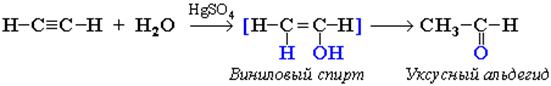Acetyl
Наведите курсор на ячейку элемента, чтобы получить его краткое описание.
Чтобы получить подробное описание элемента, кликните по его названию.
| H + | Li + | K + | Na + | NH4 + | Ba 2+ | Ca 2+ | Mg 2+ | Sr 2+ | Al 3+ | Cr 3+ | Fe 2+ | Fe 3+ | Ni 2+ | Co 2+ | Mn 2+ | Zn 2+ | Ag + | Hg 2+ | Pb 2+ | Sn 2+ | Cu 2+ | |
| OH — | Р | Р | Р | Р | Р | М | Н | М | Н | Н | Н | Н | Н | Н | Н | Н | — | — | Н | Н | Н | |
| F — | Р | М | Р | Р | Р | М | Н | Н | М | М | Н | Н | Н | Р | Р | Р | Р | Р | — | Н | Р | Р |
| Cl — | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Н | Р | М | Р | Р |
| Br — | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Н | М | М | Р | Р |
| I — | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | ? | Р | ? | Р | Р | Р | Р | Н | Н | Н | М | ? |
| S 2- | М | Р | Р | Р | Р | — | — | — | Н | — | — | Н | — | Н | Н | Н | Н | Н | Н | Н | Н | Н |
| HS — | Р | Р | Р | Р | Р | Р | Р | Р | Р | ? | ? | ? | ? | ? | Н | ? | ? | ? | ? | ? | ? | ? |
| SO3 2- | Р | Р | Р | Р | Р | Н | Н | М | Н | ? | — | Н | ? | Н | Н | ? | М | М | — | Н | ? | ? |
| HSO3 — | Р | ? | Р | Р | Р | Р | Р | Р | Р | ? | ? | ? | ? | ? | ? | ? | ? | ? | ? | ? | ? | ? |
| SO4 2- | Р | Р | Р | Р | Р | Н | М | Р | Н | Р | Р | Р | Р | Р | Р | Р | Р | М | — | Н | Р | Р |
| HSO4 — | Р | Р | Р | Р | Р | Р | Р | Р | — | ? | ? | ? | ? | ? | ? | ? | ? | ? | ? | Н | ? | ? |
| NO3 — | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | — | Р |
| NO2 — | Р | Р | Р | Р | Р | Р | Р | Р | Р | ? | ? | ? | ? | Р | М | ? | ? | М | ? | ? | ? | ? |
| PO4 3- | Р | Н | Р | Р | — | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н |
| CO3 2- | Р | Р | Р | Р | Р | Н | Н | Н | Н | ? | ? | Н | ? | Н | Н | Н | Н | Н | ? | Н | ? | Н |
| CH3COO — | Р | Р | Р | Р | Р | Р | Р | Р | Р | — | Р | Р | — | Р | Р | Р | Р | Р | Р | Р | — | Р |
| SiO3 2- | Н | Н | Р | Р | ? | Н | Н | Н | Н | ? | ? | Н | ? | ? | ? | Н | Н | ? | ? | Н | ? | ? |
| Растворимые (>1%) | Нерастворимые ( Спасибо! Ваша заявка отправлена, преподаватель свяжется с вами в ближайшее время. Вы можете также связаться с преподавателем напрямую: 8(906)72 3-11-5 2 Скопируйте эту ссылку, чтобы разместить результат запроса » » на другом сайте. Изображение вещества/реакции можно сохранить или скопировать, кликнув по нему правой кнопкой мыши. Если вы считаете, что результат запроса » » содержит ошибку, нажмите на кнопку «Отправить». Этим вы поможете сделать сайт лучше. К сожалению, регистрация на сайте пока недоступна. На сайте есть сноски двух типов: Подсказки — помогают вспомнить определения терминов или поясняют информацию, которая может быть сложна для начинающего. Дополнительная информация — такие сноски содержат примечания или уточнения, выходящие за рамки базовой школьной химии, нужны для углубленного изучения. Здесь вы можете выбрать параметры отображения органических соединений. Димеризация и тримеризация алкиновНоменклатура алкинов. Первый член гомологического ряда – этин имеет историческое название: НС≡СН ацетилен. По систематической номенклатуре названия ацетиленовых углеводородов производят от названий соответствующих алканов (с тем же числом атомов углерода) путем замены суффикса –ан на –ин: H-C≡C-H — этИН СН3-С≡С-Н – пропИН и т.д. Главная цепь выбирается таким образом, чтобы она обязательно включала в себя тройную связь (т.е. она может быть не самой длинной). Виды изомерии алкинов. 1.Изомерия положения тройной связи (начиная с С4Н6): 2.Изомерия углеродного скелета (начиная с С5Н8): 3.Межклассовая изомерия с алкадиенами ( начиная с С3Н4) и циклоалкенами (начиная с С4Н6): бутин-1 бутадиен ∣ ∣ циклобутен ПОЛУЧЕНИЕ АЛКИНОВ.
СВОЙСТВА АЛКИНОВ
Реакции присоединения. А. Гидрирование: В присутствии металлических катализаторов (Pt, Ni) алкины присоединяют водород с образованием алкенов (разрывается первая π-связь), а затем алканов (разрывается вторая π-связь): При использовании менее активного катализатора [Pd/CaCO3/Pb(CH3COO)2] гидрирование останавливается на стадии образования алкенов. Б. Галогенирование: Электрофильное присоединение галогенов к алкинам протекает медленнее, чем для алкенов (первая π-связь разрывается труднее, чем вторая): Алкины обесцвечивают бромную воду (качественная реакция). В. Гидрогалогенирование. Присоединение галогеноводородов также идет по электрофильному механизму. Продукты присоединения к несимметричным алкинам определяются правилом Марковникова: Г. Гидратация (реакция Кучерова): Присоединение воды в присутствии катализатора соли ртути (II) идет через образование неустойчивого енола, который изомеризуется в альдегид или кетон. Если гидратации подвергается АЦЕТИЛЕН, то образуется уксусный альдегид. Из всех остальных алкинов при гидратации образуются кетоны (так как присоединение протекает по правилу Марковникова). Димеризация и тримеризация алкинов. 1) Димеризация под действием водно-аммиачного раствора CuCl: 2) Тримеризация ацетилена над активированным углем приводит к образованию бензола (реакция Зелинского): Напишите уравнение реакции тримеризации бутинаРешение задачи 791. При гидролизе карбида кальция образуется ацетилен CaC2 + 2H2O = C2H2 + Ca(OH)2. При действии избытка амида натрия на ацетилен образуется ацетиленид натрия (В). При взаимодействии ацетиленида натрия с избытком иодистого метила образуется бутин-2 (С). При нагревании диметилацетилена (бутина-2) происходит тримеризация с образованием гексаметилбензола (D), при озонолизе которого с последующим восстановительным гидролизом образуется диметилглиоксаль (Е). Обработка вещества Е гдроксиламином приводит к образованию диметилглиоксима (F). При гидрировании ацетилена на катализаторе Линдлара получается этилен (G), который образует 1,2-дихлорэтан (Н) при взаимодействии с хлором. Действие избытка аммиака на 1,2-дихлорэтан приводит к образованию этилендиамина (К). Дальнейшее взаимодействие этилендиамина с монохлоруксусной кислотой приводит к образованию этилендиаминтетрауксусной кислоты(L), которую обычно используют в виде дигидрата динатриевой соли (трилон Б). 2.-3 Диметилглиоксим – известный аналитический реагент, использующийся для качественного и количественного определения никеля в растворе. Этот реагент сегодня известен под названием «реактив Чугаева», названный по фамилии известного русского химика, специалиста в области координационной химии Льва Александровича Чугаева. Структурные формулы комплексных частиц, образующихся при взаимодействии солей никеля с диметилглиоксимом и трилоном Б представлены ниже. источники: http://lektsii.org/3-10315.html http://www.niic.nsc.ru/study/studentam/157-tasks/reshenie-zadachi/554-reshenie-zadachi-84 |