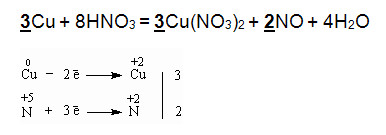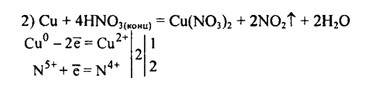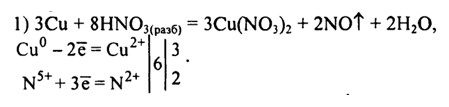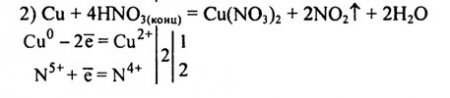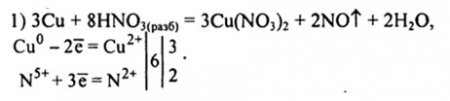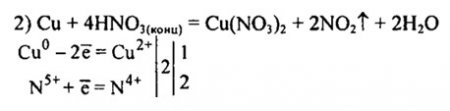Напишите уравнения реакций для следующих переходов N2 → NO → N02 →HN03 →CU(N03)2. Превращение 1 рассмотрите в свете ОВР, 4 — в свете ТЭД.
Ваш ответ
решение вопроса
Похожие вопросы
- Все категории
- экономические 43,298
- гуманитарные 33,622
- юридические 17,900
- школьный раздел 607,232
- разное 16,830
Популярное на сайте:
Как быстро выучить стихотворение наизусть? Запоминание стихов является стандартным заданием во многих школах.
Как научится читать по диагонали? Скорость чтения зависит от скорости восприятия каждого отдельного слова в тексте.
Как быстро и эффективно исправить почерк? Люди часто предполагают, что каллиграфия и почерк являются синонимами, но это не так.
Как научится говорить грамотно и правильно? Общение на хорошем, уверенном и естественном русском языке является достижимой целью.
Please wait.
We are checking your browser. gomolog.ru
Why do I have to complete a CAPTCHA?
Completing the CAPTCHA proves you are a human and gives you temporary access to the web property.
What can I do to prevent this in the future?
If you are on a personal connection, like at home, you can run an anti-virus scan on your device to make sure it is not infected with malware.
If you are at an office or shared network, you can ask the network administrator to run a scan across the network looking for misconfigured or infected devices.
Another way to prevent getting this page in the future is to use Privacy Pass. You may need to download version 2.0 now from the Chrome Web Store.
Cloudflare Ray ID: 6e1473bfaf024c2c • Your IP : 85.95.188.35 • Performance & security by Cloudflare
Ответы на контрольную работу по теме «Неметаллы»(Габриелян)
ЗАДАНИЕ 1
Напишите уравнения реакций для следующих переходов:
С →С02 →СаС03 →СаС12 →СаС03.
Превращение 1 рассмотрите в свете ОВР, 4 — в свете ТЭД.
С→СО2→ СаСО3→ CaCl2 → СаСО3
C+O2 → CO2
C0 -4e= C+4 восстановитель
O2 + 4e= 2O-2 окислитель
CO2+ CaO→CaCO3
CaCO3+2HCl→ CaCl2 +H2O + CO2
CaCl2+Na2CO3=CaCO3+2NaCl
Ca2++CO32-=CaCO3
ЗАДАНИЕ 2
Дайте характеристику реакции, уравнение которой
N2 + ЗН2 2NH3 + Q,
по всем изученным признакам классификации.
Рассмотрите данную реакцию с точки зрения ОВР.
3H2 + N2 2NH3 + Q
N20 +2*3е→2N-3 окислитель
H20 -2*1е→2H+1 восстановитель
Исходные вещества: 1 моль азота (молекула из 2 атомов азота), 3 моль водорода (молекула из 2 атомов водорода). Продукт реакции – аммиак, 2 моль. Молекула из 1 атома азота и 2 атомов водорода. Исходные вещества продукты реакции – газы.
Реакция:
Экзотермическая.
Окислительно-восстановительная.
Прямая.
Каталитическая.
Обратимая.
ЗАДАНИЕ 3
В схеме ОВР расставьте коэффициенты методом электронного баланса, укажите окислитель и восстановитель:
Сu + HN03(paз6) → CU(N03)2 + NO + Н20.
ЗАДАНИЕ 4
К раствору, содержащему 16 г сульфата меди (II), прибавили избыток железных опилок. Какая масса меди выделилась при этом?
CuSO4 + Fe = FeSO4 + Cu
n (CuSO4) = 16/160 = 0,1моль
n (CuSO4) = n (Cu) =0,1моль
m(Cu) = 0,1*64= 6,4 г
ЗАДАНИЕ 1
Напишите уравнения реакций для следующих переходов:
N2 → NO → N02 →HN03 →CU(N03)2.
Превращение 1 рассмотрите в свете ОВР, 4 — в свете ТЭД.
N2 + O2 = 2NO
N20 -4e= 2N+2 восстановитель
O20 +4e= 2O-2 окислитель
2NO + O2 = 2NO2
4NO2 + O2 + 2H2O = 4HNO3
3Cu + 8HNO3 = 3Cu(NO3)2 + 2NO + 4H2O
3Cu0 + 8H++8NO3- = 3Cu2+ +6NO3- + 2NO + 4H2O
ЗАДАНИЕ 2
Дайте характеристику реакции, уравнение которой
2N0 + 02 2N02 + Q,
по всем изученным признакам классификации.
Рассмотрите данную реакцию с точки зрения ОВР.
2NO + O2 = 2NO2 + Q
N+2 -2e = N+4 восстановитель
O2 +4e = 2O-2 окислитель
Исходные вещества: 2 моль оксида азота 2 (молекула из 1 атома азота и 1 атома кислорода), 1 моль кислорода (молекула из 2 атомов кислорода). Продукт реакции – оксид азота 4, 2 моль (1 атом азота и 2 атома кислорода в молекуле). Исходные вещества продукты реакции – газы.
Реакция:
Экзотермическая.
Окислительно-восстановительная.
Прямая.
Некаталитическая.
Обратимая.
ЗАДАНИЕ 3
В схеме ОВР расставьте коэффициенты методом электронного баланса, укажите окислитель и восстановитель:
Сu + НNO3(КОНЦ) → Cu(N03)2 + N02 + Н20.
ЗАДАНИЕ 4
6,5 г цинка обработали достаточным количеством разбавленного раствора серной кислоты. Определите объем выделившегося водорода.
H2SO4 + Zn = Zn SO4 + H2 ↑
n(Zn) = 6,5/65 = 0,1 моль
n(H2) = n(Zn) = 0,1 моль
V(H2) = 0,1*22,4 = 2,24 л
ЗАДАНИЕ 1
Напишите уравнения реакций для следующих переходов:
S → S02 →S03 H2S04 →BaS04.
Превращение 1 рассмотрите в свете ОВР, 4 — в свете ТЭД.
S+O2→ SO2
S0 -4e = S+4
O02 + 4e = 2O-2
2SO2+O2→2SO3
SO3+H2O→H2SO4
H2SO4+ BaCl2 = BaSO4↓ + 2HCl
SO42-+ Ba2+ = BaSO4↓
ЗАДАНИЕ 2
Дайте характеристику реакции, уравнение которой
С02 + С 2СО — Q,
по всем изученным признакам классификации.
Рассмотрите данную реакцию с точки зрения ОВР.
СО2 + С = 2СО– Q
С+4 +2е = С+2 окислитель
С0 -2е =С+2 восстановитель
Исходные вещества: 1 моль оксида углерода 4 (1 атом углерода, 2 атома кислорода) – газ, 1 моль углерода (1 атом углерода) -тв. Продукт реакции – 2 моль оксида углерода 2 (1 атом углерода, 1 атома кислорода) – газ.
Эндотермическая
ОВР
Прямая
ЗАДАНИЕ 3
В схеме реакции расставьте коэффициенты методом электронного баланса, укажите окислитель и восстановитель:
Zn + H2S04(KOHц) → ZnS04 + H2S↑ + H20.
Zn + H2SO4(конц.) → ZnSO4 + H2S↑ + H2O
уравнения полуреакций:
Zn0 – 2e– → Zn+2| 2 | 8 | 4 | – восстановитель
S+6 + 8e– → S–2 | 8 | 8 | 1 | – окислитель
4Zn0 + S+6 = 4Zn+2 + S–2
4Zn + 5H2SO4(конц.) = 4ZnSO4 + H2S↑ + 4H2O
ЗАДАНИЕ 4
Определите количество вещества сульфата калия, полученного при сливании избытка раствора гидроксида натрия с раствором, содержащим 2 моль серной кислоты.
2KOH + H2SO4 = K2SO4 + H2O
n(H2SO4) = n(K2SO4) = 2 моль
ЗАДАНИЕ 1
Напишите уравнения реакций для следующих переходов:
Si → Si02 →Na2Si03 →H2Si03 →Si02.
Превращение 1 рассмотрите в свете ОВР, 3 — в свете ТЭД.
1) Si + O2 = SiO2
Si0 -4е = Si+4 восстановитель
O20 +4е = 2O2- окислитель
2) SiO2 + Na2O = Na2SiO3
3) Na2SiO3 + 2HCl = H2SiO3 ↓+ 2NaCl
2H+ +SiO3 2- = H2SiO3 ↓
4) H2SiO3 = SiO2 + Н2О
ЗАДАНИЕ 2
Дайте характеристику реакции, уравнение которой
Н20(пар) + СО Н2 + С02 — Q,
по всем изученным признакам классификации.
Рассмотрите данную реакцию с точки зрения ОВР.
Н+12О + С+2О = Н02 + С+4О2 – Q
2Н+1 +2е = Н02 окислитель
С+2 -2е =С+4 восстановитель
Исходные вещества: 1 моль воды (2 атома водорода, 1 атом кислорода) – газ, 1 моль оксида углерода 2 (1 атом углерода, 1 атом кислорода) -газ. Продукты реакции – 1 моль водорода (2 атома водорода в молекуле) – газ, 1 моль оксида углерода 4 (1 атом углерода, 2 атома кислорода) – газ.
Эндотермическая
ОВР
Прямая
Обратимая
Некаталитическая.
ЗАДАНИЕ 3
В схеме реакции расставьте коэффициенты методом электронного баланса, укажите окислитель и восстановитель:
NH3 + CuO→ N2 + Сu + Н20.
2NH3 + 3CuO -> 3Cu + N2 + 3H2O
N-3 -6е = N20 восстановитель
Cu+2 +2е =Cu0 окислитель
ЗАДАНИЕ 4
10 г оксида магния обработали раствором азотной кислоты. Какая масса соли образовалась?
MgO + 2HNO3 = Mg(NO3)2 + H2O
n (MgO) = 10/40 =0,25 моль
n (MgO) = n (Mg(NO3)2) = 0,25 моль
m(Mg(NO3)2) = 0,25*148= 37 г
ЗАДАНИЕ 1
Напишите уравнения реакций для переходов:
С → СН4 →С02 →СаС03 →… →СаС03.
Превращение 2 рассмотрите в свете ОВР, 5 — в свете ТЭД.
С + 2Н2 = СН4
СН4 + 2О2 = СО2 + 2Н2О
С-4 — 8е=С+4 восстановитель
О2 о +4е = 2О-2 окислитель
СО2 + СаО = СаСО3
CaCO3 + CO2 + H2O ↔ Ca(HCO3)2
Ca(HCO3)2 = CaCO3↓ + CO2 + H2O
Ca2+ + 2HCO3- = CaCO3↓ + CO2 + H2O
ЗАДАНИЕ 2
Дайте характеристику реакции, уравнение которой
2Fe + ЗС12 = 2FeCl3 + Q,
по всем изученным признакам классификации.
Определите окислитель и восстановитель, процессы окисления и восстановления.
ЗАДАНИЕ 3
В схеме реакции расставьте коэффициенты методом электронного баланса, укажите окислитель и восстановитель:
Сu + HN03(paз6) →Cu(NO3)2 + … + Н20.
ЗАДАНИЕ 4
К 160 кг 10%-го раствора сульфата меди (II) прибавили железные опилки. Какая масса меди выделилась?
CuSO4 + Fe = FeSO4 + Cu
m (CuSO4) = 160*0,1= 16 г
n(CuSO4) = 16/160 = 0,1 моль
m (Cu) =0,1 * 64 = 6,4 г
ЗАДАНИЕ 1
Напишите уравнения реакций для переходов:
N2 → Li3N →NO →N02 … →…→ Cu(NO3)2.
Превращение 2 рассмотрите в свете ОВР, 5 — в свете ТЭД.
1)N2+6Li->t,кат. ->2Li3N
2) 4Li3N + 5O2->t->4NO+6Li2O
N-3 -5e =N+2 восстановитель
O20 +4е= 2O-2 окислитель
3)2NO+O2->2NO2
4)4NO2+2H2O+O2->4HNO3
5) Cu + 4HNO3 = Cu(NO3)2 + 2NO2 + 2H2O
Cu0 + 4H+ +2NO3 -= Cu2+ + 2NO2 + 2H2O
ЗАДАНИЕ 2
Дайте характеристику реакции, уравнение которой
2А1 + 3S = A12S3 + Q,
по всем изученным признакам классификации.
Рассмотрите данную реакцию с точки зрения ОВР.
2Al + 3S = Al2S3 + Q
Al – 3e– = Al +III восстановитель
S+ 2e– = S –Il окислитель
Экзотермическая
ОВР
Прямая
Необратимая
Некаталитическая
Исходные вещества: 2 моль алюминия – тв., 3 моль серы тв.
Продукт: 1 моль сульфида алюминия (из 2 атомов алюминия, 3 атомов серы) – тв.
ЗАДАНИЕ 3
В схеме ОВР расставьте коэффициенты методом электронного баланса, укажите окислитель и восстановитель:
Сu + HN03(KOHЦ) → Cu(N03)2 + … + Н20.
ЗАДАНИЕ 4
Достаточное количество цинка обработали 120 кг 10%-го раствора серной кислоты. Определите объем выделившегося газа.
Zn + H2SO4 = ZnSO4 + H2
m (H2SO4) = 120*0,1= 12кг= 12000 г
n(H2SO4) = 12000/98 = 122 моль
n(H2) = n(H2SO4) = 122 моль
V(H2) = 122*22,4 = 2742 л
ЗАДАНИЕ 1
Напишите уравнения реакций для переходов:
S →FeS →S02 →S03 →…→ BaS04.
Превращение 2 рассмотрите в свете ОВР, 5 — в свете ТЭД.
Fe + S = FeS
2FeS + 3O2 = 2FeO + 2SO2
S-2 -6e = S+4 восстановитель
O20 +4е= 2O-2 окислитель
2SO2 + O2 = 2SO3
SO3 + H2O = H2SO4
BaCl2 + H2SO4 → BaSO4↓ + 2HCl
Ba2+ + SO42- → BaSO4↓
ЗАДАНИЕ 2
Дайте характеристику реакции, уравнение которой
ЗСа + 2Р = Са3Р2 — Q,
по всем изученным признакам классификации.
Рассмотрите данную реакцию с точки зрения ОВР.
3Са + 2Р = Са3Р2 — Q
Са – 2e– = Са +II восстановитель
Р + 3e– = Р –IlI окислитель
Эндотермическая
ОВР
Прямая
Необратимая
Некаталитическая
Исходные вещества: 2 моль фосфора – тв., 3 моль кальция тв.
Продукт: 1 моль фосфида кальция (из 2 атомов фосфора, 3 атомов кальция) – тв.
ЗАДАНИЕ 3
В схеме ОВР расставьте коэффициенты методом электронного баланса, укажите окислитель и восстановитель:
Zn + H2S04(KOH4) → ZnS04 + … + Н20.
2H2SO4 + Zn = SO2↑ +ZnSO4 + 2H2O
Zn – 2e– = Zn +II восстановитель
S+6 + 2e– = S +4 окислитель
ЗАДАНИЕ 4
Какой объем водорода выделится при взаимодействии достаточного количества цинка с 200 г 10% -го раствора серной кислоты?
H2SO4 + Zn = Zn SO4 + H2 ↑
m (H2SO4) = 200*0,1= 20 г
n(H2SO4) = 20/98 = 0,2 моль
n(H2) = n(H2SO4) = 0,2 моль
V(H2) = 0,2*22,4 = 4,57л
ЗАДАНИЕ 1
Напишите уравнения реакций для переходов:
Si → Si02 →Na2Si03 →…→ Si02.
Превращение 1 рассмотрите в свете ОВР, 3 — в свете ТЭД.
Si + O2 = SiO2
Si0 -4е = Si+4
O20 +4е= 2O-2 окислитель
SiO2 + Na2O = Na2SiO3
Na2SiO3 + 2HCl = H2SiO3 + 2NaCl
2Н+ +SiO3 2- = H2SiO3 ↓
H2SiO3 = SiO2+ H2O
ЗАДАНИЕ 2
Дайте характеристику реакции, уравнение которой
Fe203 + 2А1 = 2Fe + А1203 + Q,
по всем известным признакам классификации.
Рассмотрите данную реакцию с точки зрения ОВР.
Fe2O3 + 2Al = 2Fe + Al2O3 + Q
Al0 – 3e– = Al +III восстановитель
Fe+3 + 3e– = Fe 0 окислитель
Экзотермическая
ОВР
Прямая
Необратимая
Некаталитическая
Исходные вещества: 2 моль алюминия – тв., 1 моль оксида железа 3 (2 атома железа и 3 атома кислорода в ФЕ) тв.
Продукты: 2 моль железа, 1 моль оксида алюминия (из 2 атомов алюминия, 3 атомов кислорода в ФЕ) – тв.
ЗАДАНИЕ 3
В схеме ОВР расставьте коэффициенты методом электронного баланса, укажите окислитель и восстановитель:
NH3 + CuO→N2 + Сu + … .
3CuO + 2NH3 = 3Cu + N2 + 3H2O
Cu+2 + 2е = Cu0 окислитель
2N-3 -6е = N20 восстановитель
ЗАДАНИЕ 4
Достаточное количество оксида магния обработали 40 кг 10%-го раствора азотной кислоты. Какая масса соли образовалась?
2HNO3 + MgO = Mg(NO3)2 + H2O
m (HNO3) = 40000*0,1= 4000 г
n(HNO3) = 4000/63 = 63,5 моль
n(Mg(NO3)2) = n(HNO3)/2 = 31,7 моль
m (Mg(NO3)2) = 31,7*148 = 4698 г = 4,698 кг
ЗАДАНИЕ 1
Напишите уравнения реакций для переходов:
С →СН4 → … →CaCO3→ … → CaCO3.
Рассмотрите все реакции в свете ОВР и ТЭД везде, где это имеет место.
С + 2Н2 = СН4
С0 +4е = С-4 окислитель
Н20 -2е = 2Н+1 восстановитель
СН4 + О2 = СО2 + Н2О
С-4 -8е = С+4 восстановитель
О20 +4е = 2О-2 окислитель
СО2 + СаО = СаСОз
CaCO3+2HCl→ CaCl2 +H2O + CO2
CaCO3+2H+→ Ca2+ +H2O + CO2↑
CaCl2+Na2CO3=CaCO3+2NaCl
Ca2++CO32-=CaCO3
ЗАДАНИЕ 2
Дайте характеристику реакции, уравнение которой
Zn + 2НС1 = ZnCl2 + H2↑ + Q,
по всем изученным признакам классификации.
Рассмотрите реакцию с точки зрения ТЭД.
Zn+2HCl=ZnCl2+H2 + Q
Исходные вещества: 1 моль цинк, 2 моль соляной кислоты (1 атом водорода, 1 атом хлора в молекуле). Продукты реакции: 1 моль хлорида цинка (1 атом цинка, 2 атома хлора в ФЕ), 1 моль водорода (2 атома водорода).
Экзотермическая реакция
Цинк – тв., соляная кислота – ж., хлорид цинка тв. (раствор), водород – г.
Без катализатора
С изменением степеней окисления
Необратимая
2H++2Cl-+Zn0=Zn2++2Cl-+H20
2H++Zn0=Zn2++H20
ЗАДАНИЕ 3
Закончите уравнение ОВР, расставьте коэффициенты методом электронного баланса, укажите окислитель и восстановитель:
Сu + HN03(paз6) →.
ЗАДАНИЕ 4
К 160 кг 10%-го раствора сульфата меди (II) прибавили избыток железных опилок. Какая масса меди выделилась, если выход продукта составил 90% от теоретически возможного?
Fe + CuSO4 = FeSO4 + Cu
m (CuSO4) = 160000*0,1= 16000 г
n (CuSO4) = 16000/160= 100 моль
n (CuSO4)= n (Cu) по уравнению (теор.) = 100 моль
n (Cu) = 100/0,9 = 90 моль (пр.)
m (Cu) = 90*64= 5760 г
ЗАДАНИЕ 1
Напишите уравнения реакций для переходов:
N2 →… →NO →N02 →… →Cu(N03)2.
Рассмотрите все реакции в свете ОВР и ТЭД везде, где это имеет место.
1)N2+3H2->t,кат. ->2NH3
N20 +2*3е→2N-3 окислитель
H20 -2*1е→2H+1 восстановитель
2)4NH3+5O2->t,кат. ->4NO+6H2O
N-3 — 5е→N+2 восстановитель
O20 +4e→2O-2 окислитель
3)2NO+O2->2NO2
N+2 — 2е→N+4 восстановитель
O20 +4e→2O-2 окислитель
4)4NO2+2H2O+O2->4HNO3
N+4 — 1е→N+5 восстановитель
O20 +4e→2O-2 окислитель
5)Cu + 4HNO3 = Cu(NO3)2 + 2NO2 + 2H2O
Cu0 + 4H+ +2NO3 -= Cu2+ + 2NO2 + 2H2O
ЗАДАНИЕ 2
Дайте характеристику реакции, уравнение которой
2NO + 02 2N02 + Q,
по всем изученным признакам классификации. Рассмотрите данную реакцию в свете ОВР.
2NO + O2 = 2NO2 + Q
N+2 -2e = N+4 восстановитель
O2 +4e = 2O-2 окислитель
Исходные вещества: 2 моль оксида азота 2 (молекула из 1 атома азота и 1 атома кислорода), 1 моль кислорода (молекула из 2 атомов кислорода). Продукт реакции – оксид азота 4, 2 моль (1 атом азота и 2 атома кислорода в молекуле). Исходные вещества продукты реакции – газы.
Реакция:
Экзотермическая.
Окислительно-восстановительная.
Прямая.
Некаталитическая.
Обратимая.
ЗАДАНИЕ 3
Закончите уравнение ОВР и расставьте коэффициенты в нем методом электронного баланса, укажите окислитель и восстановитель:
Сu + НNОз(конц.> →.
ЗАДАНИЕ 4
ЦИНК массой 6,5 кг обработали избытком раствора серной кислоты. Определите объем выделившегося газа, если выход продукта реакции составил 80% от теоретически возможного.
H2SO4 + Zn = Zn SO4 + H2 ↑
n(Zn) = 65000/65 = 1000 моль
n(H2) = n(Zn) = 1000 моль (теор.)
n(H2)практ. = 1000*0,8 = 800моль
V(H2) = 800*22,4 = 17920л
ЗАДАНИЕ 1
Напишите уравнения реакций для переходов:
S →FeS →S02 →… →H2S04 →… .
Рассмотрите все реакции в свете ОВР и ТЭД везде, где это имеет место.
S+ Fe = FeS
S0 + 2e = S-2 окислитель
Fe0 -2e= Fe+2 восстановитель
4FeS + 7O2 → 2Fe2O3 + 4SO2↑
S-2 -6e = S+4 восстановитель
O2 +4e = 2O-2 окислитель
2SO2 + O2 = 2SO3
S +4 — 2е→ S +6 восстановитель
O20 +4e→2O-2 окислитель
SO3 + H2O = H2SO4
SO3 + H2O = 2H+ +SO42-
H2SO4 + 2NaOH = Na2SO4 + H2O
2H+ +2OH- = H2O
ЗАДАНИЕ 2
Дайте характеристику реакции, уравнение которой
С02 + С 2СО — Q,
по всем изученным признакам классификации. Рассмотрите данную реакцию в свете ОВР.
СО2 + С = 2СО– Q
С+4 +2е = С+2 окислитель
С0 -2е =С+2 восстановитель
Исходные вещества: 1 моль оксида углерода 4 (1 атом углерода, 2 атома кислорода) – газ, 1 моль углерода (1 атом углерода) -тв. Продукт реакции – 2 моль оксида углерода 2 (1 атом углерода, 1 атома кислорода) – газ.
Эндотермическая
ОВР
ЗАДАНИЕ 3
Закончите уравнение ОВР и расставьте коэффициенты в нем методом электронного баланса, укажите окислитель и восстановитель:
Zn + H2S04(KOHЦ) →.
Zn + H2SO4(конц.) → ZnSO4 + H2S↑ + H2O
уравнения полуреакций:
Zn0 – 2e– → Zn+2| 2 | 8 | 4 | – восстановитель
S+6 + 8e– → S–2 | 8 | 8 | 1 | – окислитель
4Zn0 + S+6 = 4Zn+2 + S–2
4Zn + 5H2SO4(конц.) = 4ZnSO4 + H2S↑ + 4H2O
ЗАДАНИЕ 4
Какой объем водорода выделится при взаимодействии 13 г цинка с избытком раствора серной кислоты? Объемная доля выхода водорода составляет 90% от теоретически возможного.
H2SO4 + Zn = Zn SO4 + H2 ↑
n(Zn) = 13/65 = 0,2 моль
n(H2) = n(Zn) = 0,2 моль (теор.)
n(H2)практ. = 0,2*0,9 = 0,18 моль
V(H2) = 0,18*22,4 = 4,032 л
ЗАДАНИЕ 1
Напишите уравнения реакций для переходов:
Si →…→ Na2Si03 →…→ Si02.
Рассмотрите все реакции в свете ОВР и ТЭД везде, где это имеет место.
Si + O2 = SiO2
S0 -4e = S+4 восстановитель
O2 +4e = 2O-2 окислитель
SiO2 + Na2O = Na2SiO3
SiO2 + Na2O = 2Na+ +SiO32-
Na2SiO3 + 2HCl = H2SiO3 ↓+ 2NaCl
2Н+ + SiO32- = H2SiO3 ↓
H2SiO3 = SiO2 + Н2О
ЗАДАНИЕ 2
Дайте характеристику реакции, уравнение которой
H20(nap) + C0H2 + C02-Q,
по всем изученным признакам классификации.
Рассмотрите данную реакцию в свете ОВР.
Н+12О + С+2О = Н02 + С+4О2 – Q
2Н+1 +2е = Н02 окислитель
С+2 -2е =С+4 восстановитель
Исходные вещества: 1 моль воды (2 атома водорода, 1 атом кислорода) – газ, 1 моль оксида углерода 2 (1 атом углерода, 1 атом кислорода) -газ. Продукты реакции – 1 моль водорода (2 атома водорода в молекуле) – газ, 1 моль оксида углерода 4 (1 атом углерода, 2 атома кислорода) – газ.
Эндотермическая
ОВР
Прямая
Обратимая
Некаталитическая.
ЗАДАНИЕ 3
В схеме ОВР расставьте коэффициенты методом электронного баланса, укажите окислитель и восстановитель:
NH3 + CuO→N2 + … + … .
3CuO + 2NH3 = 3Cu + N2 + 3H2O
Cu+2 + 2е = Cu0 окислитель
2N-3 -6е = N20 восстановитель
ЗАДАНИЕ 4
10 кг оксида магния обработали избытком раствора азотной кислоты. Какая масса соли образовалась, если выход соли составил 80% от теоретически возможного?
2HNO3 + MgO = Mg(NO3)2 + H2O
n(MgO) = 1000/40 = 250 моль
n(Mg(NO3)2) = n(MgO) = 250 моль (теор.)
n(Mg(NO3)2)практ. = 250*0,8 = 200 моль
m (Mg(NO3)2) 200*148 = 29600 г
http://gomolog.ru/reshebniki/9-klass/gabrielyan-2014/28/2.html
http://9class.ru/40-otvety-na-kontrolnuyu-rabotu-po-teme-nemetallygabrielyan.html