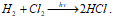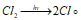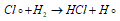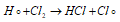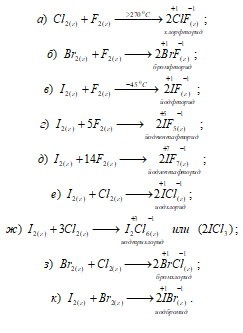Напишите уравнения реакций между хлором и следующими веществами: а) водородом; б) литием; в) алюминием; г) водой; д) гидроксидом
Ваш ответ
Похожие вопросы
- Все категории
- экономические 43,297
- гуманитарные 33,622
- юридические 17,900
- школьный раздел 607,223
- разное 16,830
Популярное на сайте:
Как быстро выучить стихотворение наизусть? Запоминание стихов является стандартным заданием во многих школах.
Как научится читать по диагонали? Скорость чтения зависит от скорости восприятия каждого отдельного слова в тексте.
Как быстро и эффективно исправить почерк? Люди часто предполагают, что каллиграфия и почерк являются синонимами, но это не так.
Как научится говорить грамотно и правильно? Общение на хорошем, уверенном и естественном русском языке является достижимой целью.
Напишите уравнения реакций между хлором и следующими веществами : водородом, литием, алюминием, водой, гидроксидом натрия (при нагревании и без нагревания)?
Химия | 5 — 9 классы
Напишите уравнения реакций между хлором и следующими веществами : водородом, литием, алюминием, водой, гидроксидом натрия (при нагревании и без нагревания).
Во всех реакциях укажите окислитель и восстановитель.
Cl2(О) + H2(В) = = 2HCl
Cl2(О) + 2Li(В) = = 2LiCl
3Cl2(О) + 2Al(В) = = 2AlCl3
Cl2(О и В, реакция диспропорционирования)) + H2O = = HClO + HCL
Cl2(О и В, реакция диспропорционирования)) + 2NaOH = = NaClO + NaCl + H2O
3Cl2(О и В, реакция диспропорционирования)) + 6NaOH = (t) = NaClO3 + 5NaCl + 3H2O.
1 / определите степень окисления хлора в следующих соединенияха)NaCIБ)KCIOВ)CI2Г)BaCI2Д)KCIO3Е)Ca(СIO4)2 2| напигите уравнение реакции между хлором и следующисми веществамиводородом литием алюминием в?
1 / определите степень окисления хлора в следующих соединениях
Е)Ca(СIO4)2 2| напигите уравнение реакции между хлором и следующисми веществами
водородом литием алюминием водой гидроксидом натрия(без нагревания) \ ( нагреванием) во всехреакциях укажите окислитель и восстановитель.
Напишите уравнение реакций между оксидом серы и следующими веществами : а)оксидом лития ; б)водой ; в)оксидом алюминия ; г)гидроксидом натрия?
Напишите уравнение реакций между оксидом серы и следующими веществами : а)оксидом лития ; б)водой ; в)оксидом алюминия ; г)гидроксидом натрия.
Составьте уравнения окислительно — воссановительных реакции : а)натрия с хлором б)натрия с соляной кислотой?
Составьте уравнения окислительно — воссановительных реакции : а)натрия с хлором б)натрия с соляной кислотой.
Укажите окислитель и восстановитель в каждой реакции.
Напишите уравнения реакций разложения при нагревании : гидроксида алюминия?
Напишите уравнения реакций разложения при нагревании : гидроксида алюминия.
Напишите уравнение реакций лития скислородом, с серой, с водой и соляной кислотой?
Напишите уравнение реакций лития скислородом, с серой, с водой и соляной кислотой.
Укажите окислитель и восстановитель.
Напишите уравнения реакций алюминия с хлором, гидроксидом натрия и разбавленной серой кисдотой?
Напишите уравнения реакций алюминия с хлором, гидроксидом натрия и разбавленной серой кисдотой.
Для первого уравнения напишите электронный баланс, укажите окислитель и восстановитель.
Составьте уравнения окислительно — восстановительных реакций : а)натрия с хлором ; б)натрия с соляной кислотой?
Составьте уравнения окислительно — восстановительных реакций : а)натрия с хлором ; б)натрия с соляной кислотой.
Укажите окислитель и восстановитель в каждой реакции.
Напишите уравнения реакций : а) между хлором и медью ; б) между хлором и алюминием?
Напишите уравнения реакций : а) между хлором и медью ; б) между хлором и алюминием.
Укажите условия протекания этих реакций, а также окислитель и восстановитель.
Напишите уравнения реакций между : а) хлором и железом ; б)хлором и фосфором Укажите окислитель и восстановитель?
Напишите уравнения реакций между : а) хлором и железом ; б)хлором и фосфором Укажите окислитель и восстановитель.
Составьте уравнения реакций между : а)Натрием, б)калием и водородом, в) литием и хлором?
Составьте уравнения реакций между : а)Натрием, б)калием и водородом, в) литием и хлором.
Укажите окислитель и восстановитель, реакции окисления и восстановления.
На странице вопроса Напишите уравнения реакций между хлором и следующими веществами : водородом, литием, алюминием, водой, гидроксидом натрия (при нагревании и без нагревания)? из категории Химия вы найдете ответ для уровня учащихся 5 — 9 классов. Если полученный ответ не устраивает и нужно расшить круг поиска, используйте удобную поисковую систему сайта. Можно также ознакомиться с похожими вопросами и ответами других пользователей в этой же категории или создать новый вопрос. Возможно, вам будет полезной информация, оставленная пользователями в комментариях, где можно обсудить тему с помощью обратной связи.
№1 ОРБИТАЛЬ – область наиболее вероятного местонахождения электрона Ионная связь — случай поляризации ковалентной полярной связи (металл + неметалл) Валентность — способность атомов химических элементов образовывать определённое число химических связ..
S + O2 — > SO2 S(0) — 4e — > S( + 4) 1 ок — ие в — ль O2(0) + 4e — > 2O( — 2) 1 в — ие ок — ль 2SO2 + O2 — > 2SO3 SO3 + H2O — > H2SO4 H2SO4 + 2NaOH — > Na2SO4 + 2H2O.
4 — незнаю точно наверное 1 или 2 5 — г 6 — 7 — б 1500 градусов 8 — г 9 — г.
1) Дано : m(Li) = 22 н Найти : m(LiOH) Решение : 2Li + 2H2O = 2LiOH + H2 газ n(Li) = m / M M(Li) = 7 г / моль n(Li) = 22 / 7 = 3 моль По уравнению реакции : n(Li) = n(LiOH) = 3 моль m(LiOH) = n•M M(LiOH) = 7 + 16 + 1 = 24 г / моль m(LiOH) = 24•3 = 72..
2Ca + O₂ = 2CaO Ca⁰ — 2e = Ca⁺² 4 2 кальций восстановитель, процесс окисления O₂ + 4e = 2O⁻² 2 1 кислород окислитель, процесс восстановления H₂ + Cl₂ = 2HCl H₂⁰ — 2e = 2H⁺¹ 2 1 водород восстановитель, процесс окисления Cl₂⁰ + 2e = 2Cl⁻¹ 2 1 хлор окис..
Вообщем так получается . На железо вверху не смотри, это к другому))).
Никакое. O2, H2 — ковалентная неполярная CaCl2 — ионная Ba — металлическая.
Цепные реакции. Реакции галогенов друг с другом
Задача 812.
Составить схему цепной реакции хлора с водородом. Какую роль в ней играет освещение? Имеет ли значение частота света?
Решение:
Синтез HCl из Н2 и Cl2 протекает на свету:
Эта реакция относится к неразветвлённым цепным реакциям. Поглощение кванта света или другой лучистой энергии (hv) молекулой Cl2 приводит к её возбуждению – к появлению в ней энергичных колебаний атомов. И, как только энергия колебаний атомов превышает энергию связи между атомами, то молекула распадается. Формирование цепи начинается с образования радикалов:
Образующиеся атомы хлора легко реагируют с молекулой водорода с образованием молекулы хлороводорода и атома водорода:
Атом водорода, в свою очередь, легко реагирует с молекулой хлора с образованием молекулы хлороводорода и атома хлора:
Эта последовательность процесса продолжается дальше, в рассматриваемом случае число звеньев может достигать 100000. При данной фотохимической реакции частота света играет существенную роль, поскольку количество энергии кванта света определяется произведением постоянной Планка (h) и частотой света (v), получим: (hv). От численного значения частоты света зависит величина количества энергии кванта. Для распада молекулы Cl2 на 2 необходима частота света чуть больше 550 ммк. Под действием получаемого при данной частоте кванта света разрушается связь Cl — Cl, а не Н — Н, так как Е(Cl — Cl) = 243 кДж/моль, а Е(Н — Н) = 436 кДж/моль.
Таким образом, под действием света энергии кванта света (Е = hv) достаточно только для разрыва связей Cl — Cl в молекуле Cl2, а не для разрыва связей Н — Н в молекуле Н2. Именно свет является фактором, который определяет начало цепной реакции — образование свободных атомов хлора.
Задача 813.
Написать уравнения реакций взаимодействия галогенов с водой и растворами щелочей (холодными и горячими).
Решение:
а) Уравнения реакций взаимодействия галогенов с водой:
Раствор брома в воде называют «бромной водой».
б) Уравнения реакций взаимодействия галогенов с холодным раствором щёлочи:
Cl2 + 2OH— ↔ Cl — + OCl — + H2O.
в) Уравнения реакции взаимодействия галогена с горячим раствором щёлочи:
3Cl2 + 6OH — ↔ 5Cl — + OCl3 — + 3H2O.
Таким образом, при растворении галогенов в холодной воде и в холодных растворах щелочей происходит восстановление хлора до степени окисления его атома +1 и окисление галогена до степени окисления -1. В горячих растворах щелочей галоген самоокисляется и самовосстанавливается соответственно до степени окисления -1 и до степени окисления +5.
Задача 814.
Привести примеры возможных реакций галогенов друг с другом. Указать степени окисленности галогенов в продуктах реакций.
Решение:
Известны соединения галогенов друг с другом (галоиды), например: BrCl, ICl3, BrF5, IF7, ClF, ClF5 IBr и другие. Все соединения галоидов могут быть получены прямым синтезом, например:
Некоторые из галоидов могут существовать в обычных условиях и не разлагаться, например ClF (газ), BrF (жидкость), IF5 (жидкость), IF7 (газ).
Задача 815.
При 300 °С степень термической диссоциации НI составляет 20%. Каковы при этой температуре равновесные концентрации Н2 и I2 в системе
Н2 +12 ↔ 2НI, если равновесная концентрация НI равна 0,96 моль/л?
Решение:
Обозначим начальную концентрацию HI через х (моль/л). Если к моменту наступления равновесия из каждых х молей йодоводорода диссоциировано х молей,
то при этом, согласно уравнению реакции, образовалось 0,5х; моля Н2 и 0,5х моля I2.
Находим начальную концентрацию HI (х) с учетом того, что термическая диссоциация ее составляет 20% (0,2), составив соотношение:
0,96 = х — (0,96 . 0,2);
х = 0,96 + 0,192 = 1,152 моля.
Тогда равновесные концентрации Н2 и I2 с учётом того, что степень термической диссоциации НI составляет 20%, получим:
[H2] =[I2] = 0,5x . 0,2 = 0,5 . 1,152 . 0,2 = 0,1152 моля.
http://himia.my-dict.ru/q/1666778_napisite-uravnenia-reakcij-mezdu-hlorom-i/
http://buzani.ru/zadachi/khimiya-glinka/1268-tsepnaya-reaktsiya-galogeny-zadachi-839