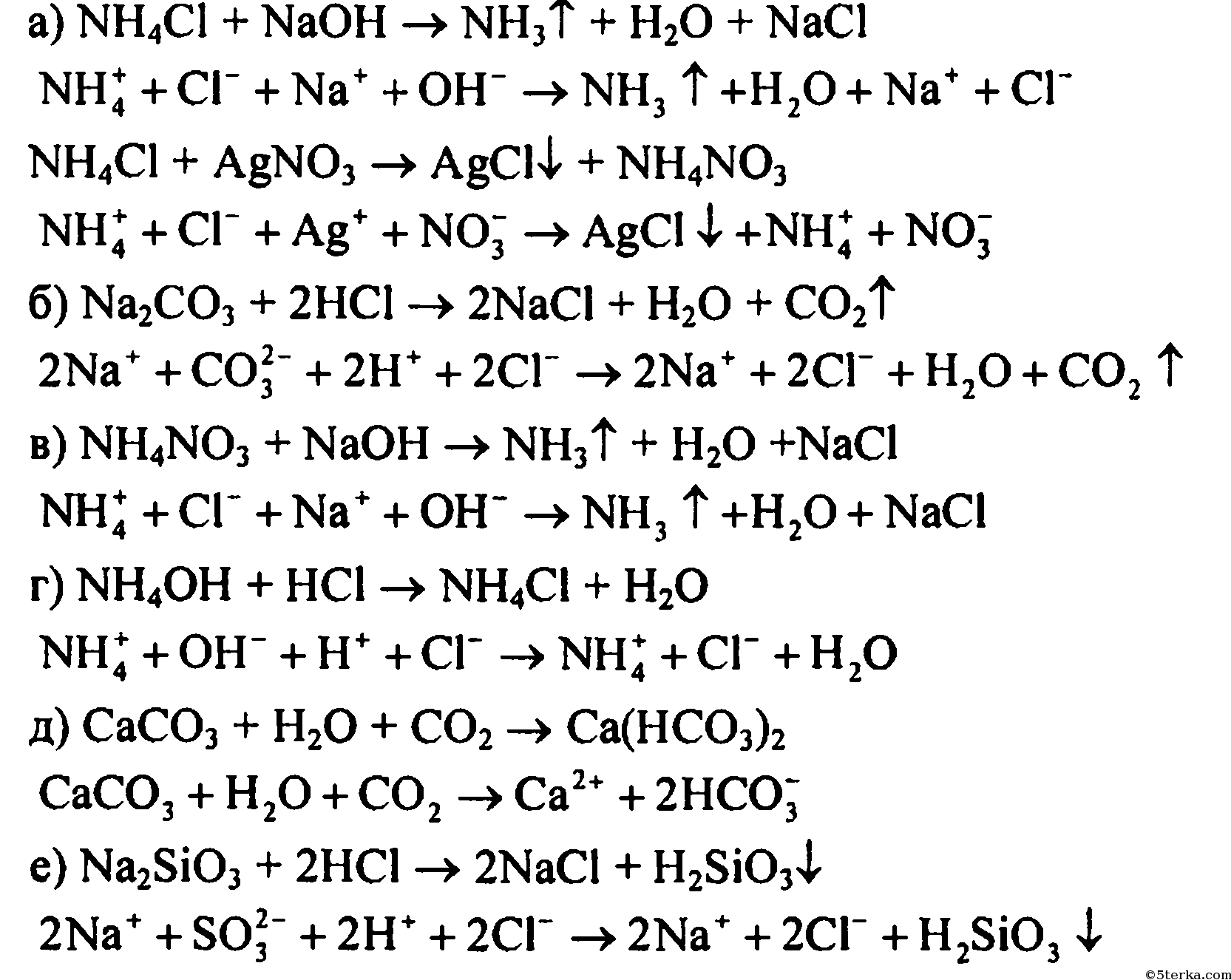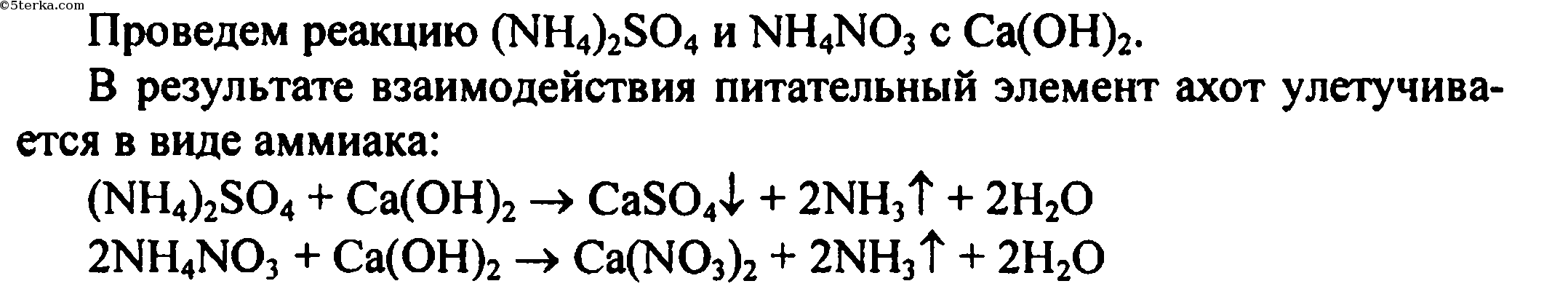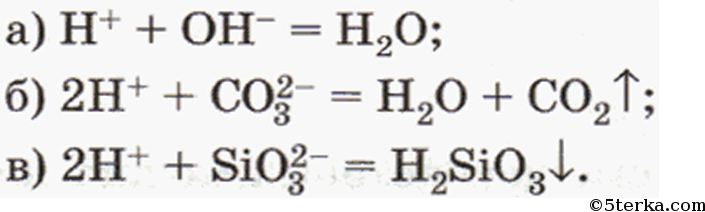Please wait.
We are checking your browser. gomolog.ru
Why do I have to complete a CAPTCHA?
Completing the CAPTCHA proves you are a human and gives you temporary access to the web property.
What can I do to prevent this in the future?
If you are on a personal connection, like at home, you can run an anti-virus scan on your device to make sure it is not infected with malware.
If you are at an office or shared network, you can ask the network administrator to run a scan across the network looking for misconfigured or infected devices.
Another way to prevent getting this page in the future is to use Privacy Pass. You may need to download version 2.0 now from the Chrome Web Store.
Cloudflare Ray ID: 6e0b8de10f519737 • Your IP : 85.95.188.35 • Performance & security by Cloudflare
Практическая работа № 5(н). Экспериментальные задачи по теме «Подгруппы азота и углерода»
Проведите реакции, с помощью которых можно доказать, что выданное вам в закрытых сосудах вещество является:
а) хлоридом аммония;
б) карбонатом натрия;
в) нитратом аммония;
г) нашатырным спиртом;
д) карбонатом кальция;
е) силикатом натрия.
Напишите уравнения проведенных реакций в молекулярном и ионном видах.
Докажите опытным путем, что сульфат аммония и нитрат аммония нельзя смешивать с известью перед внесением этих удобрений в почву, и объясните почему. Напишите уравнения реакций.
Докажите опытным путем, что:
а) в состав хлорида аммония входят ионы NH4 + и Cl — ;
б) в состав сульфата аммония входят ионы NH4 + и SO4 2- .
Напишите уравнения проведенных реакций в молекулярном и ионном видах.
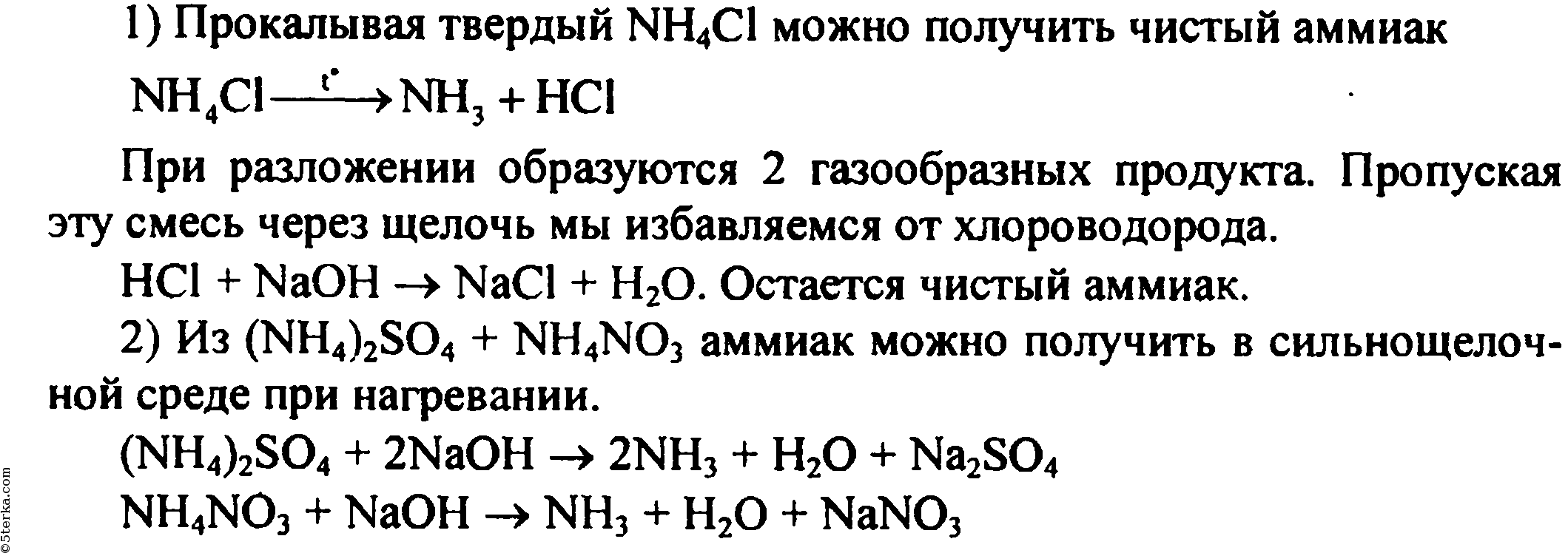
Получите аммиак из следующих солей:
а) хлорида аммония;
б) сульфата аммония;
в) нитрата аммония.
Напишите уравнения проведенных реакций в молекулярном и ионном видах.
Проведите реакции, которые выражаются сокращенными ионными уравнениями:
Напишите уравнения проведенных реакций в молекулярном и ионном видах.
В четырех пробирках вам выданы кристаллические вещества: сульфат натрия, хлорид цинка, карбонат калия, силикат натрия. Определите, какое вещество находится в каждой пробирке. Составьте уравнения реакций в молекулярном и ионном видах.

задача №5
к главе «Практические работы».
ПАМОГИТЕ с заданиями по химии !!
Задача №1
Проведите реакции , с помощью которых можно доказать , что выданное вам в закрытых сосудах вещество является :
а) хлоридом аммония ,
б)карбонатом натрия ,
в)нитратом аммония ,
г)нашатырном спиртом ,
д)карбонатом кальция ,
е)силикатом натрия ,
Напишите уравнения реакций в молекулярном и ионном видах .
Задача 2
Докажите опытным путем , что сульфат аммония и нитрат аммония нельзя смешивать с известью перед внесением этих удобрений в почву , и объясните почему . Напишите уравнения реакций .
Задача 3
Докажите опытным путем что :
а) в состав хлорида аммония входят ионы NH4 с зарядам + и CLс зарядом-
б) в состав сульфата аммония входят ионы NH4 с зарядом + и SO4 с зарядом 2-
Напишите уравнения приведенных реакций в молекуулярнном и ионном видах.
Задача 4 :
Получите аммиак из следующих солей :
а)хлорида аммония ,
б)сульфат аммония ,
в)нитрат аммония ,
Напишите уравнения проведенных реакций в молекулярном и ионных видах .
Задача 5 :
В четыреех пробирках вам выданны кристалические вещества : сульфат натрия , хлорид цинка , карбонат калия , силикат натрия . Опридилите , какое вещество находится в каждой пробирке . Составьте уровнения реакций в молекулярном и ионных видах .
Решите что сможете заранее благодарю .
Первое
NH4СL=NH3+HCl(запах аммиака при темп)
Na2CO3+CH3COOH=CH3COONa+CO2+H2O(выделение CO2)
NH4NO3=N2O+H2O
NH4OH+MgCL2=реакции нет, так как оба основания равны по силе. А также запах аммиака.
На мел такая же как на соду, мел медленно растворяется в уксусе с выделением СО2
Na2SIO3+2HCl=2NaCL+H2SIO3(SIO2+H2O)студенистый осадок
Второе
Так как сульфат гидролизуется в воде (по катиону, NH4OH-cлабое основание)
Ест-но в кислой среде известь прореагирует с серной к-той CaCO3+H2SO4=CaSO4+CO2+H2O
Тоже самое и с нитратом аммония CaCO3+2HNO3=Ca(NO3)2+H2O
Третье
А)
NH4CL=NH3+HCl(при темп, запах аммиака)
NH4CL+AgF=NH4F+AgCL(белый осадок, нерастворим в кислотах)
Б)
(NH4)2SO4+Na2CO3=Na2SO4+2NH3+CO2+H2O(карбонат аммония тут же гидролизуется нацело на CO2,H2O и аммиак)
(NH4)2SO4+BaCL2=2NH4CL+BaSO4(осадок, нерастворим в кислотах)
Четвертое
NH4CL=NH3+HCl(темп)
(NH4)2SO4+Na2CO3=Na2SO4+2NH3+CO2+H2O
2NH4NO3+Na2SIO3=2NH3+SIO2+H2O+2NaNO3
Пятое
Для начала подействуем на все эти 4 в-ва HCl
Хлорид цинка и сульфат натрия без изменений.
Карбонат прореагирует с выделением CO2,силикат с обр. студенистго осадка
K2CO3+2HCL=CO2+H2O+2KCl
CO3(2-)+2H(+)=CO2+H2O
Na2SIO3+2HCl=2NaCL+SIO2+H2O
SIO3(2-)+2H(+)=SIO2+H2O
Теперь осталось определить где сульфат а где хлорид. Для этого добавим в обе пробирки BaCL2
Хлорид не прореагирует, с сульфатом произойдет реакция
Na2SO4+BaCL2=BaSO4+2NaCl
SO4(2-)+Ba(2+)=BaSO4(осадок-нерастворимый в кислотах)
Ну и пожалуй все, все распознано.
http://5terka.com/node/10691
http://sprashivalka.com/tqa/q/23860418