Сульфат кальция: способы получения и химические свойства
Сульфат кальция CaSO4 — соль металла кальция и серной кислоты. Белый. Весьма гигроскопичный. При плавлении разлагается. Мало растворяется в воде.
Относительная молекулярная масса Mr = 136,14; относительная плотность для тв. и ж. состояния d = 2,96; tпл = 1450º C (разлагается).
Способ получения
1. В результате взаимодействия хлорида кальция и сульфата калия при 800º С образуется сульфат кальция и хлорид калия:
2. Сульфат магния взаимодействует с перхлоратом кальция с образованием сульфата кальция и перхлората магния:
3. Гидроксид кальция вступает в реакцию с серной кислотой и образует сульфат кальция и воду:
Качественная реакция
Качественная реакция на сульфат кальция — взаимодействие его с хлоридом бария, в результате реакции происходит образование белого осадка , который не растворим в азотной кислоте:
1. При взаимодействии с хлоридом бария , сульфат кальция образует сульфат бария и хлорид кальция:
Химические свойства
1. Сульфат кальция реагирует с простыми веществами :
1.1. Сульфат кальция взаимодействует с углеродом (коксом) при 900º С и образует сульфид кальция, угарный газ или углекислый газ:
CaSO4 + 4C = CaS + 4CO
2. Сульфат кальция вступает в реакцию со многими сложными веществами :
2.1. Сульфат кальция взаимодействует с оксидами :
2.1.1. Сульфат в результате реакции с угарным газом при 600 — 800º С образует сульфид кальция и углекислый газ:
CaSO4 + 4CO = CaS + 4CO2
2.2. Сульфат кальция может реагировать с кислотами :
2.2.1. При взаимодействии с концентрированной серной кислотой сульфат кальция образует гидросульфат кальция:
2.3. Сульфат кальция реагирует с солями :
2.3.1. Сульфат кальция взаимодействует с концентрированным раствором карбоната натрия . При этом образуются карбонат кальция и сульфат натрия:
3. Сульфат кальция разлагается при температуре выше 1450º С, образуя оксид кальция, оксид серы и кислород:
Реакция взаимодействия CaCl2, H2SO4
Одним из камней преткновения на первых шагах изучения химических закономерностей и основ является написание химических реакций. Поэтому вопросы о взаимодействии CaCl2, H2SO4 встречаются даже не периодически, а систематически. Разберем основные «проблемные» моменты.
Запись молекулярного уравнения
Взаимодействие между хлоридом кальция (соль) и серной кислотой протекает по обменному механизму.
- два соединения на входе (исходные вещества);
- два соединения на выходе (продукты);
- полное отсутствие простых веществ.
Обмениваясь друг с другом реакционными группами, реагенты видоизменяются, а уравнение принимает вид:
CaCl2 + H2SO4 = CaSO4 + 2HCl.
Как видно, два сложных вещества, меняясь ионами, образуют совершенно иные соединения: новую соль (CaSO4) и соляную кислоту (HCl).
Возможность протекания до конца
Ответить на сей вопрос можно запросто, записав для CaCl2, H2SO4 уравнение реакции в молекулярном виде. От вида продуктов и будет всё зависеть. До конца процесс идет в случае образования:
- труднорастворимого вещества (осадка);
- летучего соединения (газа);
- малодиссоциирущего реагента (воды, слабого электролита).
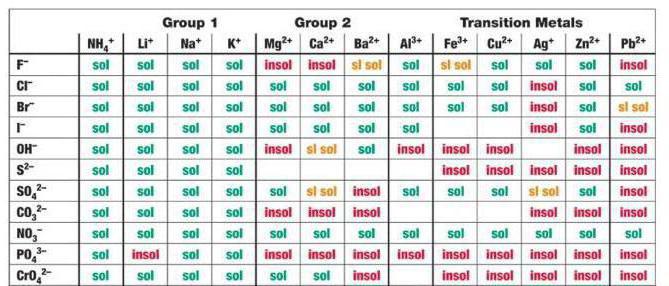
В рассматриваемом для CaCl2, H2SO4 случае среди продуктов реакции имеется сульфат кальция – малорастворимое соединение, выпадающее в осадок, согласно таблице.
Следовательно, обменный процесс пройдет до конца.
Сокращенная ионная форма записи между CaCl2, H2SO4
Расписав все растворимые соединения на ионы и сократив повторяющиеся реакционные группы, получим два искомых уравнения:
- полная ионная форма записи между CaCl2, H2SO4
ca 2+ + 2cl — + 2h + + so4 2- = caso4 + 2h + + 2cl —
- сокращенный вид уравнения
Следует помнить, что на ионы расписываются только растворимые соли, кислоты, основания (это легко определяется по специальным таблицам). Слабые электролиты типа угольной или уксусной кислоты всегда пишутся в молекулярной форме.
Теперь вы знаете, как происходит взаимодействие между хлоридом кальция (соль) и серной кислотой.
Напишите уравнения реакций кальция с кислородом, азотом, водой и разбавленной серной кислотой?
Химия | 5 — 9 классы
Напишите уравнения реакций кальция с кислородом, азотом, водой и разбавленной серной кислотой.
Кальций с кислородом : 2Ca + O2 = 2 CaO
Кальций с азотом : 3Са + N2 = Ca3N2
Кальций с водой : Ca + 2H2O = Ca(OH)2 + H2
Кальций с серной кислотой : Ca + H2SO4 = CaSO4 + H2.
Напишите уравнения реакций взаимодействия цинка с разбавленной и концентрированной серной кислотой?
Напишите уравнения реакций взаимодействия цинка с разбавленной и концентрированной серной кислотой.
Напишите уравнения реакций взаимодействия натрия с азотом, концентрированной серной кислоты и разбавленной азотной кислоты?
Напишите уравнения реакций взаимодействия натрия с азотом, концентрированной серной кислоты и разбавленной азотной кислоты.
Подберите коэффициенты методом электронного баланса.
Разбавленная серная кислотаНапишите уравнения реакций а)разбавленной серной кислоты и сульфита кальция?
Разбавленная серная кислота
Напишите уравнения реакций а)разбавленной серной кислоты и сульфита кальция.
Б) разбавленной серной кислоты и гидрокарбоната кальция.
Напишите уравнения реакций взаимодействия натрия и азота, концентрированной серной кислотой и разбавленной азотной кислотой?
Напишите уравнения реакций взаимодействия натрия и азота, концентрированной серной кислотой и разбавленной азотной кислотой.
Главное, это подобрать коэффициенты методом электронного баланса.
Напишите быстро уравнение реакции кальций + серная кислота?
Напишите быстро уравнение реакции кальций + серная кислота.
Составьте уравнения химических реакций и укажите их тип?
Составьте уравнения химических реакций и укажите их тип.
1)Оксид кальция + оксид углерода = карбонат кальция 2)Серная кислота + алюминий = сульфат алюминия + водород 3)Фосфорная кислота = вода + оксид азота(4) + кислород.
Составьте уравнения химических реакций, укажите тип реакции?
Составьте уравнения химических реакций, укажите тип реакции.
1. Алюминий + кислород 2.
Оксид калия + вода 4.
Оксид серы (IV) + вода 5.
Оксид магния + оксид азота (V) 6.
Алюминий + серная кислота 7.
Серная кислота + оксид кальция 8.
Гидроксид натрия + углекислый газ 9.
Соляная кислота + гидроксид кальция.
Напишите уравнение реакции характеризующих свойства разбавленой серной кислоты как электролита?
Напишите уравнение реакции характеризующих свойства разбавленой серной кислоты как электролита.
1. Напишите уравнения реакций кальция с кислородом, азотом, водой и разбавленной серной кислотой?
1. Напишите уравнения реакций кальция с кислородом, азотом, водой и разбавленной серной кислотой.
Для второго случая уравнения напишите электронный баланс, укажите окислитель и восстановитель.
Напишите уравнения реакций взаимодействия кальция со след веществами : азот, разбавленная серная кислота,оксид хрома (III), водой?
Напишите уравнения реакций взаимодействия кальция со след веществами : азот, разбавленная серная кислота,
оксид хрома (III), водой.
Вы открыли страницу вопроса Напишите уравнения реакций кальция с кислородом, азотом, водой и разбавленной серной кислотой?. Он относится к категории Химия. Уровень сложности вопроса – для учащихся 5 — 9 классов. Удобный и простой интерфейс сайта поможет найти максимально исчерпывающие ответы по интересующей теме. Чтобы получить наиболее развернутый ответ, можно просмотреть другие, похожие вопросы в категории Химия, воспользовавшись поисковой системой, или ознакомиться с ответами других пользователей. Для расширения границ поиска создайте новый вопрос, используя ключевые слова. Введите его в строку, нажав кнопку вверху.
1) СН3 — СН(ОН) — СН(СН3) — С(СН3)(С2Н5) — СН2 — СН3 2) СН3 — СН(ОН) — СН(С2Н5) — СН(СН3) — СН2 — СН2 — СН3 3) СН3 — СН2 — С(СН3)(СН3) — СОН 4) СН3 — СН2 — СН(С2Н5) — СН2 — СН(С2Н5) — СОН 5) СН3 — СН(СН3) — СН(СН3) — С(СН3)(С2Н5) — СН2 — СООН 6) СН3 ..
В 1 моль ортофосфата натрия содержится 69 г натрия, то 23 г его будет содержаться в 1 / 3 моль данного вещества.
Наверное так) удачи ).
Пожалуйста здесь электронный бананс можно ещё электонно — ионный написать.
HBr = H + Br H2SO4 = 2H + SO4 HNO3 = H + NO3 HClO4 = H + CLO4 H3PO4 = 3H + PO4 HMnO4 = H + MnO4 Кислоты диссоциируют на катионы водорода и анионы кислотного остатка. В растворах кислот всегда присутствуют одинаковые ионы водорода — Н( + ).
Так как если бы химию соединили с другими науками о природе, то получилась бы какая — то каша. Каждая наука изучает что — то своё.
1) Оксиды : CaO, CuO, Mn2O7, ZnO, N2O5, SO3, SO2, P2O5, Na2O, B2O3, BeO, CrO3, MnO2, Br2O5, Rb2O, PbO2 2) Основания : Cu(OH)2, LiOH, Be(OH)2, Ca(OH)2, Ba(OH)2, NaOH, KOH, Fe(OH)2, Zn(OH)2 3) Кислоты : HNO3, H2S, HCl, H2SO4, H3PO4, H2SO3, HMnO4, H3AsO..
M (Na3BO3) = (23 * 3) + 11 + (16 * 3) = 128 г \ моль.
Вроде так, но это не точно.
В) он просто не может с ним реагировать так как ничего не случиться.
http://fb.ru/article/304511/reaktsiya-vzaimodeystviya-cacl-h-so
http://himia.my-dict.ru/q/3006727_napisite-uravnenia-reakcij-kalcia-s-kislorodom/