Бензол и его гомологи
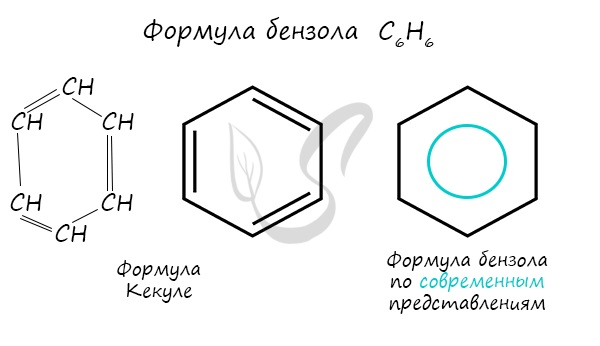
Арены — ароматические углеводороды, содержащие одно или несколько бензольных колец. Бензольное кольцо составляют 6 атомов углерода, между которыми чередуются двойные и одинарные связи.
Важно заметить, что двойные связи в молекуле бензола не фиксированы, а постоянно перемещаются по кругу.
Арены также называют ароматическими углеводородами. Первый член гомологического ряда — бензол — C6H6. Общая формула их гомологического ряда — CnH2n-6.
Долгое время структурная формула бензола оставалась тайной. Предложенная Кекуле формула с тремя двойными связями не могла объяснить то, что бензол не вступает в реакции присоединения. Как уже было сказано выше, по современным представлениям двойные связи в молекуле бензола постоянно перемещаются, поэтому более верно рисовать их в виде кольца.
За счет чередования двойных связей в молекуле бензола формируется сопряжение. Все атомы углерода находятся в состоянии sp 2 гибридизации. Валентный угол — 120°.
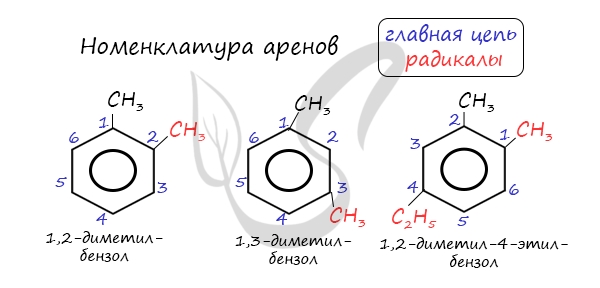
Номенклатура и изомерия аренов
Названия аренов формируются путем добавления названий заместителей к главной цепи — бензольному кольцу: бензол, метилбензол (толуол), этилбензол, пропилбензол и т.д. Заместители, как обычно, перечисляются в алфавитном порядке. Если в бензольном кольце несколько заместителей, то выбирают кратчайший путь между ними.
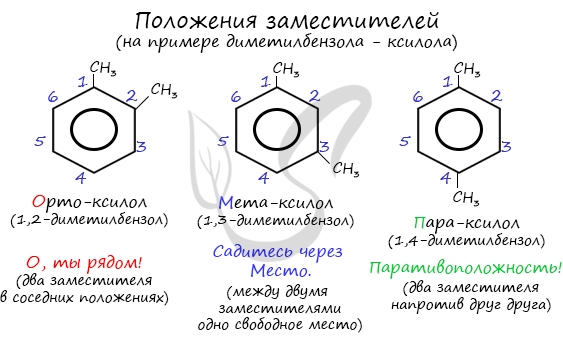
Для аренов характерна структурная изомерия, связанная с положением заместителей. Например, два заместителя в бензольном кольце могут располагаться в разных положениях.
Название положения заместителей в бензольном кольце формируется на основе их расположения относительно друг друга. Оно обозначается приставками орто-, мета- и пара. Ниже вы найдете мнемонические подсказки для их успешного запоминания 😉
Получение аренов
Арены получают несколькими способами:
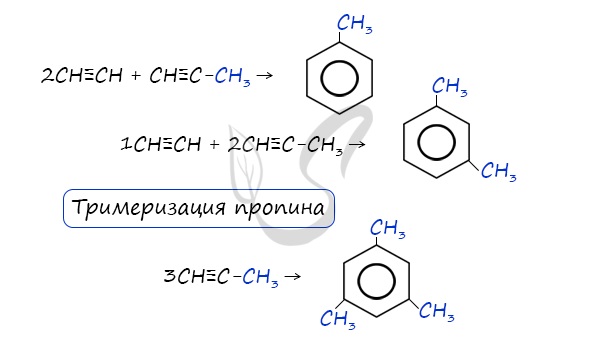
- Реакция Зелинского (тримеризация ацетилена)
Данная реакция протекает при пропускании ацетилена над активированным углем при t = 400°C. В результате образуется ароматический углеводород — бензол.
В случае, если к ацетилену добавить пропин, то становится возможным получение толуола. Увеличивая долю пропина, в конечном итоге можно добиться образования 1,3,5-триметилбензола.
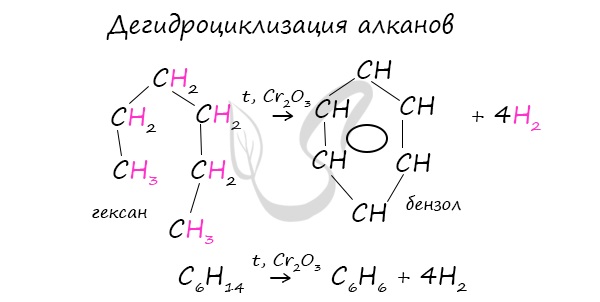
В ходе таких реакций, протекающих при повышенной температуре и в присутствии катализатора — Cr2O3, линейная структура алкана замыкается в цикл, отщепляется водород.
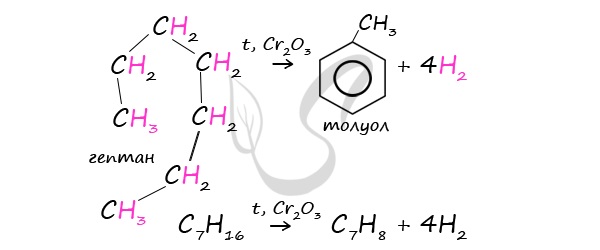
При дегидроциклизации гептана получается толуол.
В результате дегидрирования уже «готовых» циклов — циклоалканов, отщепляются 3 моль водорода, и образуется соответствующий арен, с теми же заместителями, которые были у циклоалкана.
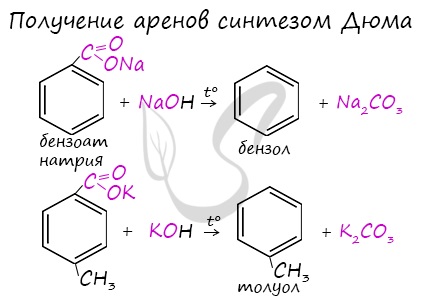
Синтез Дюма заключается в сплавлении солей карбоновых кислот с щелочами. В результате такой реакции возможно образование различных органических веществ, в том числе аренов.
Химические свойства аренов
Арены — ароматические углеводороды, которые содержат бензольное кольцо с сопряженными двойными связями. Эта особенность делает реакции присоединения тяжело протекающими (и тем не менее возможными!)
Запомните, что, в отличие от других непредельных соединений, бензол и его гомологи не обесцвечивают бромную воду и раствор перманганата калия.
При повышенной температуре и наличии катализатора, водород способен разорвать двойные связи в бензольном кольце и превратить арен в циклоалкан.
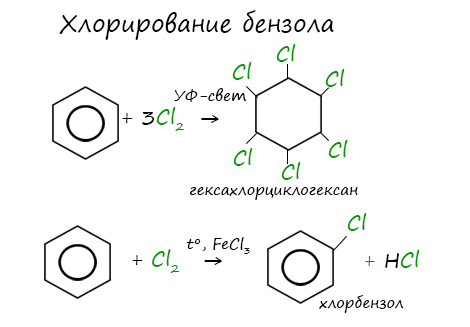
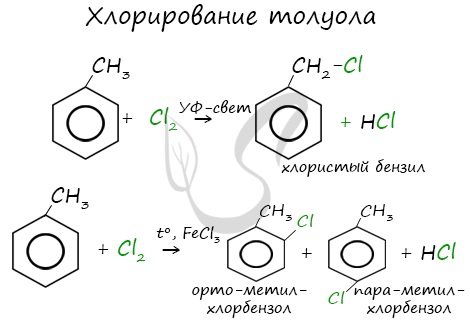
Реакция бензола с хлором на свету приводит к образованию гексахлорциклогексана, если же использовать только катализатор, то образуется хлорбензол.
Реакции с толуолом протекают иначе: при УФ-свете хлор направляется в радикал метил и замещает атом водорода в нем, при действии катализатора хлор замещает один атом водорода в бензольном кольце (в орто- или пара-положении).
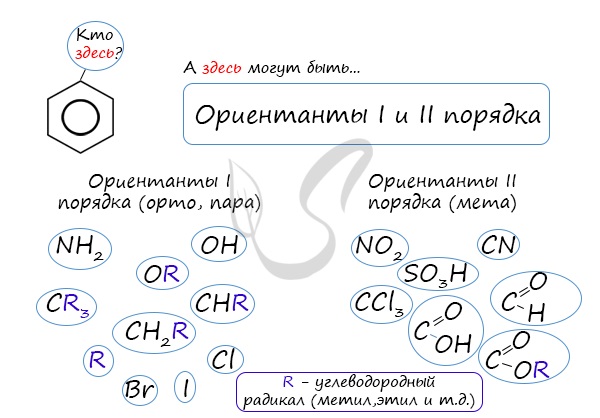
Почему хлор направляется именно в орто- и пара-положения относительно метильной группы? Здесь самое время коснуться темы ориентантов I (орто-, пара-ориентантов) и II порядков (мета-ориентанты).
К ориентантам первого порядка относятся группы: NH2, OH, OR, CR3, CHR2, CH2R, галогены. К ориентантам второго: NO2, CN, SO3H, CCl3, CHO, COOH, COOR.
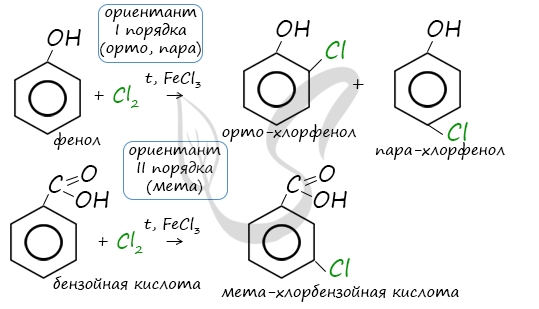
Например, ориентант I порядка, гидроксогруппа OH, обеспечивает протекание хлорирования в орто- и пара-положениях. А карбоксильная группа COOH, ориентант II порядка, обуславливает хлорирование в мета-положениях.
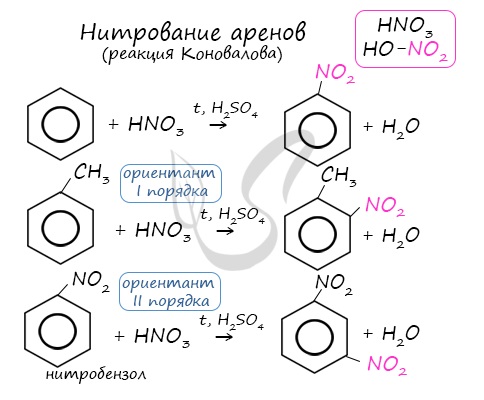
Арены вступают в реакции нитрования, протекающие при повышенной температуре и в присутствии серной кислоты, обладающей водоотнимающими свойствами.
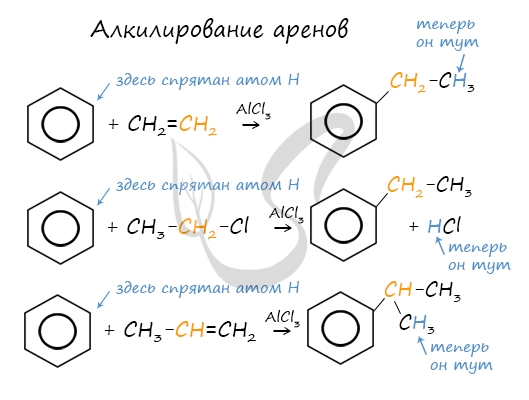
Алкилирование аренов осуществляется путем введения алкильного радикала в молекулу бензола. Алкильным радикалом чаще всего выступает алкен или галогеналкан. В подобных реакциях используют катализатор AlCl3.
В случае если для алкилирования используется алкен, то с молекулой бензола соединяется наименее гидрированный атом углерода алкена, прилежащий к двойной связи. Один атом водорода переходит из бензольного кольца к радикалу.
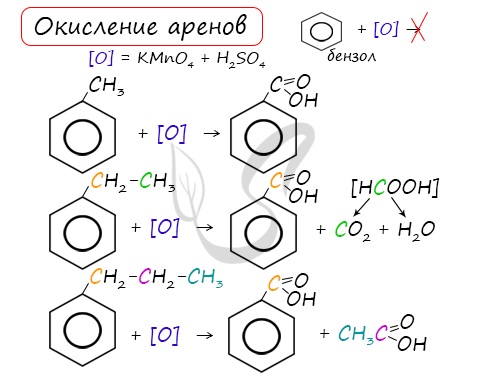
Арены, как и все органические вещества, сгорают с образованием углекислого газа и воды.
При неполном окислении гомологи бензола способны окисляться до бензойной кислоты (при подкислении раствора серной кислотой). Сам бензол не вступает в реакцию окисления с KMnO4, не обесцвечивает его раствор.
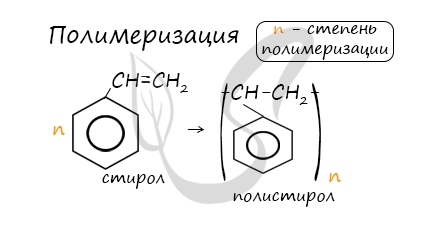
В реакцию полимеризации способен вступать стирол (винилбензол), в радикале которого содержится двойная связь.
© Беллевич Юрий Сергеевич 2018-2022
Данная статья написана Беллевичем Юрием Сергеевичем и является его интеллектуальной собственностью. Копирование, распространение (в том числе путем копирования на другие сайты и ресурсы в Интернете) или любое иное использование информации и объектов без предварительного согласия правообладателя преследуется по закону. Для получения материалов статьи и разрешения их использования, обратитесь, пожалуйста, к Беллевичу Юрию.
Что такое стирол? состав, свойства, применение
Стирол — это жидкий углеводород, известный своей невероятной способностью подвергаться полимеризации — процессу, в котором отдельные молекулы реагируют друг с другом с образованием больших трехмерных сетей или полимерных цепей.
Стирол в основном используется для производства термопластичного полимера под названием полистирол, а также ряда других пластмасс и синтетических каучуков. Этот легкий и недорогой материал обеспечивает высококачественный внешний вид, который можно разрезать на любую форму.
Профиль стирола
Химическая формула: C6H5CH=CH2
Молекулярный вес: 104,15 г/моль
Температура плавления: -30 °C
Температура кипения: 145 °C
Плотность: 0,909 г/см3
Растворимость в воде: 300 мг/л при 25 °C.
Стирол является членом углеводородной винильной группы (CH2=CH-), молекулы которой состоят из двойной связи между двумя атомами углерода.
Под действием инициаторов и катализаторов эта двойная связь может расщепляться на две одинарные связи, связывающие атом углерода другой молекулы стирола. Так образуется полистирол, в котором тысячи соединений стирола прикреплены вдоль углеродной основы.
Физические и химические свойства
Стирол представляет собой бесцветную маслянистую жидкость, которая легко испаряется. Старый образец может выглядеть слегка желтоватым. Хотя он имеет сладковатый запах, другие химические вещества могут придать ему резкий, неприятный привкус.
Хотя стирол плохо растворяется в воде, он хорошо растворяется в этаноле, эфире и ацетоне и слабо растворяется в четыреххлористом углероде. Также он образует однородную смесь с бензолом.
Стирол менее плотен, чем вода, но его пары тяжелее воздуха и раздражают глаза. Если он полимеризуется в закрытом контейнере, контейнер может разорваться на части.
Вязкость: 0,696 сП при 25 °C
Полимеризация: Постепенно при комнатной температуре и легко при температуре выше 65 °C.
Полимеризация также может происходить из-за присутствия пероксидов, окислителей или солнечного света. Чтобы предотвратить это, стирол обычно смешивают с ингибиторами. Однако это не препятствует стиролу разъедать медь и медные сплавы.
Как производится стирол?
Натуральный стирол содержится (в очень небольших количествах) в некоторых продуктах и растениях, таких как кофейные зерна, арахис, корица и бальзамические деревья. Он также содержится в каменноугольной смоле.
Однако большое количество стирола синтетически создается из этилбензола. Фактически, более 99% этилбензола, производимого во всем мире, предназначено для производства стирола. Этилбензол — легковоспламеняющаяся бесцветная жидкость, образующаяся в результате реакций Фриделя – Крафтса между этиленом и бензолом в присутствии цеолитов.
В настоящее время для производства стирола из этилбензола используются два процесса:
1. Дегидрирование этилбензола.
Около 75% стирола получают путем удаления водорода из этилбензола (C 6 H 5 CH 2 CH). Этот процесс включает нагревание этилбензола до 600 °C в присутствии катализатора, которым обычно является оксид железа (III).
Реакция поглощает значительное количество тепла (из внешней среды) и является обратимой. При этом выделяется 88-94% стирола, который затем очищается путем дистилляции.
Поскольку во время процесса стирол может подвергаться термической полимеризации, в систему постоянно добавляют ингибитор.
2. Обработка этилбензола кислородом
Реакция между этилбензолом и кислородом дает гидропероксид этилбензола. Затем этот продукт обрабатывают пропиленом для получения оксида пропилена и 1-фенилэтанола. Наконец, дегидратация 1-фенилэтанола дает стирол.
Более дешевая альтернатива
Стирол также можно получить, используя недорогое сырье: метанол (простейший спирт) и толуол (ароматический углеводород).
Реакция между этими соединениями при 425 °C и в присутствии цеолитного катализатора дает смесь стирола и этилбензола 9:1. Выход стирола более 60%.
Из коричной кислоты
В лабораториях его получают путем удаления карбоксильной группы из коричной кислоты — белого кристаллического соединения. Впервые стирол был получен именно таким способом.
Обычное использование
Ежегодно миллиарды килограммов стирола производятся промышленным способом для изготовления таких продуктов, как пищевые контейнеры, одноразовые стаканчики, пластик, резина, трубы, стекловолокно, автомобильные компоненты и различные химикаты.
Хотя стирол в основном используется для производства полистирольных пластиков и смол, он также служит промежуточным звеном в синтезе соединений, используемых для ионообменных смол.
В частности, стирол используется для производства:
Твердый полистирол, из которого делают жесткую тару для предприятий общественного питания, кухонную технику, игрушки, медицинские и оптические инструменты.
Полимерные композиты, армированные волокном, которые используются для производства коррозионно-стойких труб и резервуаров, спортивных товаров, компонентов ветряных турбин, военных и коммерческих самолетов и автомобильных запчастей.
Пенополистирол и пленки, которые используются для изготовления контейнеров для предприятий общественного питания, легкой защитной упаковки, а также для ламинирования и печати.
Самыми популярными материалами на основе стирола являются:
- АБС (акрилонитрил-бутадиен-стирол) Пластик: используется для изготовления небольших предметов домашнего обихода, игрушек и подкладок для холодильников.
- SBL (стирол-бутадиен-латекс): используется в качестве покрытия для бумажной продукции, такой как журналы и каталоги, для достижения высокого глянца и хорошей пригодности для печати.
- SAN (Стиролакрилонитрил) Пластик: используется в сантехнике, оптических волокнах и контейнерах для пищевых продуктов.
- SBR (бутадиен-стирольный каучук): каучук общего назначения, используемый в шинах, конвейерных лентах и прокладках.
Токсичность
Стирол представляет опасность при хранении при температуре выше 32 °C. При разложении (при нагревании) он выделяет едкий дым и раздражающие испарения.
Пары стирола сильно раздражают горло, нос, глаза и легкие. У работников, подвергающихся воздействию высоких уровней паров стирола, могут развиться дегенеративные заболевания нервной системы.
Длительное воздействие может привести к усталости, потере слуха, ухудшению цветового зрения, снижению концентрации, замедлению реакции и психическим проблемам. У некоторых работников наблюдались астма, аллергические кожные реакции, изменения иммунной функции и даже свертываемость крови.
Размер рынка
В 2019 году мировой рынок стирола оценивался в 48 миллиардов долларов. Прогнозируется, что к 2026 году эта цифра достигнет 70 миллиардов долларов при среднегодовом темпе роста (CAGR) в 4,6% с 2020 по 2026 год.
Постоянно растущий спрос на электронику и автомобильные компоненты — это лишь некоторые из основных факторов, способствующих росту рынка. Например, автомобильная промышленность является основным конечным потребителем SBR (бутадиен-стирольный каучук в основном используется для производства шин).
Однако растущие проблемы со здоровьем и окружающей средой при использовании стирола будут тормозить рост рынка. За последнее десятилетие были зарегистрированы различные промышленные аварии. Недавно, в мае 2020 года, в результате утечки газообразного стирола погибли тринадцать рабочих на заводе LG Chem в Висакхапатнаме, Индия.
Несмотря на вредные последствия, стирол будет пользоваться значительным спросом благодаря применению полистирола. Азиатские страны будут продолжать доминировать на рынке в течение прогнозного периода.
В частности, ожидается, что в Китае в ближайшие годы будет наблюдаться устойчивый рост из-за растущего спроса на упакованные товары в продовольственном сегменте.
Часто задаваемые вопросы
Как люди подвергаются воздействию стирола?
Стирол может попасть в организм человека при дыхании (в виде пара) или при прямом контакте с кожей. Население в целом может подвергаться воздействию при употреблении питьевой воды, употребления пищи, курения сигарет, вдыхания воздуха в помещении или использования потребительских товаров, содержащих стирол.
При попадании в окружающую среду стирол попадает в воздух с поверхности воды и влажной почвы. Небольшие количества стирола были обнаружены как в организмах, дышащих воздухом (морские птицы, хищники, люди), так и в организмах, дышащих водой (хищные рыбы).
Насколько опасен стирол?
Оксид стирола может быть канцерогенным как для человека, так и для животных. У животных он вызывает рак печени. Безопасного уровня воздействия этого газа не существует, поэтому любой контакт с ним должен быть сведен к минимально возможному уровню.
Как быстро стирол попадает в организм?
Во многих контролируемых исследованиях было установлено, что стирол задерживается в легких до 70% от вдыхаемой дозы. В окружающем воздухе он может абсорбироваться через кожу на уровне 4% от дозы, поглощенной в дыхательных путях. Более того, жидкий стирол может проникать через кожу со скоростью 1 мкг/м2 в минуту.
Как защитить себя от газообразного стирола?
Работники могут использовать средства защиты и следовать аварийным процедурам, чтобы обезопасить себя. Это включает обеспечение достаточной вентиляции и устранение всех источников воспламенения на предприятии.
Не допускайте скопления паров в небольших помещениях и предотвращайте любые утечки или проливы. Также необходимо избегать выброса продукта в окружающую среду.
Напишите уравнения реакций присоединения винилбензола
Взаимодействие стирола с хлороводородом
1) относится к реакции присоединения
2) протекает по радикальному механизму
3) протекает с разрывом -связи
4) протекает в соответствии с правилом Марковникова
5) приводит к образованию пара-хлорстирола
6) является каталитической реакцией
| ___ | ___ | ___ |
Формула стирола (винилбензола, фенилэтилена) С6H5-CH=CH2
Стирол реагирует с хлороводородом подобно алкенам.
Это реакция электрофильного присоединения по месту двойной связи (с разрывом -связи), протекает в соответствии с правилом Марковникова (водород присоединяется к наиболее гидрогенизированному атому углерода). Реакция идет без участия катализаторов.
http://new-science.ru/chto-takoe-stirol-sostav-svojstva-primenenie/
http://chem-ege.sdamgia.ru/problem?id=1853