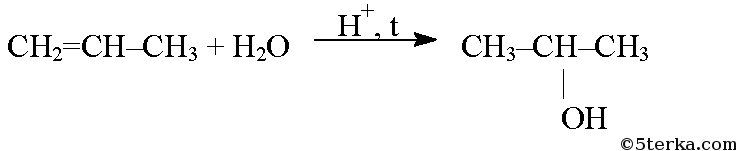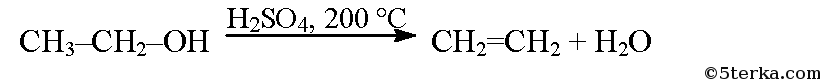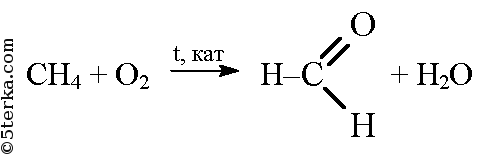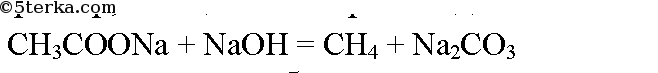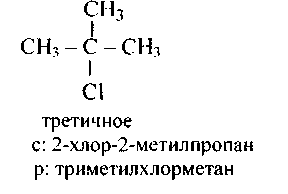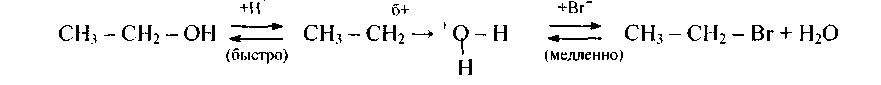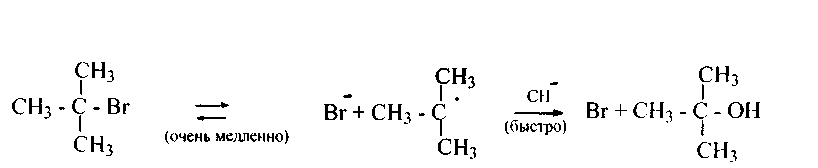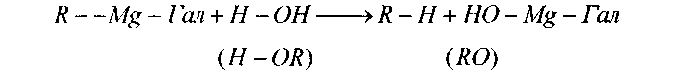№18. Согласно схеме 11 напишите уравнения соответствующих химических реакций.
Галогенопроизводные углеводородов реагируют и с натрием, при этом образуются предельные углеводороды, содержащие в молекуле вдвое больше атомов углерода, чем исходное галогенопроизводное (реакция Вюрца):
При действии на галогенопроизводные углеводородов водного раствора щелочи образуются спирты:
При взаимодействии спиртов с галогеноводородами в присутствии концентрированной серной кислоты образуются галогенопроизводные углеводородов:
При отщеплении водорода от предельных углеводородов могут образоваться углеводороды ряда этилена — алкены или углеводороды ряда ацети лена — алкины (реакция дегидрирования):
При присоединении водорода к алкенам и алкинам образуются предельные углеводороды (реакция гидрирования):
Под действием спиртового раствора щелочи от галогенопроизводных отщепляется галогеноводород, при этом образуются алкены:
При присоединении галогеноводородов к непредельным углеводородам образуются галогенопроизводные. Присоединение протекает по правилу Марковникова:
При присоединении к алкенам воды образуются спирты, реакция также протекает по правилу Марковникова.
При сильном нагревании спиртов с серной кислотой происходит дегидратация и образуются алкены:
Спирты можно окислить в альдегиды:
Можно, наоборот, восстановить альдегиды в спирты:
В результате присоединения к ацетилену воды образуется уксусный альдегид (реакция Кучерова). Это пример превращения непредельного углеводорода в альдегид.
При окислении метана кислородом в присутствии катализатора образуется метаналь (формальдегид). Это пример превращения предельного углеводорода в альдегид.
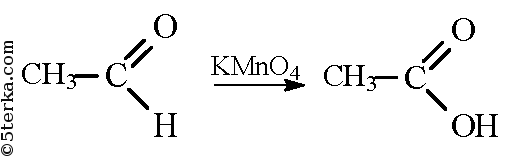
При окислении альдегидов образуются карбоновые кислоты:
Некоторые карбоновые кислоты можно получить из предельных углеводородов. Например, при окислении бутана в присутствии катализатора образуется уксусная кислота:
При нагревании солей карбоновых кислот с твердой щелочью выделяется предельный углеводород, содержащий на 1 атом углерода меньше, чем исходная кислота. Например, из ацетата натрия выделяется метан:
При взаимодействии спиртов и карбоновых кислот в присутствии катализатора, например, серной кислоты, образуются сложные эфиры.
Если нагреть смесь сложного эфира и воды в присутствии серной кислоты, то протекает обратная реакция — гидролиз сложного эфира — и образуются спирт и карбоновая кислота.

задача №18
к главе «Глава VIII. Альдегиды и карбоновые кислоты §2 Карбоновые кислоты (стр. 113) Вопросы».
1. Какие углеводороды получатся при дегидратации следующих спиртов:
а) изоамилового (СН3)2СНСН2СН2ОН;
б) втор-бутилового СН3СН2СН(ОН)СН3;
в) трет-бутилового (СН3)3СОН;
г) 2-метилнонанола-5.
Укажите, какие катализаторы используются для дегидратации и какие спирты легче дегидратируются.
2. Какие углеводороды получатся при нагревании со спиртовой щелочью следующих галогенопроизводных:
а) йодистого изобутила;
б) 2-бромпентана;
г) 3-бром-2,2-диметилпентана;
д) 4-бром-2,2-диметилпентана;
3. Напишите схемы получения:
а) 2-метилбутена-2 из 3-метил-бутена-1;
б) 2,3-диметилпентена-2 из 2-бром-3,4-диметилпентана;
в) 3-метилпентена-2 из 3-метилпентена-1.
4.Какие продукты могут быть получены при последовательном взаимодействии следующих диеновых углеводородов с двукратным избытком озона с последующим восстановительным расщеплением образовавшихся диозонидов?
а) 1,3-бутадиен;
б) 2-метил-1,3-бутадиен
5. Какие диеновые углеводороды получатся при действии цинка на следующие соединения:
а) 2,3-дибром-1-пропен;
б) 2,3-дибром-1-бутен
6. Установите строение соединения С7Н12 , обесцвечивающего раствора брома и KMnO4 , а при озонировании и разложении озонида образующего метаналь, этандиаль и 2-метилпропаналь.
7. Напишите структурные формулы следующих углеводородов:
а) 2-бутин;
б) 2-метилгексин-3;
в) трет-бутилацетилен;
г) 2,5-диметилгексин-3;
д) этил-трет-бутилацетилен;
е) диметилацетилен;
ж) 2,6,6-триметилнептин-3;
8. Предложите способ получения:
а) ацетилена из этилена;
б) 2-бутина из 2-бутена;
в) 2-бутина из 1-бутина.
Напишите уравнения реакций.
9. Напишите уравнения реакций гидратации:
а) ацетилена;
б) 1-бутина;
в) 2-бутина;
г) 1-фторпропина.
10. Определите структурную формулу углеводорода С6Н10, который при гидрировании дает 2-метилпентан, в условиях реакции Кучерова присоединяет одну молекулу воды с образованием кетона и не взаимодействует с аммиачным раствором оксида серебра.
11. Какие дигалогенпроизводные надо взять для получения приведенных ниже углеводородов:
а) диметилацетилен;
б) метилиопропилацетилен;
в) ди-трет-бутилацетилен?
VIII. ГАЛОГЕНОПРОИЗВОДНЫЕ УГЛЕВОДОРОДОВ
R(Гал)n — общая формула. Галогенопроизводные как продукты замещения водородов в углеводородах галогенами различаются:
1) по качеству галогена (F, CI, Br, I);
2) по количеству атомов галогена в молекуле (моно-, ди-, три-, тетрагалогенопроизводные и т.д.);
3) по качеству R — углеводородного радикала (предельные, непредельные, алициклические и ароматические).
Предельные моногалогензамещенные (производные алканов)
СпН2+1 — Гал — общая формула. В зависимости от места галогена в молекуле различают первичные, вторичные, третичные галогенопроизводные:

Сравнительно простые галогенопроизводные обычно называют по радикалам. Так, три вышеприведенные вещества называют соответственно: пропилхлорид, изопропилхлорид, трет-бутилхлорид.
Атом галогена является функциональной группой, обусловливающей общность свойств, характерных для данного класса соединений. Поэтому при составлении названия по систематической номенклатуре предпочтение отдают функциональной группе, а не радикалам, отходящим от основы, например.
67. Напишите формулы следующих галогенопроизводных и назовите их по рациональной и систематической номеклатурам:
а) бутилхлорид; б) втор-бутилхлорид; в) изобутилбромид; г) трет-бутилбромид; д) пентилйодид; е) 1-метилбутилйодид; ж) 1-этилпропилхлорид; з) неопентилхлорид; и) 2-метил-бутилбромид; к) трет-пентилбромид; л) втор-изопентилйодид; м) изопентилйодид.
Галогенопроизводные непредельных, алициклических, ароматических углеводородов называются по тем же правилам, что и сами углеводороды.
68. Напишите формулы следующих соединений и дайте им другие названия:
а) винилхлорид; б) аллилхлорид; в) пропенилбромид; г) изопропенилбромид; д) ацетиленилйодид; е) пропаргилйодид; ж) пропинилхлорид; э) фенилхлорид; и) бензилбромид; к) о-толилбромид; л) м-толилйодид; м) п-толилйодид.
Способы получения
1. Галогенирование, гидрогалогенирование углеводородов/
69. Напишите уравнения следующих реакций и назовите продукты. В реакции вещества взяты в эквимолярных отношениях (1:1):
а) диэтилметан + Сl2 (3 вещества); б) метилэтилметан + Сl2 (2 вещества): в) винилэтилен + С12 (2 вещества); г) триметилметан + Сl2 (2 вещества); д) хлоропрен + НС1 (3 вещества); е) изопропилацетилен+ НС1 (1 вещество); ж) изопропенилэтилен + НCl (3 вещества); з) диметилэтилметан + С12 (4 вещества).
2. Получение из спиртов.Хлор- и бромпроизводные получают взаимодействием спиртов с галогенидами фосфора, серы и галогеноводородными кислотами:
Эта реакция обратима. Чтобы равновесие сдвинулось вправо, необходимо связывать воду с помощью катализаторов ZnCI2, H2S04 конц.). Механизм нуклеофильный, ибо медленная (скорость определяющая) стадия осуществляется атакой нуклеофила:
Йодпроизводные получают действием на спирт смеси свободного йода с красным фосфором: 2P + 3I2→2PI3; PI3+3R-OH→3R-I + H3P03;
Фторпроизводные получают другими методами, например, пропусканием смеси паров углеводородов с азотом (разбавитель) через слой нагретого фторида кобальта (Ш):
Фторид кобальта (III) регенерируются фторированием образовавшегося фторида кобальта (II):
70. Напишите уравнения и условия приведенных ниже реакций и назовите продукты:
а) трет-бутиловый спирт + НСl; б) н-пентиловый спирт + SOCl2; B) трет-пентиловый спирт + РСl5; д) изопропилэтилен + НС1; е) пентен-1 + НCl; ж) 1-этилпропиловый спирт + НCl; з) 2-метил-бутиловый спирт + РС15.
Химические свойства
1. Замещение галогена на гидроксил (гидролиз) осуществляется водой, водными растворами щелочей при нагревании или свежеосажденным гидрооксидом серебра:
Вторая реакция обратимая. Для сдвига равновесия вправо галогеноводород удаляют щелочными агентами.
Легкость замещения падает в ряду йод-, бром- и хлорпроизводные, ибо соответственно растут энергии связей С — Гал (51, 65 и 81 ккал/моль), а также и в ряду третичный, вторичный и первичный галоген, вследствие возрастания индуктивных эффектов алкилов:
Механизм для первичных и вторичных галогеналканов — нуклеофильный, II порядка SN2:
для третичных- SN1 (преимущественно), ибо атака гидроксила ОН пространственно несколько затруднена и образующийся (по механизму SN1) катион третичного алкила более устойчив:
71. Приведите уравнения, условия и механизм следующих реакций: а) изобутилбромид + AgOH; б) 1-этилпропилйодид + КОН (Н20); в) аллилхлорид + Н — ОН; г) 2-хлор-З-метилбутан + КОН (Н20); д) 2-йод-2-метилпропан + Н — ОН; е) 1-бром-2-метилбутан + КОН (Н20); ж) втор-бутилхлорид + AgOH; з) изопентилйодид + AgOH; и) 2-йод-2-метилбутан + Н — ОН; к) 2-йодпентан + КОН (Н20).
2. Взаимодействие галогенопроизводных с солями неорганических и органических кислот и аммиаком (аминами)протекает при нагревании по механизму нуклеофильного замещения SN2, через активированный комплекс:
Аналогичны реакции с AgN02, NaI, NaSH, NaOR, NaOCOR и др., с помощью которых получают нитросоединения (R-N02), йодалканы (R-I), тиолы (R-SH), простые и сложные эфиры (R-O-R), (R-O-CO-R) и т.д.
72. Напишите уравнения реакций получения нитрилов, аминов, нитросоединений, йодалканов, тиолов из следующих галогенопроизводных. Приведите механизм одной из пяти реакций.
а) пропилбромид; б) 2-бром-2-метилпропан; в) втор-бутилбромид; г) изопропилхлорид; д) изобутилбромид; е) 1-бром-2-метилбутан; ж) 2-хлорпентан; з) 1-хлор-З-метилбутан; и) 2-хлор-З-метилбутан; к) 3-хлорпентан.
3. Взаимодействие галогенопроизводных с металламишироко применяется в органическом синтезе. Большое значение имеет реакция Гриньяра. Она не зависит от природы галогена (за исключением фтора — фтористые алкилы не реагируют с магнием и даже с литием) и органического радикала идет в среде абсолютного диэтилового эфира при слабом его кипении:
По-видимому, передача электрона с кристаллической решетки металла (или с поверхности капли жидкого натрия в реакции Вюрца) на углерод, связанный с галогеном, приводит к образованию свободного радикала и заряженных частиц, которые рекомбинируются по-разному:
В данном случае образуется ионная связь магний-углерод (реактив Гриньяра), в других случаях образуются углерод-углеродные σ- и π-связи в реакциях Вюрца, Вюрца-Фиттига и др.
Радикалмагнийгалогениды очень активны, устойчивы только в абсолютном эфире, небольшое присутствие соединений с подвижным водородом приводит к взаимодействию:
4. К действию окислителей галогенопроизводные довольно устойчивы. Восстановители превращают их в углеводороды:
73. Напишите уравнения следующих реакций, назовите полученные соединения:
Из других свойств галогенпроизводных следует отметить уже знакомые изученные реакции, приводящие к получению углеводородов. Это реакция дегидрогалогенирования моно- и дигалогеналканов спиртовой щелочью, дегалогенирования дигалогеналканов цинковой пылью в спирте, амальгамой лития в диоксане, реакции Вюрца, Вюрца — Фиттига, Густавсона-Фриделя-Крафтса.
IX. СПИРТЫ
R(OH)n — общая формула. Число n, показывающее количество гидроксильных групп (ОН) групп, или оксигрупп), определяет и атомность спиртов. Одноатомные, двухатомные и другие многоатомные спирты в зависимости от строения радикала могут относиться к предельным, непредельным, циклическим и ароматическим спиртам.
Последнее изменение этой страницы: 2017-05-06; Просмотров: 1358; Нарушение авторского права страницы
http://znanija.org/himiya/35581510.html
http://lektsia.com/9x597a.html