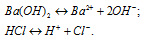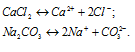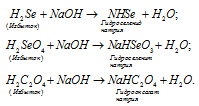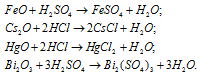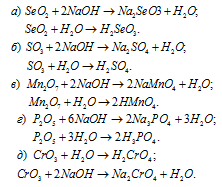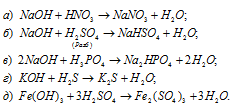Напишите уравнения реакций, свидетельствующие об основных свойствах FeO, K2O, HgO, Bi2O3, CaO?
Химия | 10 — 11 классы
Напишите уравнения реакций, свидетельствующие об основных свойствах FeO, K2O, HgO, Bi2O3, CaO.
Реакции изображены на фото.
Назовите основные химические свойства кислот напишите ионные уравнения реакции на примере одной из них?
Назовите основные химические свойства кислот напишите ионные уравнения реакции на примере одной из них.
Формулы основного и кислотного оксида соотвественно : а)FeO и Bao B)Cao , CrO3 C)P2O5, CO2 D)SO3, Cao E)Na2O , Cao?
Формулы основного и кислотного оксида соотвественно : а)FeO и Bao B)Cao , CrO3 C)P2O5, CO2 D)SO3, Cao E)Na2O , Cao.
Напишите уравнение реакции K = KOH = K2CO3 = CaCO3 = CaO?
Напишите уравнение реакции K = KOH = K2CO3 = CaCO3 = CaO.
Напишите уравнения реакций, характеризующие свойства пропанола?
Напишите уравнения реакций, характеризующие свойства пропанола.
Напишите уравнение реакции S so2 na2so3 caso3 cao?
Напишите уравнение реакции S so2 na2so3 caso3 cao.
С какими из перечисленных оксидов : CO2, CaO, FeO, SO3, MnO, SiO2 — будет реагировать гидроксид натрия?
С какими из перечисленных оксидов : CO2, CaO, FeO, SO3, MnO, SiO2 — будет реагировать гидроксид натрия?
Составьте уравнение возможных реакций.
CO + CaO — — — — — > ;PO + KO — — — — — — — > ?
Напишите уравнения химических реакций, соответствующие цепочкам превращений HgO — O2 — Al2O3?
Напишите уравнения химических реакций, соответствующие цепочкам превращений HgO — O2 — Al2O3.
1. Напишите уравнения реакций, характеризующих химические свойства натрия?
1. Напишите уравнения реакций, характеризующих химические свойства натрия.
2. Напишите уравнения реакций, с помощью которых можно осуществить следующие превращения : Ca — CaO — Ca(OH)2 — CaCO3 — CaCl2.
С какими из перечисленных веществ будет вступать в реакцию cоляная кислота?
С какими из перечисленных веществ будет вступать в реакцию cоляная кислота?
Напишите уравнения соответствующих реакций.
Pt, Fe, MgO, NaCl, KO.
На этой странице находится вопрос Напишите уравнения реакций, свидетельствующие об основных свойствах FeO, K2O, HgO, Bi2O3, CaO?. Здесь же – ответы на него, и похожие вопросы в категории Химия, которые можно найти с помощью простой в использовании поисковой системы. Уровень сложности вопроса соответствует уровню подготовки учащихся 10 — 11 классов. В комментариях, оставленных ниже, ознакомьтесь с вариантами ответов посетителей страницы. С ними можно обсудить тему вопроса в режиме on-line. Если ни один из предложенных ответов не устраивает, сформулируйте новый вопрос в поисковой строке, расположенной вверху, и нажмите кнопку.
М ( Н2О) = 1 * 2 + 16 = 18г / моль М( Al2O3) = 27 * 2 + 16 * 3 = 102 г / моль.
CH3 | CH3 — CH — C — CH2 — CH3 | | CH2 CH3 | CH3 2, 2, 3 триметилгексан СH3 | CH2 | CH3 — CH — CH2 — CH — CH — CH3 | | CH3 CH2 | CH3 2, 5 диметил 4 этил гептан СH3 | CH3 — CH2 — CH — CH — CH2 — CH2 | | CH3 CH3 3, 4 диметил гептан СH3 CH3 | | CH3 — CH..
1)Дано : (пишу в одном, в остальных аналогичное дано и найти) NH3 Найти : w(N), w(H). Решение : Mr(NH2) = 14 + 1 * 2 = 16 w(N) = 14 / 16 * 100% = 87. 4% w(H) = 2 / 16 * 100% = 12. 6% Ответ : w(N) = 87. 4%, w(H) = 12. 6% 2)Решение : Mr(H2SO4) = 1..
1) Mn — III , O — II 2) Al — III, C — IV 3)Mg — II, Br — I 4)Sn — IV, O — II 5) K — I, O — II.
4. Дано : n(C3H4) = 0. 1 моль — — — — — — — — — — — — — — — — — — — — — — — — — — — — m(C3H4) = ? V(C3H4) = ? Ответ : M(C3H4) = 40 г / моль m(C3H4) = 40 * 0. 1 = 4 г. V(C3H4) = n * Vm = 0. 1 * 22. 4 = 2. 24 л. 5. Дано : n(C4H10) = 4 моль — -..
4 — оба суждения верны.
Держи реакции на здоровье )).
C4H10 — — >C4H8 + H2 C4H8 + H2O — — >C4H9OH C4H9OH +
Дано n(Ca) = 0. 1 mol V(H2O) = 200 mL = 0. 2 L — — — — — — — — — — — — — — — — — — — — — W(Ca(OH)2) — ? N(H2O) = V / Vm = 0. 2 / 22. 4 = 0. 001 mol n(Ca) > n(H2O) m(H2O) = V(h2O) * p(H2O) = 200 * 1 = 200 g 200 X Ca + 2H2O — — >Ca(OH)2 + H2 M(h2..
Решение задач по теме «Классы неорганических соединений»
Задача 149.
Можно ли получить раствор, содержащий одновременно: а) Ва(ОН)2 и HCl; б) СаСI2 и Na2СО3; в) NaCl и AgNO3 ; г) КСI и NaNO3. Указать, какие комбинации невозможны и почему.
Решение:
а) Ba(OH)2 и HCl – сильные электролиты, поэтому в водных растворах диссоциируют полностью:
Находящиеся в растворе ионы Ba 2+ и Cl – не связываются с ионами H + и OH – с образованием осадка, газа или слабого электролита. Поэтому раствор Ba(OH)2 и HCl будет существовать.
б) Растворимые соли CaCl2 и Na2CO3 как сильные электролиты в водных растворах диссоциируют полностью по схемам:
Ионы Ca 2+ и CO3 – связываются друг с другом, образуя осадок — не растворимая соль. В растворе останутся ионы Cl – и OH – , которые не связываются друг с другом, молекулами CaCO3 и ионами воды H + и OH — . Поэтому невозможно получить раствор, содержащий одновременно CaCl2 и Na2CO3, так как выпадает осадок СаСО3.
в) NaCl и AgNO3, как сильные электролиты в водных растворах диссоциируют полностью по схемам:
Ионы Ag + и Cl — связываются друг с другом, образуя осадок AgCl. В растворе остаются ионы Na + и NO3 — , которые не связываются друг с другом с молекулами AgCl, ионами воды H+ и OH- и не образуют осадок, газ или слабый электролит. Поэтому невозможно получить раствор, содержащий одновременно NaCl и AgNO3, так как выпадает осадок AgCl.
г) КСI и NaNO3 – растворимые соли, которые в водных растворах полностью распадаются на ионы:
KCl ⇔ K + + Cl — ;
NaNO3 ⇔ Na + + NO 3 — .
Образовавшиеся ионы K + , Na + , Cl — и NO 3 — не связываются друг с другом и ионами воды H + и OH — и не образуют осадок, газ или слабодиссоциируемое вещество. Таким образом, можно получить раствор одновременно содержащий КСI и NaNO3.
Задача 150.
Какие из перечисленных кислот образуют кислые соли: HJ, H2Se, H2SeO3, H2C2O4, CH3COOH.
Решение:
Кислые соли образуют многоосновные кислоты, в которых атомы водорода не все замещены на катионы кислоты. Так как кислоты HJ и CH3COOH содержат по одному катиону водорода в составе молекул, то они не могут образовать кислых солей. Кислоты H2Se, H2SeO3, H2C2O4 являются двухосновными кислотами, то они могут образовать кислые соли при замещении одного атома водорода на катион металла. При взаимодействии этих кислот с основаниями, в случае, если кислота взята в избытке, образуется кислая соль, например:
Названия кислых солей образуются, так же как и средних, но при этом добавляют приставку «гидро» и указывают наличие незамещённых атомов водорода, число которых обозначают греческими числительными («ди», «три» и т.д.). Например: NaH2HO4 — дигидроортофосфат натрия; KH2AsO4 – дигидроортоарсенат калия; Mg(HCO3)2 – гидрокарбонат магния.
Задача 151.
Какие кислоты могут быть получены непосредственным взаимодействием с водой оксидов: Р2О5, СО2, N2O5, NO2, SO2?
Решение:
а) При взаимодействии P2O5 с водой могут образоваться различные кислоты, например метафосфорная HPO3 и ортофосфорная H3PO4:
б) При пропускании углекислого газа через воду образуется раствор слабой угольной кислоты H2CO3:
в) При растворении N2O5 в воде образуется азотная кислота HNO3 – сильный электролит.
г) при взаимодействии NO2 с водой может быть получена смесь двух кислот азотистой HNO2 и азотной HNO3:
В присутствии избытка кислорода в воде образуется только азотная кислота:
д) SO2 хорошо растворим в воде (36 об. ч. SO2 на 1 об. ч. Н2О при 20 0 С), при этом образуется сернистая кислота H2SO3 – кислота средней силы:
Задача 152.
С какими из перечисленных ниже веществ будет реагировать соляная кислота: N2O5, Zn(ОН)2, СаО, AgNO3, Н3РO3, Н2SO4? Составить уравнения реакций.
Решение:
а) Оксид азота (V) N2O5 является кислотным оксидом, поэтому не реагирует с соляной кислотой HCl.
б) гидроксид цинка Zn(ОН)2 является амфотерным основанием, поэтому реагирует как с основаниями, так и с кислотами. Реакция между Zn(ОН)2 и HCl протекает:
в) Оксид кальция СаО является основным оксидом, поэтому реагирует с соляной кислотой:
г) Нитрат серебра AgNO3 – сильный электролит, который в водных растворах диссоциирует на ионы Ag + и NO3 — , а соляная кислота как электролит распадается на ионы H + и Cl — . Ионы Ag + и Cl — , соединяясь, образуют нерастворимую соль AgCl, которая выпадает в осадок. Реакция между нитратом серебра и соляной кислотой протекает по схеме:
д) Ортофосфорная кислота Н3РO4, серная кислота H2SO4 и соляная кислота HCl – электролиты, которые в водных растворах распадаются на ионы:
Ионы PO4 3- , SO4 2- , H + и Cl — не связываются друг с другом, не образуют осадок, газ или малодиссоциируемое вещество. Поэтому Н3РO3 и Н2SO4 не реагируют с HCl.
Задача 153.
Какие из указанных веществ реагируют с гидроксидом натрия: HNO3, CaO, CO2, CuSO4, Cd(OH)2, P2O5. Составить уравнения реакций.
Решение:
а) Азотная кислота как кислота вступает в реакцию нейтрализации с основанием NaOH, при этом образуется соль и вода:
б) Оксид кальция СаО – основной оксид, поэтому не будет реагировать с NaOH – сильным основанием.
в) Оксид углерода (II) СО2 – кислотный оксид, поэтому будет реагировать с гидроксидом NaOH с образованием соли и воды:
г) CuSO4 и NaOH – сильные электролиты, поэтому в водных растворах распадаются на ионы:
CuSO4 ⇔ Cu 2+ + SO4 2- ;
NaOH ⇔ Na + + OH —
Ионы Cu 2+ и OH — связываются друг с другом, образуя осадок из нерастворимого Cu(OH)2. Значит, между CuSO4 и NaOH реакция протекает по уравнению:
д) Гидроксид кадмия Сd(OH)2 имеет слабо выраженные кислотные свойства, поэтому в растворе гидроксида натрия высокой концентрации при длительном кипячении образует неустойчивые гексагидроксокадмиат(I) – ионы [Cd(OH)6] 4- :
Сd(OH)2 + 4NaOH → Na4[Cd(OH)6]
Оксид фосфора(V) Р2О5 – кислотный оксид, поэтому будет реагировать с раствором гидроксида натрия с образованием соли и воды:
Задача 154.
Написать уравнения реакций, свидетельствующих об основных свойствах FeO, Cs2O, HgO, Bi2O3.
Решение:
Оксиды FeO, Cs2O, HgO, Bi2O3 имеют основной характер, поэтому все они растворяются в кислотах с образованием соли и воды:
Задача 155.
Написать уравнения реакций, доказывающих кислотный характер SеО2, SО3, Мn2O7, Р2O5, СrО3.
Решение:
Кислотные оксиды SеО2, SО3, Мn2O7, Р2O5 и СrО3 при взаимодействии с водой образуют соответствующие кислоты. Все они проявляют кислотные свойства, взаимодействуют как с основаниями, так и с основными оксидами:
Задача 156.
Составить уравнения реакций получения хлорида магния: а) действием кислоты на металл; б) действием кислоты на основание; в) действием кислоты на соль.
Решение:
Уравнения реакций получения хлорида магния:
а) Действием кислоты на металл:
б) Действием кислоты на основание:
в) Действием кислоты на соль:
Задача 157.
Составить уравнения реакций между кислотами и основаниями, приводящих к образованию солей: NaNO3, NaHSO4, Na2HPO4, K2S, Fe2(SO4)3.
Решение:
Уравнения реакций образования солей:
Задача 158.
Какие вещества могут быть получены при взаимодействии кислоты с солью? Кислоты с основанием? Соли с солью? Привести примеры реакций.
Решение:
а) При взаимодействии кислоты с солью могут быть получены кислота и соль, а также и другие вещества, например оксиды и вода:
б) При взаимодействии кислоты с основанием (реакция нейтрализации) образуются соль и вода:
в) Реакция между солями идёт, если при этом образуется малорастворимое соединение (реакция обмена). При взаимодействии соли с солью образуются новые соли, одна из них нерастворима:
Напишите уравнения реакций свидетельствующих об основных свойствах
Вопрос по химии:
Напишите уравнения реакций,свидетельствующих об основных свойствах FeO,Na2O,HgO,Bi2O3
Трудности с пониманием предмета? Готовишься к экзаменам, ОГЭ или ЕГЭ?
Воспользуйся формой подбора репетитора и занимайся онлайн. Пробный урок — бесплатно!
Ответы и объяснения 1
Знаете ответ? Поделитесь им!
Как написать хороший ответ?
Чтобы добавить хороший ответ необходимо:
- Отвечать достоверно на те вопросы, на которые знаете правильный ответ;
- Писать подробно, чтобы ответ был исчерпывающий и не побуждал на дополнительные вопросы к нему;
- Писать без грамматических, орфографических и пунктуационных ошибок.
Этого делать не стоит:
- Копировать ответы со сторонних ресурсов. Хорошо ценятся уникальные и личные объяснения;
- Отвечать не по сути: «Подумай сам(а)», «Легкотня», «Не знаю» и так далее;
- Использовать мат — это неуважительно по отношению к пользователям;
- Писать в ВЕРХНЕМ РЕГИСТРЕ.
Есть сомнения?
Не нашли подходящего ответа на вопрос или ответ отсутствует? Воспользуйтесь поиском по сайту, чтобы найти все ответы на похожие вопросы в разделе Химия.
Трудности с домашними заданиями? Не стесняйтесь попросить о помощи — смело задавайте вопросы!
Химия — одна из важнейших и обширных областей естествознания, наука о веществах, их составе и строении, их свойствах, зависящих от состава и строения, их превращениях, ведущих к изменению состава — химических реакциях, а также о законах и закономерностях, которым эти превращения подчиняются.
http://buzani.ru/zadachi/khimiya-glinka/1092-klassy-neorganicheskikh-soedinenij-zadachi
http://online-otvet.ru/himia/5b74966af04705552c32bc0a