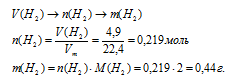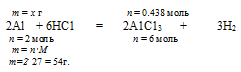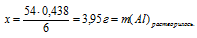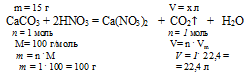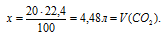Расчеты массы вещества или объема газов по известному количеству вещества, массе или объему одного из участвующих в реакции веществ
Содержание:
а) сделать запись уравнения соответствующей условию задачи реакции. Расставить правильно стехиометрические коэффициенты;
б) сделать расчёт числа молей в-ва, количество которого указано в задаче. Если речь идёт о массе какого-то в-ва (А), то применить формулу:
Если указаны объёмы газа, то вычислять по формуле:
- VA – объём газа A;
- Vm – молярный объём, равный для всех газообразных в-в при н.у. 22,4 л/моль.
Примечание. Если кол-во вещества даётся в молях, то его находить уже не требуется.
в) затем определить моли искомого в-ва (В), используя следствия из закона Авогадро –
- nA и nB – кол-во веществ А и В,
- kA и kB – коэффициенты перед ними в уравнении.
г) определив количество в-ва В, найти его массу:
для газообразного в-ва В использовать соответствующую формулу:
| Пример | |
| Условие | Сколько грамм Al2S3 нужно, чтобы при его реагировании с избытком HCl выделился газ (H2S) в объёме 33,6 литра (при н.у.). |
| Решение |
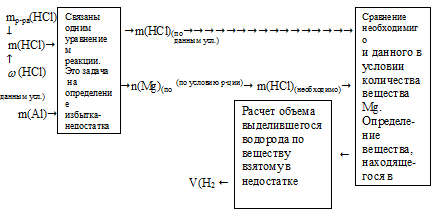
сделать расчёт кол-ва сероводорода, т.к. из условия известен его объём: используя принцип одинаковости отношений кол-ва вещества к его стехиометрическому коэффициенту в данной реакции n(Al2S3)/k(Al2S3) = n(H2S)/k(H2S), вычислить необходимое для реакции количество молей сульфида аллюминия: 4.3.3. Расчеты массы вещества или объема газов по известному количеству вещества, массе или объему одного из участвующих в реакции веществ.На данный момент задачи по этой теме кодификатора идут в КИМе ЕГЭ под номером 29. Для их решения можно воспользоваться следующим алгоритмом: 1) записать уравнение реакции, о которой идет речь в задаче, и убедиться в правильности расставленных коэффициентов; 2) рассчитать количество молей вещества, масса или объем которого указаны в условии. Если указана масса некого вещества A, то расчет количества вещества для него следует вести по формуле: Если указан объем газообразного вещества А: Иногда вместо массы или объема вещества дается его количество вещества (моль). В таком случае действия по его нахождению не требуются. 3) далее от молей вещества А нужно перейти к молям вещества, массу или объем которого спрашивают в условии. Допустим спрашивают объем или массу вещества B. Тогда для перехода от количества моль вещества А к количеству моль вещества B следует пользоваться тем правилом, что для любого вещества его количество, деленное на его коэффициент, в уравнении реакции одно и то же. Т.е. количества веществ А и В связаны друг с другом через коэффициенты в уравнении следующим образом: где n(A) и n(B) – количества вещества А и В соответственно, а k(A) и k(B) – коэффициенты в уравнении перед этими веществами. Из этого выражения следует, что количество вещества В равно: 4) далее, зная количество вещества B, мы можем найти его массу по формуле: Если же вещество B является газом и спрашивают его объем, то рассчитать его можно следующим образом: В общем, последовательность решения таких задач можно изобразить следующей схемой: 1) Зная массу или объем вещества A, рассчитываем его количество вещества. 2) Зная количество вещества A, рассчитываем количество вещества B по формуле: где n(A) и n(B) – количества веществ А и В соответственно, а k(A) и k(B) – коэффициенты в уравнении перед этими веществами. 3) В зависимости от того, требуется найти массу вещества В или объем газа В, умножаем его количество либо на молярную массу, либо на молярный объем газа: ПримерКакая масса сульфида алюминия потребуется для того, чтобы в результате его взаимодействия с избытком соляной кислоты образовался газ объемом 33,6 л (н.у.). Решение:1) Запишем уравнение реакции: 2) Рассчитываем количество вещества, для которого известна его масса или объем (в случае газа). Нам известен объем сероводорода, рассчитаем его количество вещества: 3) Отношение количества вещества любого фигуранта реакции к его коэффициенту в уравнении этой реакции всегда одно и то же. Т.е. для сульфида алюминия и сероводорода мы можем записать, что: Из этого выражения выразим n(Al2S3): Подставим известные значения n(H2S) и коэффициентов перед H2S и Al2S3: Тогда масса сульфида алюминия будет равна: Задачи с реальных экзаменов ЕГЭ на тему «Расчеты массы вещества или объема газов по известному количеству вещества, массе или объему одного из участвующих в реакции веществ» можно порешать здесь. Определение объема выделившегося газа в реакции, если одно вещество взято в избыткеОпределение избытка-недостатка Задача 6. Сначала необходимо определить, какое вещество будет в недостатке. По нему можно рассчитать объем выделившегося водорода. Алгоритм вычисления массы конечного раствора зависит от того, какое вещество окажется в избытке, поэтому отразить эту часть решения заранее невозможно. Алгоритм вычисления массы конечного раствора зависит от того, какое вещество окажется в избытке. В большинстве задач на определение избытка-недостатка при растворении металла в растворе в недостатке оказывается именно металл. В этом случае масса конечного раствора определяется очень просто: Если же металл окажется в избытке, то его излишек не будет входить в состав конечного раствора, а опустится на дно сосуда. Поэтому отразить весь алгоритм решения заранее невозможно. Схематично алгоритм первой части решения будет иметь вид: 1. Определяем массу НС1 в 200 г 8% -ного исходного раствора. 2. Определяем количество веществ НС1 и А1. 3. Выберем за основу алюминий, и определим по уравнению реакции количество вещества НС1, которое необходимо для полного растворения всего (0,296 моль) алюминия. Составляем пропорцию: 4 .Определим, какое вещество дано в недостатке. n(НС1) дано по условию 0,888моль > 0,438 моль В реакции участвует меньше НС1, чем необходимо для полного растворения А1, следовательно, НС1 дано в недостатке. В процессе реакции НС1 израсходуется полностью, а А1 расходуется не весь и часть его останется после реакции. 5. Рассчитаем по уравнению реакции объем (н.у.) выделившегося водорода. Для расчета используем НС1, т.к. это вещество взято в недостатке. Составляем пропорцию: 6. Определим массу выделившегося Н2 по алгоритму: 7. Определяем массу раствора после реакции. При определении массы конечного раствора нужно учитывать, что алюминий находился в избытке, и часть его осталась после реакции в неизменном виде. Не прореагировавший алюминий, очевидно, не входит в состав раствора и будет находиться на дне. Поэтому нам придется определить массу растворившегося А1. Это можно сделать по уравнению реакции, используя данные по НС1. Составляем пропорцию: Теперь возможно определить массу конечного раствора: mкон. р-ра = 200 + 3,95 – 0,44 = 203,51 г. Ответ: объем выделившегося водорода — 4,9 л; масса конечного раствора 203,51 г. Определение объема образовавшегося углекислого газаЗадача 7. Определим объем образовавшегося углекислого газа из пропорции: Ответ: V(CO2) = 4, источники: http://scienceforyou.ru/teorija-dlja-podgotovki-k-egje/raschety-massy-veshhestva-ili-obema-gazov-po-dannym-dlja-drugogo-uchastnika-reakcii http://buzani.ru/zadachi/ege-khimiya/1050-opredelenie-ob-ema-vydelivshegosya-gaza-zadachi-6-7 |
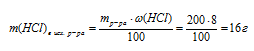
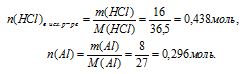
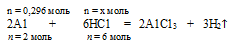
 НС1 должно расходоваться на 0,296 моль А1.
НС1 должно расходоваться на 0,296 моль А1.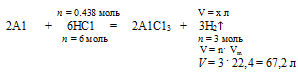
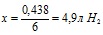 выделится в процессе реакции.
выделится в процессе реакции.