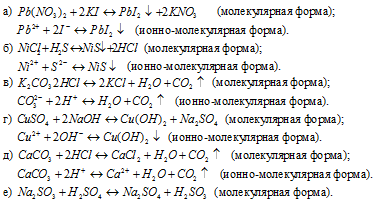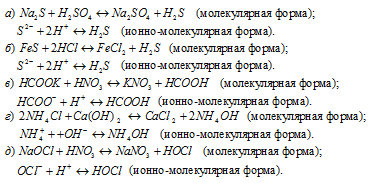Nh4br ba oh 2 ионное уравнение
Опубликовано 09.06.2017 по предмету Химия от Гость >>
Ответ оставил Гость
BaCl2 + Na2Co3 = BaCO3↓ + 2NaCl
Ba2+ + 2Cl- + 2Na+ + CO3 2- = BaCO3↓ + 2Na+ + 2Cl-
Ba2+ + CO3 2- = BaCO3↓
Na2SO3 + 2HI = 2NaI + H2O + SO2
2Na+ + SO3 2- + 2H+ + 2I- = 2Na+ + 2I- + H2O + SO2
2H+ + SO3 2- = H2O + SO2
Ba(OH)2 + 2HNO3 = Ba(NO3)2 + 2H2O
Ba2+ + 2OH- + 2H+ + 2NO3- = Ba2+ + 2NO3- + 2H2O
NH4Br + AgNO3 = AgBr↓ + NH4NO3
NH4+ + Br- + Ag+ + NO3- = AgBr↓ + NH4+ + NO3-
H2SO4 + NaBr = не взаимодействует, т.к. не образуется осадка или газа
FeCO3 + 2HCl = FeCl2 + H2O + CO2
FeCO3 + 2H+ + 2Cl- = Fe2+ + 2Cl- + H2O + CO2
FeCO3 + 2H+ = Fe2+ + H2O + CO2
Na2S + MgCl2 = не взаимодействует, т.к. не образуется осадка
2Al(OH)3 + 3H2SO4 = Al2(SO4)3 + 6H2O
3Al(OH)3 + 6H+ + 3SO4 2- = 2Al3+ + 3SO4 2- + 6H2O
3Al(OH)3 + 6H+ = 2Al3+ + 6H2O
Al2O3 + 3H2SO4 = Al2(SO4)3 + 3H2O
Al2O3 + 6H+ + 3SO4 2- = 2Al 3+ + 3SO4 2- + 3H2O
Al2O3 + 6H+ = 2Al 3+ + 3H2O
CaSO3 + 2HCl = CaCl2 + H2O + SO2
CaSO3 + 2H+ + 2Cl- = Ca2+ + 2Cl- + H2O + SO2
Сокращенное ионное уравнение: 1. NH4+ + OH- = NH3↑ + H2O; 2. Ba2+ + SO42- = BaSO4↓
Ваш ответ
решение вопроса
Похожие вопросы
- Все категории
- экономические 43,299
- гуманитарные 33,622
- юридические 17,900
- школьный раздел 607,247
- разное 16,834
Популярное на сайте:
Как быстро выучить стихотворение наизусть? Запоминание стихов является стандартным заданием во многих школах.
Как научится читать по диагонали? Скорость чтения зависит от скорости восприятия каждого отдельного слова в тексте.
Как быстро и эффективно исправить почерк? Люди часто предполагают, что каллиграфия и почерк являются синонимами, но это не так.
Как научится говорить грамотно и правильно? Общение на хорошем, уверенном и естественном русском языке является достижимой целью.
Cоставление ионно-молекулярных форм уравнений реакций
Задача 580.
Написать в ионно-молекулярной форме уравнения реакций, приводящих к образованию малорастворимых осадков или газов: 
Решение:
Так как реакция протекает с образованием сернистой кислоты – слабого электролита и при этом не выпадает осадок и не выделяется газ, то, по условию задачи, ионно-молекулярное уравнение не пишем.
Задача 581.
Написать в ионно-молекулярной форме уравнения реакций, приводящих к образованию малодиссoциированных соединений: 
Решение:
Задача 582.
Написать в ионно-молекулярной форме уравнения реакций нейтрализации: 
Указать, какие из этих реакций протекают обратимо, а какие необратимо.
Решение:
а) 2HCl + Ba(OH)2 ⇔ BaCl2 + 2H2O (молекулярная форма);
2H + + 2OH — ⇔ 2H 2 O (ионно-молекулярная форма).
Реакция протекает до конца, так как в реакцию вступают сильные электролиты соляная кислота и гидроксид бария образуется слабый электролит вода.
б) HF + KOH ⇔ KF + H2O (молекулярная форма);
H + + OH — ⇔ H2O (ионно-молекулярная форма).
В реакции участвуют два слабых электролита фтороводород и вода, согласно принципу Ле Шателье, равновесие реакции будет смещено в сторону более слабого электролита, т.е. вправо в сторону образования воды. Реакция обратима.
в) Fe(OH)3 + 3HNO3 ⇔ Fe(NO3)3 + 3H2O (молекулярная форма);
3H + + 3OH — ⇔ 3H2O (ионно-молекулярная форма).
В реакции участвуют слабое малорастворимое основание и сильная кислота, равновесие будет смещено в сторону образования более слабого электролита воды. Реакция будет протекать до конца.
г) CH3COOH + NH4OH ⇔ CH3COONH4 + H2O (молекулярная форма);
H + + OH — ⇔ H2O (ионно-молекулярная форма).
Реакция обратима, так как в реакции участвуют три слабых электролита уксусная кислота, гидроксид аммония и вода. Согласно принципу Ле Шателье равновесие системы будет смещено в сторону образования самого слабого электролита, вправо, в сторону образования воды.
д) HNO2 + NH4OH ⇔ NH4NO2 + H2O (молекулярная форма);
H + + OH — ⇔ H2O (ионно-молекулярная форма).
Реакция обратима, так как в реакции участвуют три слабых электролита уксусная кислота, гидроксид аммония и вода. Согласно принципу Ле Шателье равновесие системы будет смещено в сторону образования самого слабого электролита, вправо, в сторону образования воды.
е) H2S + 2NH4OH ⇔ (NH4)2S + 2H2O (молекулярная форма);
2H + + 2OH — ⇔ 2H2O (ионно-молекулярная форма).
Реакция обратима, так как в реакции участвуют три слабых электролита сероводородная кислота, гидроксид аммония и вода. Согласно принципу Ле Шателье равновесие системы будет смещено в сторону образования самого слабого электролита, вправо, в сторону образования воды.
Таким образом, реакции нейтрализации, в которых участвуют слабые кислоты или основания, — обратимы, т.е. могут протекать как в прямом так и в обратном направлении.
http://www.soloby.ru/991325/%D1%81%D0%BE%D0%BA%D1%80%D0%B0%D1%89%D0%B5%D0%BD%D0%BD%D0%BE%D0%B5-%D0%B8%D0%BE%D0%BD%D0%BD%D0%BE%D0%B5-%D1%83%D1%80%D0%B0%D0%B2%D0%BD%D0%B5%D0%BD%D0%B8%D0%B5-nh4-oh-nh3%E2%86%91-h2o-ba2-so42-baso4%E2%86%93
http://buzani.ru/zadachi/khimiya-glinka/1194-ionno-molekulyarnaya-forma-uravneniya-zadachi-580-582