Выражения молекулярных и ионно-молекулярных уравнений реакций
Задача 584.
Написать в ионно-молекулярной форме уравнения реакций взаимодействия между водными растворами следующих веществ:
a) NaHCO3 + HCl ⇔;
б) FeCl3 + 3KOH ⇔;
в) Pb(CH3COO)2 + Na2S ⇔;
г) 2КHS + H2SO4 ⇔;
д) Zn(NO3)2 + 2KOH ⇔;
е) Са(ОН)2 + СО2⇔;
ж) Са(ОН)2 + СО2(избыток) ⇔.
Для каждого случая указать причину смещения равновесия в сторону прямой реакции.
Решение:
a) NaHCO3 + HCl ⇔ NaCl + H2O + CO2↑;
HCO3 — + H + ⇔ H2O + CO2↑.
Равновесие системы смещено в сторону прямой реакции, потому что при реакции образуется неустойчивая угольная кислота, которая в водных растворах распадается на углекислый газ и воду:
б) FeCl3 + 3KOH ⇔ Fe(OH)3↓ + 3H2O;
Fe 3+ + 3OH — ⇔ Fe(OH)3↓.
Равновесие системы смещено в сторону прямой реакции, потому что при реакции образуется малорастворимое вещество Fe(OH)3.
Равновесие системы смещено в сторону прямой реакции, потому что при реакции образуется малорастворимое вещество PbS.
Равновесие системы смещено в сторону образования малодиссциируемого электролита H2S.
В результате реакции образуется малорастворимое вещество гидроксид цинка, поэтому равновесие системы сместится вправо.
Равновесие реакции смещено вправо, потому что образуется малорастворимое вещество карбонат кальция.
2ОН — +2СО 2– ⇔ НСО3 — .
При избытке углекислого газа карбонат кальция превращается в гидрокарбонат кальция. В данной реакции при избытке углекислого газа в растворе происходит реакция:
Хотя при данном процессе образуется электролит, но равновесие реакции всё же смещено вправо, потому что согласно принципу Ле Шателье, равновесие системы при избытке углекислого газа будет смещено в сторону уменьшения его концентрации, действительно при постоянном подведении углекислого газа в систему осадка не образуется.
Задача 585.
Какие из перечисленных ниже солей подвергаются гидролизу: NaCN, KNO3, KOCl, NaNO2, CH3COONH4, CaCl2, NaClO4, HCOOK, KBr? Для каждой из гидролизующихся солей написать уравнение гидролиза в ионно-молекулярной форме и указать реакцию ее водного раствора.
Решение:
a) NaCN — соль сильного основания и слабой кислоты, поэтому гидролиз соли проходит по аниону:
CN — + H2O ⇔ HCN + OH — .
При гидролизе образуется дополнительное количество ионов OH-, которые придают раствору щелочную среду, рН > 7.
б) KNO3 — соль сильного основания и сильной кислоты, поэтому гидролизу не подвергается. рР = 7, реакция среды нейтральная.
в) KOCl — соль сильного основания и слабой кислоты, поэтому гидролиз соли проходит по аниону:
ClO — + H2O ⇔ HOCl + OH —
При гидролизе соли образуется дополнительное количество ионов OH-, которые придают раствору щелочную среду, рН > 7.
г) NaNO2 — соль сильного основания и слабой кислоты, поэтому гидролиз соли проходит по аниону:
При гидролизе образуется дополнительное количество ионов OH-, которые придают раствору щелочную среду, рН > 7.
д) CH3COONH4 — соль слабого основания и слабой кислоты, поэтому гидролиз протекает как по катиону, так и по аниону:
Так как K(NH4OH) ()= K(CH3COOH) = 1.8 . 10 -5 , то гидролиз соли равномерно протекает как по катиону, так и по аниону, т.е. содержание ионов H+ и OH- примерно одинаково, поэтому рН ((= 7. Реакция среды нейтральная.
е) CaCl2, NaClO4 и KBr являются солями сильных оснований и сильных кислот, поэтому гидролиз этих солей не протекает и, реакция их растворов будет нейтральной, рН = 7.
ж) HCOOK — соль сильного основания и слабой кислоты, поэтому гидролиз соли протекает по аниону:
HCOO — + H2O ⇔ HCOOH + OH —
При гидролизе соли образуется дополнительное количество ионов OH-, которые придают раствору щелочную среду, рН > 7.
Гидролиз солей слабых оснований и слабых кислот.
В этом случае в реакции одновременно участвуют и катион, и анион соли, связывающие ионы OH — и H + из воды.
В качестве примера рассмотрим гидролиз соли CH3COONH4.Уравнение диссоциации соли:
Краткое ионное и молекулярное уравнения реакции гидролиза:
Значение рН растворов таких солей зависит от относительной силы кислоты и основания, образующих соль. Константы диссоциации уксусной кислоты и гидроксида аммония равны: 
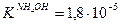
если 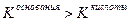
если 
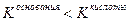
если 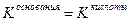
Соли многоосновных слабых кислот и многокислотных слабых оснований гидролизованы в растворе полностью, с образованием кислоты и основания:
Такие соли в водных растворах существовать не могут.
Частные реакции катионов первой аналитической группы
Читайте также:
|
| Ион | Реагент | Условия проведения реакции | Уравнение реакции в молекулярном и ионном виде | Внешний эффект реакции | Вывод |
Реакции обнаружения катиона калия К +
1. Гидротартрат натрия NaHC4H4O6,или винная кислота,в присутствии ацетата натрия при достаточной концентрации ионов калия К + в растворе дает белый кристаллический осадок гидротартрата калия:
Осадок растворяется в сильных кислотах и щелочах, поэтому реакцию проводят в нейтральной или слабокислой средах:
Реакцию следует проводить при охлаждении под струей водопроводной воды, так как растворимость осадка гидротартрата калия КНС4Н4О6 повышается при увеличении температуры.
Для ускорения выпадения осадка стенки пробирки потирают стеклянной палочкой для образования центров кристаллизации.
Реакция протекает при больших концентрациях ионов калия К + и является малочувствительной. Ионы аммония NH + 4 мешают определению ионов калия К + из-за того, что тоже дают белый кристаллический осадок с этими реагентами и поэтому соли аммония предварительно разлагают при нагревании.
Реакция является фармакопейной.
2. Гексанитрокобальтат (III) натрия Na3[Co(NO2)6] в нейтральном или слабокислом растворе с ионом калия К + дает желтый кристаллический осадок гексанитрокобальтата (III) калия-натрия:
В щелочной среде реакцию обнаружения К + проводить нельзя, так как в этой среде гексанитрокобальтат (III) натрия разлагается с образованием гидроксида кобальта (III) бурого цвета:
В сильных кислотах осадок K2Na[Co(NO2)6] растворяется с образованием нестойкой кислоты гексанитрокобальтата (III) водорода H3[Co(NO2)6].
Реакцию обнаружения ионов калия следует проводить в отсутствии ионов NH4 , так как последние дают аналогичный осадок с Na3[Co(NO2)6]. Рассматриваемая реакция обнаружения иона калия более чувствительна, чем реакция с гидротартратом натрия и является также фармакопейной.
3. Окрашивание пламени. При выполнении этой реакции платиновую проволочку, впаянную в стеклянную палочку, смачивают хлороводородной кислотой и вносят в бесцветное пламя горелки. Прокаливают до тех пор, пока окрашивание пламени не прекратится. Затем раскаленной проволокой касаются мелкого порошка или опускают ее в раствор соли калия и снова вносят в бесцветное пламя горелки. Если в образце или растворе присутствуют ионы калия, то пламя горелки окрашивается в фиолетовый цвет. Присутствие ничтожных следов натрия, окрашивающего пламя в желтый цвет, маскирует окраску.
Эта реакция используется при анализе фармацевтических препаратов.
Реакции обнаружения катиона натрия Na +
1. Гексагидроксостибиат калия K[Sb(OH)6] образует с ионом натрия белый кристаллический осадок гексагидроксостибиат (V) натрия:
Обнаружение иона Na + с помощью гексагидроксостибиата (V) калия проводят в нейтральном или слабощелочном растворе, так как кислоты разлагают реагент:
образуя белый аморфный осадок метасурьмяной кислоты. Щелочи растворяют осадок Na[Sb(OH)6] с образованием хорошо растворимой средней соли:
Соли аммония, дающие в результате гидролиза кислую реакцию среды, также разлагают исходный реактив с образованием метасурьмяной кислоты. Поэтому добиваются отсутствия в растворе ионов NH + 4 до определения в нем ионов К + .
Для образования центров кристаллизации и скорейшего выпадения осадка гексагидроксостибиата (V) натрия реакцию проводят при охлаждении и потирают стенки пробирки стеклянной палочкой.
2. Микрокристаллоскопическая реакция. Ацетат уранила UO2(CH3COO)2 образует в уксуснокислой среде с солями натрия желтоватые кристаллы уранилацетата натрия Na[(UO2)(CH3COO)3]:
При выполнении реакции раствор соли натрия выпаривают досуха и обрабатывают ацетатом уранила. Выпавшие кристаллы имеют форму желтоватых тетраэдров (или октаэдров) под микроскопом ( рис. 8.1).
Рис. 8.1. Кристаллы уранилацетата натрия
Реакция используется в фармакопее.
3. Окрашивание пламени. Соли натрия окрашивают бесцветное пламя горелки в желтый цвет. Реакция очень характерна и является фармакопейной.
Установить присутствие натрия в исследуемом веществе по окрашиванию бесцветного пламени можно только тогда, когда желтая окраска пламени сохраняется 25-30 с.
Реакции обнаружения катиона аммония NH + 4
1. Щелочи NaOH и КОН разрушают аммонийные соли с выделением аммиака:
Выделяющийся аммиак можно обнаружить с помощью влажной красной или фиолетовой лакмусовой бумажки. Образующиеся по реакции
гидроксид-ионы ОН — изменяют окраску лакмуса в синий цвет. Подобную реакцию можно провести в газовой камере (см. рис. 7.8). При большой концентрации выделяющегося аммиака его можно обнаружить и по запаху. Реакция фармакопейная.
2. Реактив Несслера (смесь K2[HgI4] и КОН). Этот реактив дает с аммонийными солями красно-бурый осадок:
При очень малых количествах солей аммония вместо осадка образуется желтый раствор; при большом их количестве — осадок растворяется. Реакция очень чувствительна. Ионы калия и натрия не мешают определению ионов аммония.
Дата добавления: 2014-11-13 ; просмотров: 58 ; Нарушение авторских прав
http://helpiks.org/4-60635.html
http://lektsii.com/1-6402.html


