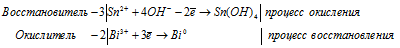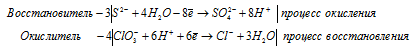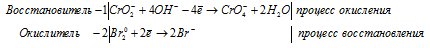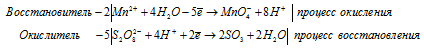Please wait.
We are checking your browser. gomolog.ru
Why do I have to complete a CAPTCHA?
Completing the CAPTCHA proves you are a human and gives you temporary access to the web property.
What can I do to prevent this in the future?
If you are on a personal connection, like at home, you can run an anti-virus scan on your device to make sure it is not infected with malware.
If you are at an office or shared network, you can ask the network administrator to run a scan across the network looking for misconfigured or infected devices.
Another way to prevent getting this page in the future is to use Privacy Pass. You may need to download version 2.0 now from the Chrome Web Store.
Cloudflare Ray ID: 6e28f6038832716e • Your IP : 85.95.188.35 • Performance & security by Cloudflare
Составление уравнений окислительно-восстановительного процесса в молекулярной и ионной форме
Задача 640.
Закончить уравнения реакций, записать их в ионно-молекулярной форме:
а) BiCl3 + SnCl2 + KOH → Bi +
б) NaClO3 + H2S → H2SO4 +
в) KCrO2 + Br2 + KOH →
г) MnSO4 + (NH4)2S2O8 + H2SO4 → HMnO4 +
Решение:
а) BiCl3 + SnCl2 + KOH → Bi +
Ионно-молекулярная форма процесса:
2Bi 3+ + 3Sn 2+ + 12OH — = 3Sn(OH)4 + 2Bi 0
Молекулярная форма будет иметь вид:
2BiCl3 + 3SnCl2 +12KOH = Bi + 3Sn(OH)4 + 12KCl.
2Bi 3+ + 3Sn 2+ + 12OH — + 12Cl — + 12K + = 3Sn(OH)4 + 2Bi 0 + 12K + + 12Cl — .
Сокращенная ионно-молекулярная форма процесса:
2Bi 3+ + 3Sn 2+ + 12OH — = 3Sn(OH)4 + 2Bi 0 .
Ионно-молекулярная форма процесса:
3S 2- + 4ClO3 — + 12H2O + 24H + = 4Cl — + 3SO4 2- + 12H2O + 24H +
После приведения членов в обеих частях равенства получим молекулярную форму:
4Na + + 4ClO3 — + 6H + + 3S 2- = 6H + + 3SO4 2- + 4Na + + 4Cl — .
Сокращённая ионно-молекулярная форма:
в) KCrO2 + Br2 + KOH →
Ионно-молекулярная форма процесса:
Молекулярная форма процесса:
5K + + CrO2 — + 2Br2 0 + 4OH — = 5K + + 4Br — + CrO4 — + 2H2O.
Сокращённая ионно-молекулярная форма:
Ионно-молекулярная форма процесса:
После приведения членов в обеих частях равенства получим:
Молекулярная форма процесса:
Для уравнивания атомов водорода и группы SO4 добавим в левую часть равенства одну молекулу H2SO4, получим:
Общая химия
Гидролиз солей
В общем случае гидролиз – это реакция обменного разложения вещества водой. Гидролизу подвержены соединения различных классов.
Гидролиз солей – процесс взаимодействия ионов, образовавшихся при диссоциации соли, с молекулами воды, сопровождающийся образованием слабых электролитов и изменением рН среды.
В реакции гидролиза вступают соли, образованные слабой кислотой и слабым основанием, или слабой кислотой и сильным основанием, или слабым основанием и сильной кислотой. Соли, образованные сильной кислотой и сильным основанием, гидролизу не подвергаются
Растворы солей, образованных слабой кислотой и сильным основанием, имеют щелочную реакцию. Например при растворении в воде цианида калия он полностью диссоциирует (все соли сильные электролиты):
Образующиеся в результате диссоциации ионы калия соответствуют сильному электролиту КОН, а цианид-ионы — слабой циановодородной кислоте HCN. Ионы водорода, образовавшиеся в результате диссоциации молекул воды, связываются цианид-ионами в молекулы HCN, в результате в растворе накапливаются ионы гидроксила:
Обычно эти два процесса при записи объединяют, получая сокращенное ионное уравнение гидролиза:
рН этого раствора больше 7. Такой гидролиз называется гидролизом по аниону. Для него можно записать полное ионное:
K + + CN — + H2O =K + + HCN + OH —
и молекулярное уравнение:
Растворы солей, образованных слабым основанием и сильной кислотой, имеют кислую реакцию. Аналогично предыдущему примеру гидролиз хлорида аммония NH4Cl:
Диссоциация при растворении соли:
Слабому основанию — аммиаку — соответствует ион аммония NH4 + , он и будет взаимодействовать с молекулами воды образуя слабый электролит:
В растворе накапливаются ионы водорода, среда кислая, рН раствора меньше 7. Такой гидролиз называется гидролизом по катиону. Полное ионное уравнение:
Особенно глубоко протекает гидролиз солей, образованных слабой кислотой и слабым основанием. В этом случае происходит гидролиз по катиону и аниону. Пример — гидролиз сульфида аммония. Соль при растворении в воде диссоциирует:
Оба иона, образовавшиеся при диссоциации, соответствуют слабым элетролитам, поэтому протекает гидролиз по катиону:
Ионы водорода и гидроксила дают молекулы воды — среда не может быть одновременно кислотй и щелочной:
однако среда не будет нейтральной. Реакция среды будет определяться соотношением констант диссоциации кислоты и основания. Если больше константа диссоциации основания (основание сильнее кислоты), среда будет щелочной, если больше константа диссоциации кислоты (кислота сильнее основаниия) — кислой. В приведенном примере аммиак — более сильный электролит по сравнению с сероводородной кислотой, поэтому среда будет слабощелочной, рН > 7.
В редких случаях, когда константы диссоциации кислоты и основания практически одинаковы, например, при гидролизе ацетата аммония CH3COONH4, среда будет почти нейтральная.
Если соль образована многокислотным основанием или многоосновной кислотой, гидролиз протекает ступенчато. Пример — гидролиз хлорида железа(III). Диссоциация соли при растворении:
Ион Fe 3+ соответствует слабому трехкислотному основанию Fe(OH)3, он и подвергается ступенчатому гидролизу. I-я ступень:
Гидролиз по первой ступени всегда протекает в значительно большей степени, чем по второй. Кроме того, ионы, образующиеся при гидролизе по первой ступени (в рассмотренном примере — ионы H + ), способствуют смещению равновесия второйступени влево, т. е. также подавляют гидролиз по второй ступени. Поэтому в обычных условиях (комнатная температура, атмосферное давление) гидролизом по второй и последующим ступеням можно пренебречь.
Следующий пример — гидролиз карбоната натрия Na3CO3. Диссоциация:
Ион соответствует слабой двухосновной угольной кислоте, именно он и подвергается гидролизу. I-я ступень:
И опять в обычных условиях существенна только первая ступень гидролиза.
http://buzani.ru/zadachi/khimiya-glinka/1221-ionno-molekulyarnaya-forma-protsessa-okisleniya-vosstanovleniya-zadacha-640
http://www.chem03.ru/index.php/data/index.php?id=33