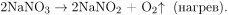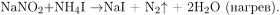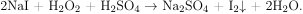Нитрат натрия: способы получения и химические свойства
Нитрат натрия NaNO3 — соль щелочного металла натрия и азотной кислоты. Белое вещество, весьма гигроскопичное, которое плавится без разложения, при дальнейшем нагревании разлагается.
Относительная молекулярная масса Mr = 84,99; относительная плотность для тв. и ж. состояния d = 2,266; tпл = 306,5º C;
Способ получения
1. Нитрат натрия можно получить путем взаимодействия гидроксида натрия и разбавленной азотной кислоты, образуется нитрат натрия и вода:
2. В результате взаимодействия горячего гидроксида натрия, оксида азота (IV) и кислорода образуется нитрат натрия и вода:
3. В результате реакции между горячим гидроксидом натрия, оксидом натрия (IV) и кислородом, происходит образование нитрата натрия и воды:
4. При комнатной температуре, в результате взаимодействия оксида азота (IV) и натрия образуется нитрат натрия и газ оксид азота (II):
2NO2 + Na = NO↑ + NaNO3
5. При смешивании горячего пероксида водорода и нитрита азота происходит образование нитрата натрия и воды:
Качественная реакция
Качественная реакция на нитрат натрия — взаимодействие с медью при нагревании в присутствии концентрированной кислоты:
1. При взаимодействии с серной кислотой и медью, нитрат натрия образует сульфат натрия, нитрат меди, газ оксид азота и воду:
Химические свойства
1. Hитрат натрия разлагается при температуре 380–500º С с образованием нитрита натрия и кислорода:
2. Н итрат натрия может реагировать с простыми веществами :
2.1. Н итрат натрия реагирует со свинцом при температуре выше 350 ºС . При этом образуется нитрит натрия и оксид свинца:
NaNO3 + Pb = NaNO2 + PbO
2.2. Нитрат натрия реагирует при комнатной температуре с цинком и разбавленной хлороводородной кислотой с образованием нитрита натрия и воды:
Нитрат натрия прокалили уравнение реакции
Нитрат натрия прокалили. Твердый продукт реакции нагрели с иодидом аммония, выделился газ, входящий в состав воздуха. Соль обработали раствором пероксида водорода, подкисленным серной кислотой. Образовавшееся простое вещество прореагировало при нагревании с раствором гидроксида натрия.
Напишите уравнения четырёх описанных реакций.
1) При разложении нитратов щелочных металлов образуется нитрит щелочного металла и выделяется кислород:
2) При нагревании нитритов с аммонийными солями образуется неустойчивый нитрит аммония, который разлагается до азота и воды:
3) При взаимодействии иодидов с пероксидом водорода в сернокислой среде выделяется молекулярный йод:
4) При взаимодействии йода с горячим раствором щелочи протекает реакция диспропорционирования, в результате которой молекулярный йод окисляется до и восстанавливается до
:
Vuz-24.ru
Материалы в помощь студентам и научным работникам
Задание с ответами: химия. ЕГЭ — 2018
Нитрат натрия прокалили. Твердый продукт реакции нагрели с иодидом аммония, выделился газ, входящий в состав воздуха. Соль обработали раствором пероксида водорода, подкисленным серной кислотой. Образовавшееся простое вещество прореагировало при нагревании с раствором гидроксида натрия.
Напишите уравнения четырёх описанных реакций.
Сведения для решения
1) При разложении нитратов щелочных металлов образуется нитрит щелочного металла и выделяется кислород:
2) При нагревании нитритов с аммонийными солями образуется неустойчивый нитрит аммония, который разлагается до азота и воды:
3) При взаимодействии иодидов с пероксидом водорода в сернокислой среде выделяется молекулярный йод:
4) При взаимодействии йода с горячим раствором щелочи протекает реакция диспропорционирования, в результате которой молекулярный йод окисляется до 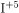
http://chem-ege.sdamgia.ru/problem?id=6989
http://vuz-24.ru/task/task-2981.php