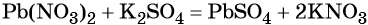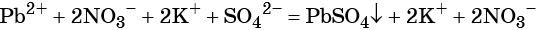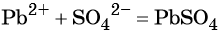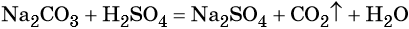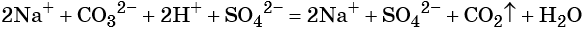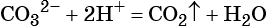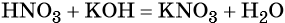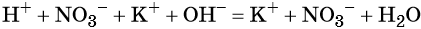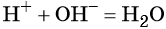Напишите уравнение реакций в молекулярной, полной и сокращенной ионной формах : а) гидроксид кальция + фосфорная кислота ; б) карбонат натрия + серная кислота ; в) нитрат свинца + фторид натрия ; г) х?
Химия | 10 — 11 классы
Напишите уравнение реакций в молекулярной, полной и сокращенной ионной формах : а) гидроксид кальция + фосфорная кислота ; б) карбонат натрия + серная кислота ; в) нитрат свинца + фторид натрия ; г) хлорид меди( II ) + гидроксид калия.
Укажите тип и признак химической реакции.
На счет в не уверен На, так PbF2 малорастворим.

Карбонат калия и соляная кислота Хлорид железа (3) и гидроксида калия Гидроксид натрия и серная кислота Напишите уравнения в молекулярном и ионном виде?
Карбонат калия и соляная кислота Хлорид железа (3) и гидроксида калия Гидроксид натрия и серная кислота Напишите уравнения в молекулярном и ионном виде.
Карбонат натрия, хлорид железа 2, гидроксид калия, серная кислота, сульфит натрия составить уравнения : полное ионное, ионно — сокращенное?
Карбонат натрия, хлорид железа 2, гидроксид калия, серная кислота, сульфит натрия составить уравнения : полное ионное, ионно — сокращенное.
Закончить уравнения реакций ионного обмена в молекулярном виде, составить полное и сокращенное ионные уравнения : Фосфорная кислота + гидроксид натрия = Нитрат железа (III) + гидроксид натрия =?
Закончить уравнения реакций ионного обмена в молекулярном виде, составить полное и сокращенное ионные уравнения : Фосфорная кислота + гидроксид натрия = Нитрат железа (III) + гидроксид натрия =.
Составить уравнение реакций в молекулярной и ионных формах между веществами : Карбонат натрия и серной кислота азотной кислота и гидроксид калия сульфат цинка и гидроксид лития?
Составить уравнение реакций в молекулярной и ионных формах между веществами : Карбонат натрия и серной кислота азотной кислота и гидроксид калия сульфат цинка и гидроксид лития.
Составьте молекулярные и ионные уравнения реакций между веществами : — сульфидом калия и соляной кислотой, — гидроксидом меди 2 и азотной кислотой — нитратом свинца 2 и сульфатом кальция — карбанатом ?
Составьте молекулярные и ионные уравнения реакций между веществами : — сульфидом калия и соляной кислотой, — гидроксидом меди 2 и азотной кислотой — нитратом свинца 2 и сульфатом кальция — карбанатом магния и соляной кислотой — хлоридом железа 3 и нитратом серебра — гидроксидом бария и серной кислотой — гидроксидом натрия и нитратом аммония.
Гидроксид натрия образуется при взаимодействии : а)карбоната натрия и гидроксида калия б)карбоната натрия и гидроксида кальция в)оксида натрия и воды г)нитрата натрия и гидроксида кальция Написать ура?
Гидроксид натрия образуется при взаимодействии : а)карбоната натрия и гидроксида калия б)карбоната натрия и гидроксида кальция в)оксида натрия и воды г)нитрата натрия и гидроксида кальция Написать уравнения возможных реакций в молекулярном , полном и сокращенно ионно — молекулярном виде.
Запишите уравнение возможных реакций в молекулярном а также полном и сокращенном ионном виде а) фторид натрия и нитрат серебра б) нитрат магния и фосфат калия в) карбонат натрия и серная кислота?
Запишите уравнение возможных реакций в молекулярном а также полном и сокращенном ионном виде а) фторид натрия и нитрат серебра б) нитрат магния и фосфат калия в) карбонат натрия и серная кислота.
Напишите молекулярное, полное и сокращенное ионные уравнения реакций между растворами следующий веществ :Хлорид алюминия + гидроксид калияХлорид цинка + гидроксид натрияНитрат серебра + хлорид кальция?
Напишите молекулярное, полное и сокращенное ионные уравнения реакций между растворами следующий веществ :
Хлорид алюминия + гидроксид калия
Хлорид цинка + гидроксид натрия
Нитрат серебра + хлорид кальция.
Напишите молекулярные, полные и сокращенные ионные уравнения реакций между веществами :А)гидроксидом калия и серной кислотойБ)нитратом серебра и хлоридом кальцияВ)карбонатом натрия и азотной кислотой?
Напишите молекулярные, полные и сокращенные ионные уравнения реакций между веществами :
А)гидроксидом калия и серной кислотой
Б)нитратом серебра и хлоридом кальция
В)карбонатом натрия и азотной кислотой.
Напишите в молекулярной и ионно — молекулярной форме уравне — ния реакций между : серной кислотой и нитратом натрия ; хлоридом строн — ция и карбонатом калия ; гидроксидом железа (III) и сероводородом?
Напишите в молекулярной и ионно — молекулярной форме уравне — ния реакций между : серной кислотой и нитратом натрия ; хлоридом строн — ция и карбонатом калия ; гидроксидом железа (III) и сероводородом.
Вы зашли на страницу вопроса Напишите уравнение реакций в молекулярной, полной и сокращенной ионной формах : а) гидроксид кальция + фосфорная кислота ; б) карбонат натрия + серная кислота ; в) нитрат свинца + фторид натрия ; г) х?, который относится к категории Химия. По уровню сложности вопрос соответствует учебной программе для учащихся 10 — 11 классов. В этой же категории вы найдете ответ и на другие, похожие вопросы по теме, найти который можно с помощью автоматической системы «умный поиск». Интересную информацию можно найти в комментариях-ответах пользователей, с которыми есть обратная связь для обсуждения темы. Если предложенные варианты ответов не удовлетворяют, создайте свой вариант запроса в верхней строке.
1)аг (точно оба подходят) 2)а 3)ав 4)вг 5)а 6)а 7)а 8)г 9)г 10) не понятно в сколько молярном(число).
Под кетоновыми телами подразумевают группу продуктов метаболизма, образующихся в результате обмена основных нутриентов : углеводов, жиров и белков. Последние трансформируются с образованием вещества под названием ацетил — КоА (через гликолиз, бета -..
Напишите молекулярные и ионные уравнения реакций взаимодействия а) фторида натрия и нитрата свинца
| 🎓 Заказ №: 22185 |
| ⟾ Тип работы: Задача |
| 📕 Предмет: Химия |
| ✅ Статус: Выполнен (Проверен преподавателем) |
| 🔥 Цена: 153 руб. |
👉 Как получить работу? Ответ: Напишите мне в whatsapp и я вышлю вам форму оплаты, после оплаты вышлю решение.
➕ Как снизить цену? Ответ: Соберите как можно больше задач, чем больше тем дешевле, например от 10 задач цена снижается до 50 руб.
➕ Вы можете помочь с разными работами? Ответ: Да! Если вы не нашли готовую работу, я смогу вам помочь в срок 1-3 дня, присылайте работы в whatsapp и я их изучу и помогу вам.
⚡ Условие + 37% решения:
Напишите молекулярные и ионные уравнения реакций взаимодействия а) фторида натрия и нитрата свинца; б) гидроксида марганца (II) и серной кислоты.
Решение: а) Молекулярное уравнение Ионное уравнение
Научись сам решать задачи изучив химию на этой странице:
|
Услуги:
|
Готовые задачи по химии которые сегодня купили:




















































Образовательный сайт для студентов и школьников
Копирование материалов сайта возможно только с указанием активной ссылки «www.lfirmal.com» в качестве источника.
© Фирмаль Людмила Анатольевна — официальный сайт преподавателя математического факультета Дальневосточного государственного физико-технического института
Реакции ионного обмена и условия их осуществления
Реакциями ионного обмена называют химические реакции, которые протекают между ионами без изменения степеней окисления элементов и приводят к обмену составных частей реагентов.
Уравнения обменных реакций записывают в молекулярной форме (с указанием формул всех реагирующих веществ со стехиометрическими коэффициентами); в полной ионной форме (с указанием всех существующих в растворе ионов) и в сокращённой ионной форме (с указанием только тех ионов, которые непосредственно взаимодействуют между собой). При написании уравнений реакций в ионной форме формулы малодиссоциирующих веществ (слабых электролитов) записывают в молекулярной форме.
Уравнения реакций обмена в водных растворах электролитов составляют так.
- Записывают в левой части уравнения все формулы веществ, вступивших в реакцию, в молекулярной или ионной форме.
- Руководствуясь знаниями физико-химических свойств реагентов и таблицами растворимости веществ, составляют формулы продуктов реакции.
- Проверяют число атомов каждого элемента в обеих частях уравнения и определяют необходимые стехиометрические коэффициенты перед формулами.
Реакции ионного обмена в растворах электролитов протекают практически необратимо и до конца, если в качестве продуктов образуются осадки (малорастворимые вещества), газы (легколетучие вещества), слабые электролиты (малодиссоциированные соединения) и комплексные ионы.
Если при взаимодействии растворов электролитов не образуется ни одно из указанных видов соединений, химическое взаимодействие практически не происходит.
Уравнения обменных реакций можно записать в молекулярной форме, полной ионной форме, с указанием всех существующих в растворе ионов и в сокращённой ионной форме, которая, собственно, и выражает взаимодействие ионов. Следует отметить, что при написании уравнений реакций в ионной форме малодиссоциирующие вещества (слабые электролиты) записывают в молекулярной форме.
Пример 1. Реакция между нитратом свинца и сульфатом калия. В результате этой реакции образуется нерастворимый сульфат свинца и выделяется растворимый нитрат калия:
(полная ионно-молекулярная форма),
(сокращённая ионно-молекулярная форма).
Пример 2. Взаимодействие карбоната натрия с серной кислотой. При этом выделяется углекислый газ и вода, а в растворе остаются катионы натрия и сульфат-ионы:
(полная ионно-молекулярная форма),
(сокращённая ионно-молекулярная форма).
Пример 3. Реакция между азотной кислотой и едким калием. В результате данной реакции образуется малодиссоциированное соединение — вода и в растворе остаются катионы калия и нитрат-ионы:
(полная ионно-молекулярная форма),
(сокращённая ионно-молекулярная форма).
Тренировочные задания
1. Осадок образуется при взаимодействии водных растворов
2. Газ выделяется при взаимодействии водных растворов
3. Краткое ионное уравнение H + + OH – = H2O описывает взаимодействие
1) гидроксида кальция и фосфорной кислоты
2) гидроксида лития и фосфорной кислоты
3) гидроксида натрия и бромоводородной кислоты
4) гидроксида алюминия и бромоводородной кислоты
4. Краткое ионное уравнение 3Ba 2+ + 2PO4 3– = Ba3(PO4)2↓ описывает взаимодействие
1) карбоната бария и фосфорной кислоты
2) карбоната бария и фосфата натрия
3) хлорида бария и фосфорной кислоты
4) хлорида бария и фосфата натрия
5. Краткое ионное уравнение Ba 2+ + SO4 2– = BaSO4↓ описывает взаимодействие
1) хлорида бария и сульфата натрия
2) хлорида бария и сернистой кислоты
3) гидроксида бария и сульфата натрия
4) гидроксида бария и серной кислоты
6. Краткое ионное уравнение Ag + + Cl – = AgCl↓ описывает взаимодействие
1) хлорида кальция и бромида серебра
2) фосфата серебра и соляной кислоты
3) карбоната серебра и хлорида натрия
4) нитрата серебра и хлорида калия
7. Краткое ионное уравнение H + + OH – = H2O отвечает взаимодействию
1) азотной кислоты и гидроксида железа (III)
2) бромоводородной кислоты и гидроксида натрия
3) азотной кислоты и гидроксида меди
4) сернистой кислоты и гидроксида кальция
8. Краткое ионное уравнение 2Н + + S 2– = Н2S↑ отвечает взаимодействию
1) соляной кислоты и сульфида железа (II)
2) сернистой кислоты и сульфида калия
3) азотной кислоты и сульфида меди
4) азотной кислоты и сульфида натрия
9. Краткое ионное уравнение 2Н + + CO3 2– = CO2↑ + H2O отвечает взаимодействию
1) соляной кислоты и карбоната кальция
2) сернистой кислоты и карбоната бария
3) азотной кислоты и карбоната калия
4) серной кислоты и карбоната бария
10. Краткое ионное уравнение 2Н + + CaCO3 = Ca 2+ + CO2↑ + H2O отвечает взаимодействию
1) соляной кислоты и карбоната кальция
2) сернистой кислоты и карбоната кальция
3) фосфорной кислоты и карбоната кальция
4) серной кислоты и карбоната кальция
11. Краткое ионное уравнение Al 3+ + 3OH – = Al(OH)3↓ отвечает взаимодействию
1) сульфата алюминия и гидроксида кальция
2) сульфата алюминия и гидроксида бария
3) сульфата алюминия и гидроксида меди
4) сульфата алюминия и гидроксида натрия
12. Краткое и полное ионное уравнения совпадают для реакции
1) соляной кислоты и карбоната калия
2) уксусной кислоты и карбоната бария
3) уксусной кислоты и гидроксида калия
4) серной кислоты и гидроксида калия
13. Одновременно в растворе не могут существовать ионы
1) Ba 2+ , Fe 2+ , PO4 3– , CO3 2–
2) Ba 2+ , NO3 – , Cl – , K +
3) CH3COO – , Li + , Br – , Al3 +
4) Mg 2+ , Br – , K + , Cl –
14. Одновременно в растворе могут существовать ионы
1) Ba 2+ , Fe 2+ , PO4 3– , SO4 2–
2) Ba 2+ , SO4 2– , Ca 2+ , PO4 3–
3) Na + , Ba 2+ , NO3 – , Cl –
4) Mg 2+ , Ca 2+ , SO3 2– , CO3 2–
15. Образование осадка происходит при взаимодействии водных растворов
16. Образование газа происходит при взаимодействии водных растворов
1) сульфата калия и хлорида бария
2) гидроксида алюминия и серной кислоты
3) хлорида кальция и карбоната натрия
4) соляной кислоты и карбоната натрия
17. С выпадением осадка протекает реакция ионного обмена между растворами
1) нитрата натрия и фторида калия
2) хлорида алюминия и избытка гидроксида калия
3) нитрата серебра и фторида натрия
4) нитрата магния и гидроксида калия
18. С выделением газа протекает реакция ионного обмена между растворами
1) карбоната калия и бромоводородной кислоты
2) сульфата натрия и гидроксидом калия
3) нитрата серебра и бромида цинка
4) нитрата алюминия и гидроксида бария
19. С выделением газа протекает реакция ионного обмена между растворами
1) гидроксида бария и азотной кислоты
2) сульфата алюминия и нитрата бария
3) нитрата серебра и йодида лития
4) азотной кислотой и карбоната аммония
20. С выделением воды протекает реакция ионного обмена между растворами
1) нитрата меди и хлорида железа
2) гидрокарбоната натрия и гидроксида натрия
3) нитрата ртути и бромида лития
4) нитрата аммония и нитрита натрия
http://lfirmal.com/%D0%9D%D0%B0%D0%BF%D0%B8%D1%88%D0%B8%D1%82%D0%B5-%D0%BC%D0%BE%D0%BB%D0%B5%D0%BA%D1%83%D0%BB%D1%8F%D1%80%D0%BD%D1%8B%D0%B5-%D0%B8-%D0%B8%D0%BE%D0%BD%D0%BD%D1%8B%D0%B5-%D1%83%D1%80%D0%B0%D0%B2%D0%BD-6/
http://himi4ka.ru/ogje-2018-po-himii/urok-11-reakcii-ionnogo-obmena-i-uslovija-ih-osushhestvlenija.html