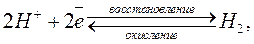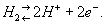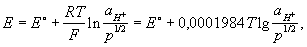Вопрос29. Водородный электрод. Устройство и электродные процессы. Стандартный водородный электрод. Зависимость величины потенциала водородного электрода от рН среды
Измеряют относительную величину электродного потенциала, сравнивая его с потенциалом электрода, выбранного в качестве эталона.
В качестве такого электрода, называемого электродом сравнения, часто используют стандартный водородный электрод.
Водородный электрод состоит из платиновой пластинки, покрытой платиновой чернью (электролитически осажденной платиной), которая абсорбирует продуваемый через электрод газообразный водород. Пластина погружена в раствор кислоты.
На электроде устанавливается равновесие:
Водородный электрод, находящийся при стандартных условиях ([Н + ] = 1 моль/л, Р 0 = 101,3 кПа), называют стандартным водородным электродом, а потенциал такого электрода условно принят за ноль при любой температуре. Условная запись водородного электрода:
рН влияет на величину равновесного потенциала.
Это означает, что при изменении рН на единицу потенциал водородного электрода уменьшается на 59 мВ.
Чем кислее раствор, тем большую величину имеет потенциал водородного электрода.
Вопрос30. Гальванические элементы. Как можно практически определить электродный потенциал металла? От каких факторов зависит величина электродных потенциалов? Уравнение Нернста. Уравнение Нернста для металлических электродов при стандартных условиях.
Устройства, в которых энергия химической окислительно-восстановительной реакции превращается в электрическую энергию, называются источниками электрической энергии, или гальваническими элементами. Всякий гальван. элемент сост. из двух электродов – металлов, погруженных в растворы электролитов; последние сообщаются друг с другом – обычно через пористую перегородку. Переход Ме из кристалла в раствор электролита в виде гидратированных ионов с оставлением эквивалентного количества е в кристалле, называется анодным процессом — процесс окисления. Обратным анодному является катодный процесс – объединение каких-либо частиц среды с электронами металла, с восстановлением частиц на поверхности металла. Электродвижущая сила Е(э.д.с.)-максимальное напряжение гальванического элемента, отвечающего обратимому протеканию происходящей в нем реакции. В результате изучения потенциалов различных электродных процессов установлено, что их величины зависят от следующих факторов: 1) от природы веществ –участников электродного процесса. 2) от соотношения м/у концентрациями этих веществ 3) от температуры системы. Эта зависимость выражается уравнением Нернста (В. Нернст, 1889г.): E=E 0 +RT*ln(aокисл формы/aвосстан формы)/n*F, где E 0 – стандартный электродный потенциал, n – число е, принимающих участие в о.-в. реакциях , F – число фарадея (96500), а – активность (эффективная или условная концентрация, в соответствии с которой ион действует при хим активности) а=f*C(Для разбавленных растворов a=C, f->1).Формула Нернста для Ме электрода при T=298K: EМе=E0+0.059*lnaМе+n/n
Вопрос31. Типы гальванических элементов. Химические, концентрационные и термогальванические элементы. Э.Д.С. гальванических элементов. Приведите примеры. Укажите процессы, протекающие на электродах, и рассчитайте ЭДС какого-либо химического гальванического элемента.
Устройства, в которых энергия химической окислительно-восстановительной реакции превращается в электрическую энергию, называются источниками электрической энергии, или гальваническими элементами. Всякий гальван. элемент сост. из двух электродов – металлов, погруженных в растворы электролитов; последние сообщаются друг с другом – обычно через пористую перегородку. Переход Ме из кристалла в раствор электролита в виде гидратированных ионов с оставлением эквивалентного количества е в кристалле, называется анодным процессом — процесс окисления. Обратным анодному является катодный процесс – объединение каких-либо частиц среды с электронами металла, с восстановлением частиц на поверхности металла. Типы гальванических элементов: Химические – состоят из разных электродов, концентрационные – составлены из одинаковых электродов с разными концентр электролитов, термогальванические – одинаковые электроды, но при разных температурах. Медноцинковый элемент –Zn\ZnSO4\\CuSO4\Cu. ЭДС – Eк – Eа=1,1В. Процессы на аноде – окисление (Zn 0 – 2е = Zn +2 ), на катоде – восстановление (Cu +2 + 2е = Сu 0 ).
Водородный электрод
Водор о дный электр о д, платиновая пластинка, электролитически покрытая платиновой чернью, погружённая в раствор кислоты с определённой концентрацией ионов водорода Н + и омываемая током газообразного водорода. Потенциал водородного электрода возникает за счёт обратимо протекающей реакции
Между водородом, адсорбированным платиновой чернью, и ионами водорода в растворе устанавливается равновесие. Потенциал электрода Е определяется уравнением Нернста:
где Т — абсолютная температура (К), аН + — активная концентрация ионов водорода (г-ион/л), р — давление водорода [кгс/см 2 (атм)], Е° — нормальный (или стандартный) потенциал водородного электрода при р = 1 кгс/см 2 (1 атм) и aH + = 1. При любой заданной температуре Е° условно принято считать равным нулю. От потенциала стандартного водородного электрода отсчитывают потенциалы всех других электродов (так называемая водородная шкала потенциалов). При работе с водородным электродом необходима тщательная очистка водорода от примесей. Особенно опасны соединения серы и мышьяка, а также кислород, реагирующий с водородом на поверхности платины с образованием воды, что приводит к нарушению равновесия
Назначение и устройство водородного электрода
Стандартный водородный электрод – это элемент сравнения, применяющийся для определения потенциалов в гальванических элементах и при различных электрохимических реакциях.
Так как измерить потенциал отдельного электрода невозможно, используется сравнительный элемент, в частности в составе электролитических ячеек.
Стандартный водородный электрод: что это?
Электроды сравнения – электрохимические системы, использующиеся для измерения электродных потенциалов.
Любой электрод, находящийся в состоянии термодинамического равновесия, способный обеспечить постоянство во времени и воспроизводимость всех характеристик, может служить элементом сравнения.

Наиболее распространенными являются водородный, каломельный, галогеносеребряный и оксидно-ртутный вариант устройства.
Стандартный элемент сравнения представляет собой проволоку или пластинку, выполненную из металла, который хорошо адсорбирует гидроген.
Обычно используются такие металлы, как платина или палладий, на которые электролитическим методом нанесена платина в тонкодисперсном состоянии. Это увеличивает активную площадь поверхности для взаимодействия с гидрогеном.
Пластина погружается в водный раствор, насыщенный ионами гидрогена. Через раствор, под атмосферным давлением, пропускается химически чистый водород.
В результате поверхность платиновой пластины гидрогенизируется и на границе поверхности платиновой пластины с раствором устанавливается равновесие между переходом гидрогена из молекулярного состояния в атомарное и наоборот.
Как он работает?
Принцип работы устройства основан на растворимости металлов в электролите. Даже при погружении металла в воду он начинает подвергаться действию ее молекул.
С поверхности пластины начинают отрываться ионы, и они попадают в слой воды, контактирующий с металлом. В результате нейтральный атом превращается в ион.
Это приводит к высвобождению отрицательно заряженных частиц – электронов. Между положительными атомами и электронами появляется потенциал. Его действие обуславливает концентрацию ионов у поверхности металла, образуя адсорбционный слой.
Такая структура носит название – двойной электрический слой.

В электрохимии потенциалы металлов измеряются в вольтах, по отношению к некоторому стандартному элементу. Согласно международной договоренности, в качестве такого элемента принято считать стандартный ВЭ.
При давлении газообразного водорода на границе с раствором в 1 атмосферу, концентрации положительных ионов водорода 1 моль/л и температуре 298 К, потенциал принимается равным 0 и его называют нормальным водородным электродом.
В настоящее время не существует методики, позволяющей независимо определить потенциал отдельно взятого электрода. Для этих целей применяется данное устройство.
В частности, собирается гальваническая цепь, состоящая из измеряемого и ВЭ. Так как потенциал второго принят за 0, то относительный потенциал второго будет равен электродвижущей силе гальванического элемента.
При работе данного устройства важно использовать гидроген, хорошо очищенный от примесей серы и мышьяка. Также нежелательной примесью является кислород, который может реагировать с гидрогеном на поверхности платиновой пластины с образованием воды, что приведет к нестабильной работе.
Схема стандартного водородного электрода
Данное устройство используют для измерения потенциалов электрохимических реакций.

Схема водородного электрода представляет собой:
- пластину, изготовленную из палладия или платины;
- подвод газообразного водорода;
- водный раствор, как правило, соляной или серной кислоты с концентрацией водорода 1 моль/л;
- водяной затвор;
- электролитический мост для соединения со второй половиной гальванической цепи.
Устройство элемента сравнения очень простое. Кроме того, его можно применять в широком интервале температур и давлений, а также в не водных и частично водных растворах.
Эксплуатация устройства сопряжена с определенными трудностями, например, с необходимостью постоянной подачи химически чистого водорода. Несмотря на это, стандартные элементы сравнения широко использовались в работах многих известных ученых.
Так, С.П.Л. Серенсен, с использованием данного устройства, разработал современную теорию pH-метрии, а Макклендон впервые использовал электрод сравнения для внутрижелудочной pH-метрии.
Стандартный сравнительный элемент широко используется для определения потенциалов электродов. Для этого собирается гальванический элемент, состоящий из измеряемого и стандартного водородного электрода.
Также его применяют для определения растворимости, pH-метрии, скорости протекания электрохимических реакций и для измерения концентрации ионов водорода. Простота схемы ВЭ делает его наиболее удобным для использования.
http://xumuk.ru/bse/521.html
http://tutsvarka.ru/oborudovanie/vodorodnyj-elektrod