Напишите уравнение реакции окисления оксида азота(II) до оксида азота(IV). Протекает ли эта реакция при обычных условиях? Какую
Ваш ответ
решение вопроса
Похожие вопросы
- Все категории
- экономические 43,300
- гуманитарные 33,630
- юридические 17,900
- школьный раздел 607,261
- разное 16,836
Популярное на сайте:
Как быстро выучить стихотворение наизусть? Запоминание стихов является стандартным заданием во многих школах.
Как научится читать по диагонали? Скорость чтения зависит от скорости восприятия каждого отдельного слова в тексте.
Как быстро и эффективно исправить почерк? Люди часто предполагают, что каллиграфия и почерк являются синонимами, но это не так.
Как научится говорить грамотно и правильно? Общение на хорошем, уверенном и естественном русском языке является достижимой целью.
Окисление оксида азота II (NO).
Лекция 8.
Оксид азота II (NO) имеет низкую растворимость в воде. Коэффициент поглощения 
| Т, °С | ||||||
 | 0,07381 | 0,05709 | 0,04706 | 0,03507 | 0,02954 | 0,0270 |
Вследствие чего NO не может быть использован для производства азотной кислоты, поэтому его подвергают дальнейшему окислению.
При окислении NO образуются высшие оксиды. Образование высших оксид протекает по реакциям:



Оксиды азота имеют различную термодинамическую устойчивость, которая в свою очередь зависит от температуры.
| Температура, К | Термодинамические устойчивости различных оксидов, расположенные в порядке уменьшения |
| N2O4>N2O>N2O5>NO2>N2O3>NO | |
| NO>N2O>NO2>N2O3>N2O4>N2O5 |
Таким образом, при низких температурах наибольшей термодинамической устойчивость обладает N2O4, а при высоких – NO. Так как оксид азота II (NO) имеет низкую растворимость в воде, то его целесообразно окислять при низких температурах, когда его термодинамическая устойчивость наименьшая по сравнению с другими оксидами.
С понижением температуры равновесие реакций (1)-(3) смещается в сторону образования продуктов. При низких температурах и времени, достаточном для установления равновесия, а так же при избытке кислорода преобладающим продуктом окисления будет оксид N2O4. Об условиях превращений одних оксидов азота в другие и перехода их из газообразной фазы в жидкую и твердую можно судить по диаграмме состояния системы NO-NO2 при атмосферном давлении (рисунок 1).
 | Рис. 1. Диаграмма состояния системы NO-NO2 при атмосферном давлении. |
При недостатке кислорода или неустановившемся равновесии в нитрозных газах могут одновременно содержаться N2O4, NO2, N2O3, NO.
Оксид азота N2O5 при окислении N2O4 кислородом не образуется, даже если процесс происходит при повышенном давлении. Оксид азота N2O5 может быть получен только окислением N2O4 озоном, при этом протекает реакция:

Одновременно с образованием N2O5 может образовываться N2O6.
От степени полноты протекания реакции (1) будет зависеть остаточное содержание NO в газовой смеси. Поэтому при окислении оксида азота NO данная реакция является определяющей. Зависимость константы равновесия реакции:
выраженная через парциальные давления веществ имеет следующий вид:

Существует эмпирическое уравнение, описывающее зависимость константы равновесия от температуры (уравнение Боденштейна):

На рисунке 2 представлен график зависимости равновесной степени окисления оксида азота NO ( 
 | Рис. 2. Зависимость равновесной степени окисления оксида азота NO (  ) от температуры и давления при начальной концентрации 9,92% NO и 5,68 О2. Значения Р, МПа: 1 – 0,1; 2 – 0,8. ) от температуры и давления при начальной концентрации 9,92% NO и 5,68 О2. Значения Р, МПа: 1 – 0,1; 2 – 0,8. |
Из диаграммы (рис. 2) следует, что понижение температуры и повышение давления газа смещают равновесие реакции в сторону образования продуктов. При температуре менее 200°С реакция окисления NO при давлении 0,1 МПа протекает почти на 100%. Поэтому при данных условиях реакцию можно рассматривать как протекающую необратимо в сторону образования NO2.
Окисление оксида азота NO протекает по уравнению реакции третьего порядка. Дифференциальное уравнение скорости окисления NO кислородом имеет вид:
где 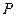

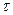
Значения констант скорости реакции, по данным М. Боденштейна, представлены в таблице 1.
Константы скорости окисления NO кислородом при различных температурах и давлении 1 МПа
Для определения времени, необходимого для окисления NO до заданной степени, можно использовать уравнение:
где 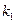
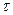



Степень окисления NO в долях единицы можно при помощи уравнения: 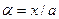
На рисунке 3 представлена номограмма для определения скорости окисления NO.
Рис. 3. Номограмма для определения скорости окисления NO.
На номограмме: 



Реакция окисления NO является суммой двух бимолекулярных реакций:
Первая реакция протекает быстро, вторая – медленно. С повышением температуры равновесие первой реакции смещается в сторону исходных веществ, концентрация NO3 уменьшается, поэтому реакция образования NO2 замедляется. С понижением температуры концентрация NO3 увеличивается, что приводит к ускорению второй реакции, которая и определяет общую скорость процесса.
Реакция окисления NO кислородом относится к тем немногочисленным процессам, скорость протекания которых с понижением температуры увеличивается.
Как видно из уравнения кинетики окисления NO, скорость реакции давлению во второй степени. То есть если увеличить общее давление в 2 раза, то скорость окисления увеличится в четыре раза.
В действительности практически невозможно достичь 100% окисления NO в NO2, так как для этого требуется высокое давление, высокие концентрации NO и кислорода в исходных реагентах (другими словами исходные газы должны содержать как можно меньше примесей в своем составе).
Переработка нитрозных газов зачастую производят при низких температурах. В этих условиях двуокись азота практически не существует, часть ее всегда полимеризуется в четырех окись азота:
Степень полимеризации тем выше, чем ниже температура и больше концентрация двуокиси азота NO2. Процесс диссоциации (распада молекулы N2O4 на NO2) имеет обратную зависимость.
Зависимость содержания диоксида азота (NO2) и четырех окиси азота (N2O4) от температуры можно проследить по следующим данным:
| Температура, °С | ||||||||||||||||||||||||||
| Содержание NO2, % об. | 31,0 | 88,0 |
| Оксиды азота | Цвет | Фаза | Характер оксида |
| N2O Оксид азота (I), закись азота, «веселящий газ» | бесцветный | газ | несолеобразующий |
| NO Оксид азота (II), закись азота, «веселящий газ» | бесцветный | газ | несолеобразующий |
| N2O3 Оксид азота (III), азотистый ангидрид | синий | жидкость | кислотный |
| NO2 Оксид азота (IV), диоксид азота, «лисий хвост» | бурый | газ | кислотный (соответствуют две кислоты) |
| N2O5 Оксид азота (V), азотный ангидрид | бесцветный | твердый | кислотный |
Оксид азота (II)
Оксид азота (II) NO – это несолеобразующий оксид. В нормальных условиях это бесцветный ядовитый газ, плохо растворимый в воде. На воздухе коричневеет из-за окисления до диоксида азота. Сжижается с трудом; в жидком и твёрдом виде имеет голубой цвет.
Способы получения
1. В лаборатории оксид азота (II) получают действием разбавленной азотной кислоты (30%) на неактивные металлы.
Например , при действии 30 %-ной азотной кислоты на медь образуется NO:
Также NO можно получить при окислении хлорида железа (II) или иодоводорода азотной кислотой:
FeCl2 + NaNO3 + 2HCl → FeCl3 + NaCl + NO + H2O
2HNO3 + 2HI → 2NO + I2 + 2H2O
2. В природе оксид азота (II) образуется из азота и кислорода под действием электрического разряда, например, во время грозы:
3. В промышленности оксид азота (II) получают каталитическим окислением аммиака :
Химические свойства
1. Оксид азота (II) легко окисляется под действием окислителей .
Например , горит в атмосфере кислорода:
Оксид азота (II) легко окисляется под действием хлора или озона:
2NO + Cl2 → 2NOCl
2. В присутствии более сильных восстановителей проявляет свойства окислителя . В атмосфере оксида азота (II) могут гореть водород, углерод и т.п.
Например , оксид азота (II) окисляет водород и сернистый газ:
3. Как несолеобразующий оксид, при обычных условиях с основаниями, основными оксидами, амфотерными оксидами, кислотными оксидами, кислотами и амфотерными гидроксидами оксид азота (II) не реагирует:
http://poisk-ru.ru/s39378t6.html
http://chemege.ru/oksid-azota-ii/








 .
. .
.

 .
.