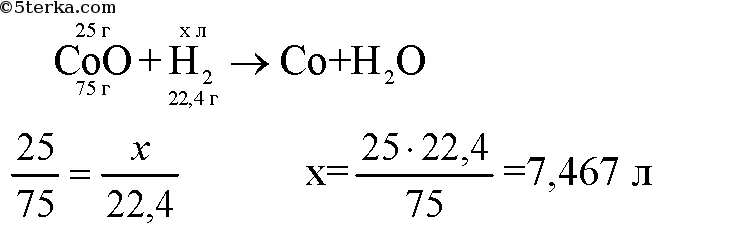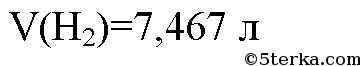Оксид магния: способы получения и химические свойства
Оксид магния MgO — бинарное неорганическое вещество . Белый, тугоплавкий, термически устойчивый, не реагирует с водой. Проявляет основные свойства.
Относительная молекулярная масса Mr = 40,3; относительная плотность для тв. и ж. состояния d = 3,62; tпл ≈ 2825º C; tкип = 3600º C.
Способ получения
1. Оксид магния получается при разложении карбоната магния при температуре 350 — 650º C. В результате разложения образуется оксид магния и углекислый газ:
2. В результате разложения нитрата магния при температуре выше 300º С образуется оксид магния, оксид азота (IV) и кислород:
3. Гидроксид магния разлагается при 350-480º С с образованием оксида магния и воды:
4. Оксид магния можно получить путем разложения сульфата магния при температуре выше 1200º C, образуется оксид магния, кислород и оксид серы (IV):
5. Оксид магния можно получить сжиганием магния в в кислороде при 600 — 650º С:
2Mg + O2 = 2MgO
Химические свойства
1. Оксид магния реагирует с простыми веществами :
1.1. В результате реакции между оксидом магния и кальцием при температуре выше 400º С образуется магний и оксид кальция:
MgO + Ca = CaO + Mg
1.2. Оксид магния реагирует с углеродом при температуре выше 2000º С и образует магний и угарный газ:
MgO + C = Mg + CO
2. Оксид магния взаимодействует со сложными веществами:
2.1. Оксид магния взаимодействует с кислотами . При этом образуются соль и вода.
2.1.1. О ксид магния с разбавленной соляной кислотой образует хлорид магния и воду:
MgO + 2HCl = MgCl2 + H2O
2.3. Оксид магния взаимодействует с водой при 100 — 125º С, образуя гидроксид магния:
Тема III. Работа 1. Получение и свойства водорода. Вариант 2
Вопросы:
1. Напишите уравнения реакций: а) магния с серной кислотой; б) водорода с оксидом молибдена(VI) MoO3; в) водорода с серой (сера в образующемся соединении двухвалентна).
2. В каком виде элемент водород встречается на Земле?
3. Рассчитайте массу водорода, который вступит в реакцию с 25 г оксида кобальта(II) CoO.
Уравнение реакции: CoO + H2 = H2O + Co
Решения и ответы:
2. Смесь водорода с кислородом, что возможно при надувании воздушных шаров и аэростатов, взрывоопасна.

задача №2
к главе «Тема III. Водород. Кислоты. Соли. Работа 1. Получение и свойства водорода».
В какие реакции вступает оксид магния
Всё о химических свойствах оксида магния
Оксид магния — порошкообразное вещество, которое в природе встречается в форме минерала периклаз. Порошок этот очень тугоплавкий (расплав образуется при температуре свыше 2650 ⁰С).
Оксид магния легко впитывает влагу, благодаря чему он нашел широкое применение. Оксид магния применяется в пищевой промышленности (кодируется как пищевая добавка Е 530) против комкообразования и слеживания.
В медицине MgO используется как антацид (средство против повышенной кислотности в желудке), как слабительное или как вспомогательное вещество во многих лекарствах, которые выпускаются в форме таблеток.
Нашел MgO широкое распространение и как наполнитель в производстве резины, огнеупоров, цемента, а также в качестве мелкого абразива в электронной промышленности.
Интересное оптическое свойство порошка оксида магния обуслаливает его применение в качестве эталонного отражателя: в широком спектре его коэффициент отражения равен 1.
Одно из названий MgO — жженая магнезия, так как он получается при обжиге минералов магнезита и доломита:
Получить это вещество можно простым способом — взаимодействием магния и кислорода:
Будучи основным оксидом, MgO вступает в реакции с:
- водой, образуя гидроксид магния (о нюансах этой реакции расскажем чуть позже);
- с кислотами, образуя соли и воду;
- с кислотными оксидами, образуя сложные соли;
- c амфотерным оксидами при сплавлении образует сложные вещества — двойные оксиды.
Примеры реакций оксида магния
Растворение в кислотах:
- MgO + HCl (разб) → MgCl₂ + H₂O (для протекания реакции нужны неконцентрированные кислоты)
- MgO + H₂SO₄ → MgSO₄ + H₂O В реакциях с кислотами MgO показывает общие свойства оксидов (образуя соль и воду).
Реакции MgO с кислотными оксидами
MgO + SO₃ → MgSO₄ — образуется сульфат магния
MgO + СO₃ → MgСO₃ — образуется карбонат магния
Реакции с амфотерным оксидами:
Al₂O₃ + MgO → MgAl₂O₄
В этой реакции оксида магния с оксидом алюминия образуется алюминат магния (двойной оксид магния и алюминия). Реакция протекает при высокой температуре (свыше 1500 ⁰С).
Как MgO реагирует с водой?
Являясь основным оксидом, MgO взаимодействует с водой, образуя основание — гидроксид магния.
С холодной водой оксид магния реагирует очень медленно, но если реакцию проводить с водяным паром, реакция пойдет быстрее.
MgO + H₂O (вода в виде горячего пара) → Mg(OH)₂
В результате этой реакции образуется гидроксид магния
А вот если у экспериментатора есть полоска магния, можно провести очень зрелищный опыт:
- полоску металла частично опустить в стакан с водой;
- поджечь оставшуюся часть магния.
Mg + 2H₂O = Mg(OH)₂ + H₂↑
Горение магния продолжается даже в воде. При этом выделяющийся водород тоже вступает в реакцию горения.
Внимание! Не пытайтесь повторить этот опыт самостоятельно!
http://5terka.com/node/11278
http://melscience.com/RU-ru/articles/v-kakie-reakcii-vstupaet-oksid-magniya/