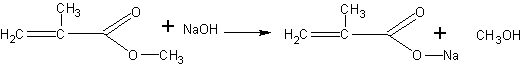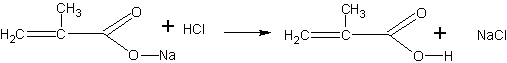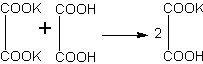Глава 10. КАРБОНОВЫЕ КИСЛОТЫ
Карбоновыми кислотами называют производные углеводородов, которые содержат в молекуле одну или несколько карбоксильных групп -COOH. Число карбоксильных групп определяет основность кислот. Монокарбоновые или одноосновные кислоты содержат одну группу –СООН, например, уксусная кислота СН3СООН. Дикарбоновые кислоты или двухосновные кислоты содержат две карбоксильные группы, например, щавелевая кислота, НООС-СООН. В зависимости от строения углеродного радикала, с которым связана карбоксильная группа, бывают алифатические, циклические и ароматические кислоты. Карбоновые кислоты с числом атомов углерода свыше шести называются высшими жирными кислотами. В зависимости от природы радикала, связанного с карбоксильной группой, карбоновые кислоты делятся на предельные и непредельные.
Химические свойства карбоновых кислот определяются строением карбоксильной группы. В этой группе электронная плотность связи О-Н смещена к атому кислорода, имеющему большую электроотрицательность. В свою очередь под влиянием поляризованной карбонильной группы такое смещение усиливается еще в большей степени. В результате облегчается отрыв атома водорода в виде протона — происходит процесс кислотной диссоциации:
R-COOH → R-COO — + H +
Карбоновые кислоты — слабые кислоты. Константы диссоциации и рК кислот приведены в табл. 2 (см. Приложение).
В химических реакциях участвует или протон карбоксильной группы, или вся карбоксильная группа (-СООН).
Опыт 24. Получение одноосновных карбоновых кислот
Опыт 24.1. Получение уксусной кислоты кислотным гидролизом этилацетата
В пробирку помещают 4 капли этилацетата и 2 капли 2н. раствора серной кислоты. Содержимое пробирки перемешивают и нагревают на водяной бане. Появляется запах уксусной кислоты:
Опыт 24.2. Получение уксусной кислоты из ацетата натрия
К трем каплям раствора ацетата натрия добавляет одну каплю раствора серной кислоты. Появляется резкий запах уксусной кислоты. Это доказывает, что уксусная кислота, как и все органические кислоты является слабой кислотой и вытесняется из растворов солей сильными минеральными кислотами:
Опыт 24.3. Получение муравьиной кислоты из хлороформа
Муравьиная кислота может рассматриваться как карбоновая кислота и как альдегид одновременно. Поэтому для нее характерна реакция «серебряного зеркала»
В первую пробирку помещают одну каплю хлороформа и 3 капли раствора гидроксида натрия. Содержимое пробирки аккуратно нагревают до тех пор, пока капля хлороформа не исчезнет.
НСCl3 + 4NaOH → HCOONa + 3NaCl + 2H2O
Во второй пробирке приготовляют аммиачный раствор оксида серебра (l) — реактив для открытия альдегидной группы. Для этого в пробирку помещают одну каплю раствора нитрата серебра и одну каплю раствора гидроксида натрия. Образовавшийся осадок Ag2O растворяют в растворе аммиака.
Для открытия образовавшегося формиата натрия вливают в первую пробирку заготовленный реактив из второй пробирки. Полученный раствор нагревают. Серебро восстанавливается на стенках пробирки в виде зеркального налета или в виде черного осадка . Химизм процесса:
Опыт 25. Химические свойства одноосновных карбоновых кислот
25.1. Кислотные свойства карбоновых кислот
В три пробирки помещают по 3 капли раствора уксусной кислоты. В первую пробирку добавляют одну каплю метилового оранжевого, во вторую- одну каплю лакмуса, а в третью- одну каплю фенолфталеина. В пробирках с метиловым оранжевым и с лакмусом появляется красное окрашивание, что указывает на кислотные свойства уксусной кислоты. Фенолфталеин остается бесцветным.
Опыт 25.2. Взаимодействие карбоновых кислот с металлами
В пробирку помещают маленький кусочек магниевой стружки и добавляют 6 капель уксусной кислоты. Наблюдается выделение пузырьков газа — водорода. Эта реакция является характерной реакцией взаимодействия разбавленных кислот с активными металлами:
Опыт 25.3. Разложение солей слабых кислот уксусной кислотой
В пробирку помещают несколько крупинок карбоната натрия или кальция и приливают 2 капли уксусной кислоты. Наблюдается интенсивное выделение углекислого газа. Это доказывает, что уксусная кислота является более сильной, чем угольная кислота:
Опыт 25.4. Гидролиз солей карбоновых кислот
а) В пробирку помещают 3 капли раствора ацетата натрия и одну каплю раствора фенолфталеина. Содержимое пробирки окрашивается в розовый цвет. Это доказывает, что соль уксусной кислоты подвергается гидролизу по аниону. Напишите уравнение гидролиза ацетата натрия.
б) В пробирку помещают несколько кристалликов ацетата натрия, 3 капли воды и 2 капли раствора хлорида железа (III) . Раствор нагревают до кипения. Выпадают хлопья красно-бурого цвета. Это доказывает, что уксусная кислота, как и другие карбоновые кислоты, является слабой кислотой. Поэтому ее соли со слабым основанием подвержены необратимому гидролизу:
Опыт 25.5. Разложение муравьиной кислоты.
В пробирку помещают 6 капель муравьиной кислоты и 6 капель концентрированной серной кислоты. Наблюдается бурное выделение газа. При поджигании он горит голубоватыми вспышками, что характерно для СО:
НСООН » СО + Н2 О
Это свойство разлагаться в присутствии серной кислоты отличает муравьиную кислоту от других карбоновых кислот.
Опыт 25.6. Окисление муравьиной кислоты перманганатом калия
В пробирку приливают 10 капель муравьиной кислоты, 2 мл 2н серной кислоты и 2 мл раствора перманганата калия. Пробирку закрывают пробкой с газоотводной трубкой, конец которой помещают в пробирку с известковой водой. Реакционную смесь нагревают над пламенем горелки. Через некоторое время розовая окраска раствора обесцвечивается и наблюдается выделение газа. Известковая вода мутнеет, что доказывает выделение углекислого газа. Реакция идет по схеме:
Расставьте стехиометрические коэффициенты в данном уравнении.
Опыт 25.7. Получение уксусноэтилового эфира (этилацетата)
Важнейший способ получения сложных эфиров — взаимодействие карбоновых кислот со спиртами (реакция этерификации) в присутствии водоотнимающих веществ.
а) Получение этилацетата из уксусной кислоты и этилового спирта
В сухую пробирку помещают 4 капли этилового спирта и 4 капли ледяной уксусной кислоты. Затем в пробирку добавляют 2 капли концентрированной серной кислоты и содержимое пробирки осторожно нагревают над пламенем горелки. Появляется запах этилацетата (запах лака для ногтей, запах клея «момент»):
б) Получение этилацетата из ацетата натрия и этилового спирта.
В пробирку помещают немного безводного ацетата натрия и 3 капли этилового спирта. Затем в пробирку добавляют 2 капли концентрированной серной кислоты и осторожно нагревают полученную смесь над пламенем горелки. Появляется характерный запах этилацетата:
Опыт 26. Химические свойства двухосновных карбоновых кислот.
Опыт 26.1. Разложение щавелевой кислоты при нагревании
Несколько кристалликов щавелевой кислоты нагревают в пробирке с газоотводной трубкой, конец которой опущен в пробирку с известковой водой. Газ, выделяющийся при нагревании, вызывает помутнение этого раствора – СО2. Одновременно ощущается резкий запах муравьиной кислоты:
НООС-СООН » СО2 + НСООН (муравьиная кислота)
Такая реакция декарбоксилирования происходит легко при нагревании щавелевой и малоновой кислот. Двухосновные кислоты с четырьмя и пятью атомами углерода в молекуле (янтарная и глутаровая) при нагревании отщепляют воду с образованием циклических ангидридов.
Опыт 26.2. Разложение щавелевой кислоты при нагревании с концентрированной серной кислотой
В пробирку помещают несколько кристалликов щавелевой кислоты и добавляют две капли концентрированной серной кислоты. Пробирку закрывают пробкой с газоотводной трубкой и нагревают на пламени газовой горелки. Выделяющийся газ поджигают. Он горит голубоватыми вспышками, так как образуется оксид углерода (II). Конец газоотводной трубки опускают в пробирку с известковым раствором, который мутнеет, что доказывает выделение углекислого газа. Щавелевая кислота разлагается полностью по схеме:
Опыт 26.3. Окисление щавелевой кислоты перманганатом калия.
В пробирку помещают несколько кристалликов щавелевой кислоты, две капли разбавленного раствора серной кислоты и две капли раствора перманганата калия. Пробирку закрывают пробкой с газоотводной трубкой, конец которой опускают в пробиркой с известковой водой. Реакционную смесь нагревают. Розовый цвет перманганата калия исчезает, а известковая вода мутнеет. Реакция протекает по схеме:
Расставьте стехиометрические коэффициенты в данном уравнении.
Опыт 27. Химические свойства непредельных одноосновных кислот.
Состав непредельных одноосновных кислот можно выразить общей формулой Сn H2n-1 COOH. Их химическая активность определяется, с одной стороны, — наличием карбоксильной группы, а с другой стороны, — наличием двойной связи. Как кислоты, они образуют соли, эфиры и другие, присущие кислотам, соединения. По своей силе непредельные кислоты превосходят соответствующие предельные кислоты. (см. табл. 2. Приложение). Как непредельные соединения, имеющие двойную связь, они способны к реакциям присоединения, окисления и полимеризации.
Опыт 27.1. Взаимодействие олеиновой кислоты с бромной водой
В пробирку наливают 5 капель бромной воды и 5 капель олеиновой кислоты. Смесь перемешивают и наблюдают обесцвечивание бромной воды:
Опыт 27.2. Окисление олеиновой кислоты перманганатом калия
В пробирку налвают 3 капли раствора перманганата калия, 2 капли раствора карбоната натрия и 3 капли олеиновой кислоты. Полученную смесь встряхивают и наблюдают, что фиолетовая окраска перманганата калия переходит в бурую. Выпадает осадок диоксида марганца. Реакция протекает по схеме
Расставьте стехиометрические коэффициенты в данном уравнении.
Опыт 28. Химические свойства ароматических карбоновых кислот.
Ароматические карбоновые кислоты по своему строению являются ароматическими углеводородами, у которых в бензольном кольце один или несколько атомов водорода замещены карбоксильными группами. Простейшим представителем одноосновных ароматических кислот является бензойная кислота, С6Н5-СООН.
Опыт 28.1. Получение бензоата натрия
Бензойная кислота при взаимодействии со щелочами образует соли – бензоаты. В пробирку помещают 0,5 г бензойной кислоты и прибавляют раствор гидроксида натрия до полного растворения кристаллов бензойной кислоты.
Если к прозрачному раствору бензоата натрия прилить раствор соляной кислоты, то снова выпадает осадок бензойной кислоты. Напишите уравнение соотвуетствующей реакци.
Опыт 28.2. Взаимодействие салициловой кислоты с хлоридом железа (III)
Салициловая кислота является о-оксибензойной кислотой:
Салициловая кислота образует с ионами трехвалентного железа комплексное соединение фиолетового цвета. В пробирку наливают 2 мл воды и добавляют несколько кристалликов салициловой кислоты. К полученному раствору добавляют 2 капли раствора хлорида железа (III). Окраска раствора становится фиолетовой. Напишите уравнение соответствующей реакци-и.
Опыт 28.3. Взаимодействие бензойной и салициловой кислот с бромной водой
Бензойная кислота бромируется только в присутствии катализатора. Салициловая кислота из-за наличия гидроксильной группы легко взаимодействует с бромной водой. В две пробирки наливают по 1 мл насыщенных растворов, соответственно, бензойной и салициловой кислот. В каждую пробирку добавляют по несколько капель насыщенной бромной воды. В пробирке с бензойной кислотой бромная вода не обесцвечивается. Напротив, салициловая кислота обесцвечивает бромную воду, образуя 4,6-дибромсалициловую кислоту. Напишите уравнение соответствующей реакции.
Опыт 28.4. Гидролиз ацетилсалициловой кислоты (аспирина)
В пробирку помещают 0,5 г ацетилсалициловой кислоты и приливают 1 мл воды. Содержимое пробирки нагревают и кипятят 2-3 мин. Затем в пробирку добавляют несколько капель раствора хлорида железа (III). Появляется фиолетовая окраска раствора, которая свидетельствует о том, что при нагревании усиливается гидролиз ацетилсалициловой кислоты с образованием салициловой и уксусной кислот.
Опыт 29.Получение и химические свойства жирных кислот.
Алифатические карбоновые кислоты с числом атомов углерода выше 6 называют высшими (жирными кислотами).
Название «жирных» эти кислоты получили потому, что большинство из них могут быть выделены из жиров. Они разделяются на предельные и непредельные. В качестве примеров можно привести следующие жирные кислоты.
а) предельные кислоты:
а) непредельные кислоты:
Природные и растительные жиры состоят из глицеридов — сложных эфиров глицерина и различных жирных кислот. Три гидроксила глицерина могут быть этерифицированы либо только одной кислотой, либо двумя или тремя различными кислотами. Содержание непредельных кислот в жирах очень сильно влияет на их физические и химические свойства. Если жир содержит, в основном, непредельные кислоты, то это жидкий жир (масло). Для них характерны реакции окисления и полимеризации. В результате этого такие масла образуют на воздухе эластичные, гибкие и прочные пленки. Такие масла называют высыхающими — льняное, тунговое.
Жиры, содержащие предельные кислоты, — твердые жиры (свиной жир, говяжий жир). Однако, если твердый жир содержит примесь непредельных кислот, то он способен «прогоркать»- приобретать неприятный вкус и запах. Поэтому одним из основных анализов жиров является анализ на содержание непредельных кислот — непредельность.
Опыт 29.1. Определение непредельности жиров раствором йода
Анализ на непредельность выполняют с помощью йода. Степень непредельности выражают «йодным числом», т.е. числом граммов йода, поглощенного 100 граммами жира.
В две пробирки помещают по 10 капель растительного масла и растопленного говяжьего или свиного жира. В каждую пробирку добавляют 20 капель хлороформа и содержимое пробирок энергично перемешивают. Получаются прозрачные растворы. Затем в каждую пробирку прибавляют по две капли раствора крахмала и по каплям, при энергичном встряхивании, спиртовой раствор йода до появления устойчивого синего окрашивания. Считают число капель раствора йода, пошедшего на реакцию, и делают вывод о степени непредельности растительного масла и жира.
Опыт 29.2. Взаимодействие жиров с бромом.
В пробирку помещают 4 капли растительного масла и добавляют 1-2 капли раствора брома в тетрахлорметане. Окраска брома исчезает, что указывает на содержание непредельных кислот в масле:
Опыт 29.3. Окисление растительных масел водным раствором перманганата калия (реакция Вагнера)
В пробирку помещают 3 капли растительного масла, 3 капли раствора карбоната натрия и 2 капли водного раствора перманганата калия. Смесь энергично встряхивают. При этом малиновая окраска перманганата калия исчезает и выпадает бурый осадок диоксида марганца. Это указывает на окисление перманганатом калия остатков непредельных кислот, входящих в состав масла. Реакция протекает по схеме:
Расставьте стехиометрические коэффициенты в данном уравнении реакции
Опыт 29.4 Получение стеариновой кислоты из мыла
Мыла представляют собой щелочные соли высших жирных кислот. В качестве примера можно привести С17Н35СООNa — стеарат натрия (мыло).
В промышленности для получения мыла применяются животные жиры (сало низких сортов, жир морских животных), хлопковое, пальмовое, кокосовое масла, гидрогенезированные жиры. При нагревании их с раствором гидроксида натрия или калия происходит их омыление, т.е. образование солей жирных кислот. При этом образуется густой раствор (мыльный клей) содержащий воду, глицерин и соли жирных кислот. Для выделения мыла к полученному раствору добавляют насыщенный раствор хлорида натрия («высаливание» мыла). При этом мыло отделяется от раствора и всплывает на поверхность. Натриевые мыла после застывания представляют собой твердую массу и называются «ядровыми мылами». Мягкие или жидкие мыла являются калиевыми мылами.
Разные жиры имеют различный состав и содержат как предельные, так и непредельные жирные кислоты. Поэтому мыла так же имеют переменный состав в зависимости от исходного сырья.
В пробирку помещают маленький кусочек мыла, добавляют
5 капель воды и тщательно взбалтывают содержимое пробирки в течение 1-2 мин. После этого содержимое пробирки нагревают в пламени горелки. Натриевое мыло хорошо растворяется в воде. К раствору мыла, добавляют одну каплю раствора серной кислоты и слегка подогревают содержимое пробирки в пламени горелки. Всплывает белый маслянистый слой свободных жирных кислот, водный раствор осветляется. Содержимое пробирки оставляют для следующего опыта. Химизм процесса:
Опыт 29.5. Доказательство непредельности жирных кислот, входящих в состав мыла
В пробирку с выделенными в предыдущем опыте жирными кислотами добавляют 3 капли бромной воды и энергично перемешивают. Бромная вода обесцвечивается. Следовательно, в состав жирных кислот, выделенных из мыла, входят и непредельные кислоты:
Опыт 29.6. Гидролиз спиртового раствора мыла
Все мыла, являясь щелочными солями слабых кислот, в воде подвергаются гидролизу с образованием свободной жирной кислоты и гидроксида щелочного металла, поэтому их растворы имеют щелочную реакцию. В сухую пробирку помещают кусочек мыла и 4 капли спирта. Содержимое пробирки перемешивают и к полученному раствору добавляют каплю фенолфталеина. Окраска раствора не меняется. К спиртовому раствору мыла прибавляют по каплям дистиллированную воду. По мере прибавления воды появляется розовое окрашивание, что указывает на щелочную реакцию полученного раствора, т.к. добавление воды вызывает гидролиз мыла. В результате образуются малодиссоциированные жирные кислоты и гидроксид натрия. Реакция мыла в водных растворах всегда щелочная. Напишите уравнение реакции.
Опыт 29.7. Образование нерастворимых в воде кальциевых солей жирных кислот
Мыла делятся на растворимые в воде и нерастворимые. Натриевые и калиевые мыла в воде растворяются хорошо. Соли щелочно-земельных металлов (Cа, Mg) и некоторых тяжелых металлов (например, Сu) -так называемые металлические мыла — в воде нерастворимы. Поэтому моющая способность мыла в жесткой воде, содержащей растворенные соли Cа и Mg сильно падает. В результате обменной реакции образуются кальциевые или магниевые мыла, нерастворимые в воде, и выпадающие в виде хлопьев.
В пробирку помещают 3 капли раствора мыла и одну каплю раствора хлорида кальция. Содержимое пробирки перемешивают. Выпадает белый осадок кальциевых солей жирных кислот:
Кальциевые соли жирных кислот (кальциевое мыло) нерастворимы в воде. Кальциевое мыло выделяется при мытье в жесткой воде.
Опыт 29.8. Образование нерастворимого в воде медного мыла
В пробирку помещают I каплю раствора мыла и 4 капли раствора сульфата меди (II) . Выпадает голубовато-белый осадок медного мыла. Раствор нагревают до кипения, при этом медное мыло всплывает на поверхность раствора в виде зеленого кольца. Если в растворе остается не вошедшее в реакцию натриевое мыло, то зеленого кольца не получится. В таком случае добавляют еще 2-3 капли раствора сульфата меди (II) и снова нагревают до кипения.
Опыт 29.9. Омыление жиров спиртовым раствором щелочи
В широкую пробирку помещают 2 мл касторового масла и приливают 6 мл спиртового раствора гидроксида натрия. Смесь перемешивают стеклянной палочкой и нагревают на водяной бане до начала кипения. Омыление ведут 3-5 минут, пока жидкость не станет однородной. Для определения конца омыления помещают в пробирку несколько капель полученной смеси, добавляют 4-5 мл воды и нагревают раствор при встряхивании на пламени горелки. Если смесь растворяется в воде нацело, без выделения капель жира, то омыление можно считать законченным. Если выделяются капли жира, то продолжают нагревать смесь на водяной бане еще несколько минут, а затем снова проверяют полноту омыления. К полученной густой жидкости добавляют 6-7 мл насыщенного раствора хлорида натрия. Жидкость мутнеет и выделяется слой мыла, всплывающий на поверхность. Дают смеси отстояться, затем охлаждают пробирку холодной водой.
Опыт 30. Химические свойства аминокислот
Аминокислоты — это карбоновые кислоты, которые содержат аминогруппу. В общем виде строение аминокислот выражается формулой: H2N-R-COOH. Количество карбоксильных групп определяет основность аминокислот. Различают одноосновные и двухосновные аминокислоты. В зависимости от количества аминогрупп встречаются моноаминокислоты и диаминокислоты. Положение аминогруппы по отношению к карбоксильной группе определяют α-, β- и γ-аминокислоты. Греческая буква характеризует удаленность аминогруппы от карбоксильной группы. В природе встречаются только α-аминокислоты, которые получаются при гидролизе белковых веществ животного и растительного происхождения. Все α-аминокислоты имеют тривиальные названия, которые приводятся в табл. 3. Приложение. Простейшим представителем α-аминокислот является аминоуксусная кислота NH2-CH2-COOH.
Ион водорода, получающийся при диссоциации карбоксильной группы α-аминокислоты, присоединяется к ее аминогруппе. В результате внутримолекулярной нейтрализации кислотной и основной групп образуются биполярные ионы:
Н2N – CHR — COOH 
Высокая растворимость аминокислот в воде объясняется их ионным характером. Значение рН раствора, при котором положительный и отрицательный заряды в молекуле аминокислоты нейтрализуют друг друга, называется изоэлектрической точкой pI. Для каждой аминокислоты характерна своя величина pI, которая определяется строением боковой цепи R (табл. 3. Приложение). При добавлении кислоты или щелочи в раствор аминокислоты ее частицы приобретают тот или иной заряд: при рН, большим, чем pI, образуются анионы аминокислоты; при меньшем рН — ее катионы:
H3N + -CH2-COOН 

Под действием электрического тока, в зависимости от рН среды, частицы движутся к аноду или катоду. Это явление используется для электрофоретического разделения аминокислот и их идентификации (электрофорез на носителе).
В настоящее время при гидролизе белков удалось выделить 26 α-аминокислот. Некоторые из этих α-аминокислот не вырабатываются в живом организме. Организм получает их только с пищей. Такие α-аминокислоты (валин, лейцин, изолейцин, лизин, метионин, треонин, фенилаланин и триптофан) называются незаменимыми.
Поскольку аминокислоты являются амфотерными соединениями, то они могут давать соли как с основаниями, так и с кислотами.
Опыт 30.1. Кислотно-основные свойства аминокислот.
В первую пробирку добавляют 3 капли раствора соляной кислоты и I каплю лакмуса. Во вторую пробирку добавляют 3 капли раствора гидроксида натрия и I каплю фенолфталеина. Затем в обе пробирки по каплям добавляют раствор аминоуксусной кислоты (глицина) до изменения цвета индикаторов. Объяснить наблюдаемый эффект. Химизм процесса:
хлорид аминоуксусной кислоты
б) Щелочная среда
Опыт 30.2. Образование медной соли аминоуксусной кислоты
В пробирку помещают 2 капли раствора сульфата меди (II) и I каплю раствора гидроксида натрия. Выпадает синий осадок гидроксида меди (II). В пробирку прибавляют по каплям раствор аминоуксусной кислоты. Содержимое пробирки постоянно перемешивают. Осадок растворяется с образованием прозрачного раствора, окрашенного в темно-синий цвет. Образуется внутрикомплексное соединение — аминоацетат меди:
В этом соединении связь между атомами меди и азота координационная и образуется за счет свободной пары электронов азота аминогруппы. Такие соли очень устойчивы. Для доказательства этого к полученному раствору внутренней комплексной соли добавляют 2 капли раствора гидроксида натрия. Осадок гидроксида меди (II) не образуется.
Опыт 30.3. Действие азотистой кислоты на аминокислоты
На этой реакции основано количественное определение аминогрупп в аминокислотах, а также в белках и продуктах их распада. Выделяющийся азот определяется объемным методом.
В пробирку помещают 2 капли раствора аминоуксусной кислоты, 2 капли раствора нитрита натрия и 2 капли раствора соляной кислоты. При встряхивании содержимого пробирки выделяются пузырьки газа:
Опыт 30.4. Цветные реакции аминокислот с нингидрином
Различные α-аминокислоты с нингидрином образуют окрашенные соединения, отличающиеся окраской. Реакции с нингидрином очень чувствительны, поэтому их часто применяют для качественного анализа α-аминокислот.
В несколько пробирок приливают по 2 мл различных аминокислот. В каждую пробирку добавляют по три капли 0,1%-ного раствора нингидрина в ацетоне. Содержимое пробирки нагревают на водяной бане. Через некоторое время появляется окраска раствора.
Составьте таблицу зависимости оттенка окраски раствора от аминокислоты.
Опыт 30.5. Окислительное расщепление аминокислот
Строение аминокислот может быть установлено окислительным расщеплением, в результате которого образуется альдегид, аммиак и углекислый газ. В качестве окислителя могут применяться перекиси, персульфаты и др.
Берут две пробирки. В первую пробирку приливают 3 капли перманганата калия, 6 капель раствора серной кислоты и 4 капли раствора аминоуксусной кислоты (глицина). Пробирку закрывают пробкой с газоотводной трубкой, конец которой помещают во вторую пробирку с дистиллированной водой. Раствор в первой пробирке обесцвечивается. Глицин окисляется до уксусного альдегида, имеющего запах зеленых яблок. Процесс осуществляется по схеме:
Расставьте стехиометрические коэффициенты в уравнении реакции.
Выделяющиеся газы растворяются во второй пробирке. Наличие во второй пробирке ионов аммония определяется с помощью реактива Несслера.
Опыт 30.6. «Аминокислотное» брожение
Аминокислоты расщепляются дрожжами. В результате этого процесса образуются спирты, аммиак и углекислый газ.
В пробирку наливают дрожжевой раствор, добавляют 2 капли гидроксида натрия и 6 капель аминоизовалериановой кислоты (валина). Выделяющийся 2-метилпропанол определяют по резкому запаху. Процесс осуществляется по схеме:
1. На нейтрализацию смеси раствора уксусной кислоты и фенола массой 30 г израсходовано 100 мл 2н раствора гидроксида натрия. При действии бромной воды на то же количество исходного раствора образовался осадок массой 33,1 г. Определите массовую долю уксусной кислоты и фенола в растворе.
2. Напишите уравнение реакции получения масляной кислоты из бутана.
3. На нейтрализацию одноосновной предельной кислоты массой 3, 7 г израсходовано 100 мл 0, 5н раствора гидроксида калия. Напишите структурную формулу этой кислоты.
4. Получите стеариновую кислоту гидролизом соответствующего жира.
5. Для нейтрализации 125 г смеси этилового спирта и уксусной кислоты потребовалось 76, 92 мл 5%-ного раствора гидроксида натрия, плотность которого 1, 04 г/мл. При действии на то же количество раствора избытка металлического натрия выделилось 3, 36 л водорода (н.у.). Определите массовую долю этилового спирта и уксусной кислоты в исходном растворе.
6. С помощью каких реакций можно получить аминопропионовую кислоту из пропена.
7. Какие α-аминокислоты называются незаменимыми?
НЕПРЕДЕЛЬНЫЕ КИСЛОТЫ
Из класса непредельных одноосновных карбоновых кислот наибольший интерес для изучения представляют акриловая и олеиновая кислоты. Первая — как первый член гомологического ряда, производные которой имеют большое значение при получении синтетических материалов. Олеиновая кислота является представителем непредельных кислот, входящих в состав жиров.
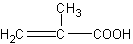
Вместо акриловой кислоты СН2=СН—СООН можно воспользоваться ее ближайшим и более доступным гомологом — метакриловой кислотой, эфиры которой применяются для получения широко известных полимерных продуктов (органического стекла).
Получение метакриловой кислоты (по В.В.Некрасову). Метакриловая кислота может быть получена гидролизом сложного эфира — метилметакрилата. Метилметакрилат для этого опыта может быть в свою очередь получен деполимеризацией полиметилметакрилата (органического стекла), как это описано на с. 68. Гидролиз проводится в присутствии щелочи. Метакриловая кислота при этом образует соль, из которой она может быть выделена действием более сильной кислоты:
Помещают в пробирку 2 мл метилового эфира метакриловой кислоты (метилметакрилата) и 4 мл концентрированного раствора едкого натра. Чтобы смесь получилась гомогенной, добавляют 1 мл этанола и встряхивают. Через 15—20 мин переливают жидкость в фарфоровую чашку и выпаривают досуха на слабом пламени. Остаток представляет собой натриевую соль метакриловой кислоты с возможной примесью щелочи. Дальнейшая задача сводится к выделению кислоты из соли. Для этого сухой остаток переносят в пробирку и, охлаждая ее водой, добавляют несколько миллилитров концентрированной соляной кислоты (до кислой реакции на индикатор). После отстаивания смеси метакриловая кислота собирается сверху в виде маслянистой жидкости с характерным запахом. Кислоту переносят при помощи пипетки в другую пробирку.
Свойства метакриловой кислоты. Метакриловая кислота, будучи соединением непредельным, реагирует с бромной водой, перманганатом калия и легко полимеризуется.
а) К небольшому количеству (нескольким каплям) метакриловой кислоты приливают бромную воду и смесь встряхивают. Бромная вода обесцвечивается вследствие присоединения брома по месту двойной связи. Учащиеся составляют уравнение реакции.
Подобным образом проводится опыт с водным раствором пер-манганата калия.
б) К небольшому количеству метакриловой кислоты добавляют несколько крупинок перекиси бензоила в качестве инициатора реакции и нагревают до начала кипения. Кислота быстро полимеризуется.
Непредельность олеиновой кислоты. Олеиновая кислота является единственным представителем класса непредельных кислот, входящих в состав жиров и изучаемых в школьном курсе химии. Непредельность ее может быть проиллюстрирована действием обычных реактивов на двойную связь: бромной воды и раствора перманганата калия.
К 5—8 мл олеиновой кислоты в пробирке или колбочке приливают равный объем бромной воды или раствора перманганата калия и встряхивают. Окраска брома и перманганата калия исчезает вследствие присоединения по месту двойной связи.
ЩАВЕЛЕВАЯ КИСЛОТА
Наибольшее значение в этом разделе имеют опыты, связанные со строением щавелевой кислоты и ее двухосновностью.
Получение щавелевой кислоты из муравьиной. Первым подтверждением структурной формулы щавелевой кислоты может служить получение ее солей из солей муравьиной кислоты.
Формиат натрия при нагревании выделяет водород; одновременно образуется оксалат натрия
Очевидно, что из молекулы соли при этом уходит единственный атом водорода. А так как радикалы неспособны к сколько-нибудь длительному существованию, то они рекомбинируются, образуя молекулы новой соли, которой отвечает кислота
В пробирке, закрытой пробкой с вертикальной трубкой, нагревают в пламени горелки сухой формиат натрия.
Соль плавится и затем (при сильном нагревании) разлагается. Устанавливают выделение водорода, собирая его в пробирку или поджигая через некоторое время у отводной трубки.
Разложение щавелевой кислоты при нагревании с серной кислотой. Если щавелевая кислота имеет формулу
то можно предположить, что при отнятии от нее элементов воды должны выделяться углекислый газ и оксид углерода (II). Этот факт послужил бы подтверждением структурной формулы кислоты.
Учащимся можно предложить самим придумать прибор, в котором следовало бы провести эту реакцию так, чтобы обнаружить оба образующихся газа.
Опыт может быть осуществлен, например, в приборе, изображенном на рис. 32.
В небольшую колбочку помещают 2—3 г щавелевой кислоты и двойной объем концентрированной серной кислоты. В пробирку с отводной трубкой наливают известковую воду. При нагревании смеси кислот на горелке известковая вода мутится. Когда можно будет предположить, что воздух вытеснен из прибора, поджигают у отводной трубки пробирки оксид углерода (II), который горит характерным синим пламенем.

Окисление щавелевой кислоты. Щавелевая кислота окисляется легче уксусной. Распадаясь на воду, углекислый газ и оксид углерода (II), она, очевидно, нуждается в незначительном количестве кислорода, чтобы дать конечные продукты окисления — углекислый газ и воду. Для простоты можно считать, что действие окислителя сводится к превращению угарного газа в углекислый.
В качестве окислителя может быть взят не раз применявшийся в подобных случаях перманганат калия с серной кислотой.
В небольшую колбочку с отводной трубкой наливают 5 мл концентрированного раствора щавелевой кислоты и равный объем разбавленной серной кислоты (1 : 5).
Из капельной воронки в колбу приливают постепенно 10 мл не слишком слабого раствора перманганата калия. При нагревании колбы фиолетовая окраска быстро исчезает и наблюдается энергичное выделение углекислого газа. Его пропускают в известковую или баритовую воду или же собирают в цилиндр и затем испытывают соответствующим способом. Уравнение реакции можно представить следующим образом:
Образование кислых и средних солей щавелевой кислоты. В молекуле щавелевой кислоты имеются две карбоксильные группы, следовательно, щавелевая кислота двухосновная.
Как кислота двухосновная, щавелевая кислота может давать соли кислые и средние. Это может быть показано на реакции нейтрализации.
Растворяют 12 г щавелевой кислоты примерно в 20 мл воды и делят раствор пополам. К одной части раствора приливают понемногу концентрированный раствор гидроксида калия. Наблюдают, что сначала образуется осадок, который при дальнейшем прибавлении щелочи растворяется. Очевидно, что сначала получается кислая соль (гидрооксалат калия), нерастворимая в воде. В дальнейшем, при добавлении щелочи, эта соль превратилась в среднюю, растворимую в воде:
Если теперь к раствору средней соли прилить вторую порцию щавелевой кислоты, то снова образуется обильный осадок гидрооксалата калия:
БЕНЗОЙНАЯ КИСЛОТА
Изучение бензойной кислоты на уроке не входит в программу по химии. Учителя иногда посвящают несколько минут ознакомлению с нею лишь для того, чтобы показать, как образуются кислоты в ароматическом ряду и что они собой представляют. Если ранее ставился опыт окисления бензальдегида в бензойную кислоту, здесь можно познакомить учащихся лишь с физическими свойствами ее.
Растворимость бензойной кислоты в воде. Встряхивая в пробирке очень небольшое количество кристаллов бензойной кислоты с водой, убеждаются, что заметного растворения не происходит. При нагревании пробирки происходит растворение кислоты, а при охлаждении она вновь кристаллизуется. Убеждаются, что водный раствор бензойной кислоты окрашивает лакмус в красный цвет.
Растворимость бензойной кислоты в щелочах. К небольшому количеству бензойной кислоты в пробирке прибавляют воду. Убедившись, что кислота не растворяется, добавляют по каплям крепкий раствор щелочи, пока кислота не растворится. После этого подкисляют раствор соляной кислотой. Выделяются мелкие кристаллы бензойной кислоты:
Возгонка бензойной кислоты. Собирают прибор из двух пробирок разной величины, как показано на рис. 33. В большую пробирку на дно насыпают бензойную кислоту, а маленькая пробирка наполнена холодной водой. При нагревании прибора на пламени горелки бензойная кислота возгоняется и осаждается в виде белых кристаллов на пробирке-холодильнике.
С помощью бензойной кислоты учащимися может быть осуществлена имитация «зимнего пейзажа».
На картоне (с отверстиями) или на листе пористой (фильтровальной) бумаги монтируют небольшой макет сада. Под картоном (бумагой) нагревают в фарфоровой или железной чашке бензойную кислоту, накрыв всю установку стеклянным колпаком. Возгоняющаяся кислота, проходя через отверстия в картоне или поры в бумаге, осаждается на «деревьях» в виде красивого инея. Следует остерегаться попадания паров бензойной кислоты в атмосферу.
Получение бензойной кислоты окислением бензальдегида. Бензальдегид легко окисляется в бензойную кислоту кислородом воздуха.
На стеклянную пластинку, часовое стекло или в фарфоровую чашку помещают несколько капель бензальдегида. Через несколько минут начинают появляться кристаллы. К концу урока весь альдегид превращается в кислоту.
Взяв для опыта несколько миллилитров альдегида, таким способом можно получить бензойную кислоту в количестве, необходимом для демонстрации опытов с ней.
Получение бензола из бензойной кислоты (см. опыт на с. 63).
Опыты по химии. Карбоновые кислоты
Взаимодействие бромной воды с олеиновой кислотой
Олеиновая кислота относится к непредельным карбоновым кислотам. Непредельность соединений можно обнаружить с помощью качественных реакций с бромной водой или раствором перманганата калия. В данном случае воспользуемся бромной водой. К олеиновой кислоте прибавим бромную воду и энергично перемешаем содержимое пробирки. Происходит обесцвечивание бромной воды. Мы доказали, что олеиновая кислота непредельная карбоновая кислота.
СН3 – (СН2)7 – СН=СН – (СН2)7 – СООН + Вr2 = СН3 – (СН2)7 – СНBr – СНBr – (СН2)7 – СООН
Оборудование: пробирка, штатив для пробирок.
Техника безопасности. Соблюдать правила работы с бромом (бромной водой).
Постановка опыта и текст – к.п.н. Павел Беспалов.
Взаимодействие уксусной кислоты с карбонатом натрия
Уксусная кислота – слабая кислота. Но она способна вытеснять более слабые кислоты из их солей. Убедимся в этом. К раствору карбоната натрия прильем раствор уксусной кислоты. Наблюдается обильное выделение углекислого газа.
Уксусная кислота вытеснила угольную кислоту из раствора ее соли. Угольная кислота – непрочное соединение, она распадается на углекислый газ и воду.
2СН3СООН + Na2CO3 = H2O + CO2 + 2CH3COONa
Оборудование: химические стаканы.
Техника безопасности. Соблюдать правила работы с горючими газами.
Постановка опыта и текст – к.п.н. Павел Беспалов.
Взаимодействие уксусной кислоты с металлами
Уксусной кислоте, как и неорганическим кислотам, присущи общие свойства кислот. Убедимся в том, что эта кислота способна реагировать с металлами. В две пробирки поместим кусочки магния и цинка. Прильем к ним раствор уксусной кислоты. В пробирке с магнием идет энергичная реакция – выделяется водород. В пробирке с цинком, менее активным металлом, выделение водорода едва заметно.
2СН3СООН + Мg = H2 + ( CH3COO)2 Mg
2СН3СООН + Zn = H2 + ( CH3COO)2 Zn
При взаимодействии металлов с раствором уксусной кислоты образуется водород и соли уксусной кислоты. Соли уксусной кислоты называются ацетатами.
Оборудование: штатив для пробирок, пробирка, горелка, зажим для пробирок.
Техника безопасности. Соблюдать правила работы с кислотами.
Постановка опыта и текст – к.п.н. Павел Беспалов.
Взаимодействие уксусной кислоты с оксидом меди (II)
Как и неорганические кислоты, уксусная кислота реагирует с оксидами металлов. Проведем реакцию между оксидом меди (II) и уксусной кислотой. При обычных условиях реакция идет очень медленно. Нагреем смесь на пламени горелки. Наблюдается растворение оксида меди и появление голубой окраски раствора. В пробирке образовался ацетат меди (II).
2СН3СООН + CuO = H2О + ( CH3COO)2 Cu
Оборудование: штатив для пробирок, пробирка, горелка, зажим для пробирок.
Техника безопасности. Соблюдать правила работы с кислотами.
Постановка опыта и текст – к.п.н. Павел Беспалов.
Взаимодействие уксусной кислоты с раствором щелочи
Реакция нейтрализации характерна для всех кислот. Нальем в бюретку раствор уксусной кислоты. В колбу для титрования – раствор гидроксида натрия. Прибавим к щелочи немного фенолфталеина. Раствор окрашивается в малиновый цвет. Прибавляем из бюретки раствор кислоты к раствору щелочи. Происходит нейтрализация щелочи. Когда вся щелочь переходит в соль – малиновая окраска исчезает. В растворе образовалась соль – ацетат натрия.
СН3СООН + NaOH = CH3COONa + H2O
Оборудование: штатив, бюретка, стакан химический, коническая колба.
Техника безопасности. Соблюдать правила работы с растворами кислот и щелочей.
Постановка опыта и текст – к.п.н. Павел Беспалов.
Возгонка бензойной кислоты
Бензойная кислота – ароматическая карбоновая кислота. Ее особенность – способность к возгонке. Возгонка — переход из твердого состояния в пароообразное, минуя жидкое. В стакан с бензойной кислотой положим еловую ветку и закроем колбой. В колбе – холодная вода. Колба будет служить и крышкой, и холодильником. Бензойная кислота при легком нагреве переходит из твердого состояния – в парообразное. Соприкасаясь с холодным дном колбы, пары бензойной кислоты охлаждаются – и конденсируются в виде кристалликов бензойной кислоты.
Оборудование: химический стакан, штатив, огнезащитная прокладка, колба круглодонная, горелка.
Техника безопасности. Соблюдать правила работы с нагревательными приборами. Бензойная кислота вызывает раздражение дыхательных путей. После проведения опыта дать прибору остыть и лишь после этого его можно разбирать.
Постановка опыта и текст – к.п.н. Павел Беспалов.
Гидролиз ацетата натрия
Уксусная кислота – слабый электролит. Ацетат натрия – соль образованная сильным основанием и слабой кислотой. При растворении этой соли в воде создается щелочная среда. Особенностью кристаллогидрата ацетата натрия является то, что он при нагревании легко плавится и ацетат натрия растворяется в своей кристаллизационной воде. Смешает ацетат натрия с сухим индикатором фенолфталеином. Полученную смесь нагреем. Появляется малиновая окраска. Соль частично расплавилась, в расплаве появились гидроксид- ионы.
CH3COONa + HOН = СН3СООН + NaОН
CH3COO — + HOН = СН3СООН + ОН —
При охлаждении соль кристаллизуется, равновесие смещается в сторону образования ацетата натрия, гидроксид-илны исчезают, и окраска пропадает. Опыт доказывает, что уксусная кислота является слабой кислотой.
Оборудование: штатив для пробирок, пробирки, горелка, зажим для пробирок.
Техника безопасности. Соблюдать правила работы с нагревательными приборами.
Постановка опыта и текст – к.п.н. Павел Беспалов.
Горение уксусной кислоты на воздухе
Безводная уксусная кислота – огнеопасное вещество, ее пары легко загораются. Убедимся в этом. Нагреем уксусную кислоту до кипения. При поднесении горящей лучины пары кислоты загораются. При горении уксусной кислоты образуются углекислый газ и вода.
СН3СООН + 2О2 = 2H2О + 2СО2
Склянки с уксусной кислотой хранят в металлических контейнерах.
Оборудование: штатив для пробирок, пробирка, горелка, лучина.
Техника безопасности. Соблюдать правила работы с кислотами.
Постановка опыта и текст – к.п.н. Павел Беспалов.
Замораживание уксусной кислоты
Безводная уксусная кислота при ее охлаждении примерно до 15 0 С переходит в кристаллическое состояние. В этом состоянии она очень похожа по внешнему виду на лед. Поэтому безводную уксусную кислоту называют ледяной. Приготовим охлаждающую смесь из воды и льда. Опустим в нее пробирку с уксусной кислотой. Через некоторое время уксусная кислота кристаллизуется.
Оборудование: химический стакан, пробирка, термометр, штатив.
Техника безопасности. Соблюдать правила работы с кислотами.
Постановка опыта и текст – к.п.н. Павел Беспалов.
Карбоновые кислоты – слабые электролиты
Слабые электролиты — это вещества, которые частично распадаются на ионы при растворении в воде. Обнаружить ионы в растворе можно с помощью прибора для изучения электропроводности. Если вещество или его раствор распадается на ионы, то лампочка прибора загорается. Проверим электропроводность уксусной кислоты. Опускаем электроды в концентрированную уксусную кислоту. Лампочка не загорается.
Разбавим уксусную кислоту водой и вновь проверим электропроводность. Лампочка не горит. Прибавим к раствору уксусной кислоты большой объем воды. Лампочка загорается. Мы убедились в том, что уксусная кислота — слабый электролит.
Уксусная кислота в значительной степени распадается на ионы лишь при большом разбавлении водой.
Оборудование: стакан химический, пипетка, набор для опытов с электрическим током.
Техника безопасности. Соблюдать правила работы с кислотами и правила работы с электроприборами.
Постановка опыта и текст – к.п.н. Павел Беспалов.
Образование нерастворимых кальциевых солей жирных кислот
Кальциевые соли жирных кислот нерастворимы в воде. Это можно наблюдать в следующем опыте. К раствору мыла прильем немного раствора хлорида кальция. Выпадает обильный осадок нерастворимого стеарата кальция.
2С17Н35СООNa + СаСI2 =(C17 H35COO)2Ca + 2NaCI
Такой процесс происходит при мытье в жесткой воде. Поэтому мыло в жесткой воде плохо мылится.
Оборудование: штатив для пробирок, пробирки.
Техника безопасности. Опыт безопасен.
Постановка опыта и текст – к.п.н. Павел Беспалов.
Окисление муравьиной кислоты раствором перманганата калия
Муравьиная кислота отличается по строению от всех остальных карбоновых кислот. Поэтому она совмещает свойства и кислоты и альдегида. Альдегиды, как известно, легко окисляются. Прильем к раствору муравьиной кислоты раствор перманганата калия. Нагреем смесь. Происходит обесцвечивание раствора. Муравьиная кислота окислилась до углекислого газа и воды.
НСООН + [О]= H2О + CO2
Оборудование: штатив для пробирок, пробирки, горелка, зажим для пробирок.
Техника безопасности. Соблюдать правила работы с кислотами и нагревательными приборами.
Постановка опыта и текст – к.п.н. Павел Беспалов.
Разложение муравьиной кислоты
Под действием водоотнимающих средств муравьиная кислота разлагается с выделением монооксида углерода. В быту он носит название угарный газ. В качестве водоотнимающего средства используем серную кислоту. В пробирку с муравьиной кислотой прибавим концентрированную серную кислоту. Сразу же начинается бурная реакция. Подожжем выделяющийся угарный газ. Он горит голубым пламенем.
НСООН = H2О + CO
Эту реакцию используют в лаборатории для получения угарного газа.
Оборудование: пробирка, зажим для пробирок, газоотводная трубка.
Техника безопасности. Соблюдать правила работы с кислотами. Опыт проводить под тягой.
Постановка опыта и текст – к.п.н. Павел Беспалов.
Растворимость в воде различных карбоновых кислот
Уксусная и масляная кислота при нормальной температуре – жидкости, стеариновая кислота — твердое вещество. Посмотрим, как эти карбоновые кислоты растворяются в воде. В три пробирки с водой добавим разные карбоновые кислоты. Уксусная и масляная кислоты хорошо растворяются в воде, а стеариновая кислота в воде не растворяется. Фиолетовый раствор лакмуса изменяет цвет лишь в растворах уксусной и масляной кислот. В пробирке со стеариновой кислотой лакмус остается фиолетовым.
Оборудование: пробирки, штатив для пробирок.
Техника безопасности. Соблюдать правила безопасности при работе с кислотами.
Постановка опыта и текст – к.п.н. Павел Беспалов.
http://helpiks.org/6-41730.html
http://www.yoursystemeducation.com/opyty-po-ximii-karbonovye-kisloty/