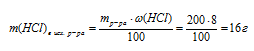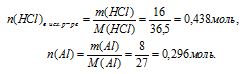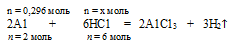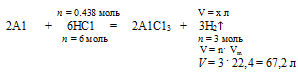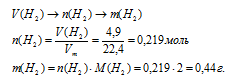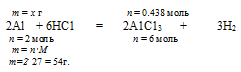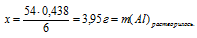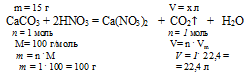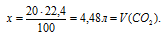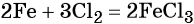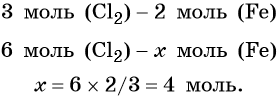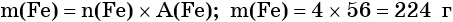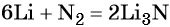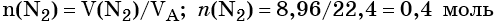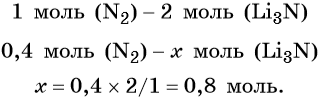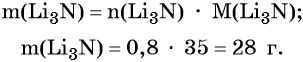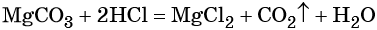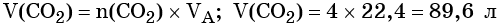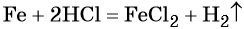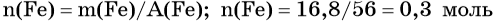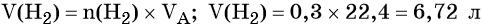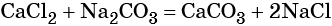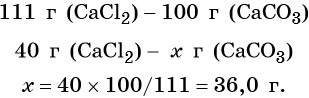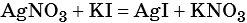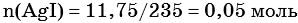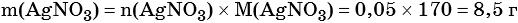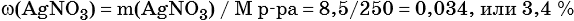Определение объема выделившегося газа в реакции, если одно вещество взято в избытке
Определение избытка-недостатка
Задача 6.
Определите объем газа (н.у.), который получится, если 8 г алюминия поместить в 200 г 8% -ного раствора соляной кислоты. Найдите массу раствора после реакции.
Дано:
масса алюминия: m(А1) = 8 г;
масса соляной кислоты: mр-ра(НС1) = 200 г;
массовая доля хлороводорода в соляной кислоте: (НС1) = 8% .
Найти:
объем выделившегося газа;
массу раствора после реакции.
Решение:
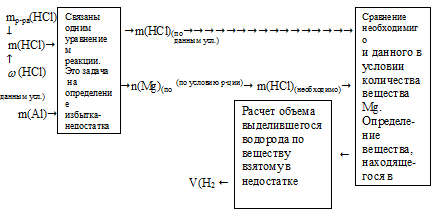
Сначала необходимо определить, какое вещество будет в недостатке. По нему можно рассчитать объем выделившегося водорода. Алгоритм вычисления массы конечного раствора
зависит от того, какое вещество окажется в избытке, поэтому отразить эту часть решения заранее невозможно. Алгоритм вычисления массы конечного раствора зависит от того, какое
вещество окажется в избытке. В большинстве задач на определение избытка-недостатка при растворении металла в растворе в недостатке оказывается именно металл. В этом случае
масса конечного раствора определяется очень просто:
Если же металл окажется в избытке, то его излишек не будет входить в состав конечного раствора, а опустится на дно сосуда.
Поэтому отразить весь алгоритм решения заранее невозможно.
Схематично алгоритм первой части решения будет иметь вид:
1. Определяем массу НС1 в 200 г 8% -ного исходного раствора.
2. Определяем количество веществ НС1 и А1.
3. Выберем за основу алюминий, и определим по уравнению реакции количество вещества НС1, которое необходимо для полного растворения всего (0,296 моль) алюминия.
Составляем пропорцию:
на 0,296 моль А1 должно расходоваться х моль НС1 (по условию)
на 2 моль А1 полностью расходуется 6 моль НС1 (но уравнению)

4 .Определим, какое вещество дано в недостатке.
n(НС1) дано по условию
0,888моль > 0,438 моль
В реакции участвует меньше НС1, чем необходимо для полного растворения А1, следовательно, НС1 дано в недостатке. В процессе реакции НС1 израсходуется полностью, а А1 расходуется не весь и часть его останется после реакции.
5. Рассчитаем по уравнению реакции объем (н.у.) выделившегося водорода. Для расчета используем НС1, т.к. это вещество взято в недостатке.
Составляем пропорцию:
0,438 моль НС1 дают х л Н2 (по условию)
6 моль НС1 дают 67,2 л Н2 (по уравнению)
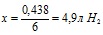
6. Определим массу выделившегося Н2 по алгоритму:
7. Определяем массу раствора после реакции.
При определении массы конечного раствора нужно учитывать, что алюминий находился в избытке, и часть его осталась после реакции в неизменном виде. Не прореагировавший алюминий, очевидно, не входит в состав раствора и будет находиться на дне. Поэтому нам придется определить массу растворившегося А1. Это можно сделать по уравнению реакции, используя данные по НС1.
Составляем пропорцию:
х т А1 растворяются в 0,438 моль НС1 (по условию)
54 г А1 растворяются в 6 моль НС1 (по уравнению)
Теперь возможно определить массу конечного раствора:
mкон. р-ра = 200 + 3,95 – 0,44 = 203,51 г.
Ответ: объем выделившегося водорода — 4,9 л; масса конечного раствора 203,51 г.
Определение объема образовавшегося углекислого газа
Задача 7.
Определите объем выделившегося газа при взаимодействии 20,0 г карбоната кальция с избытком азотной кислоты.
Решение:
Несмотря на то, что в условии говориться об избытке азотной кислоты, данная задача не относится к типу «на определение избытка-недостатка». В условии указана масса только одного из участников реакции (СаСО3). Указание на избыток другого участника (НNO3) показывает, что карбонат кальция расходуется полностью и объем выделившегося газа необходимо считать именно по СаСО3.
Определим объем образовавшегося углекислого газа из пропорции:
20 г А1 дают х л СО2 (по условию)
100 г А1 дают 22,4 л СО2 (по уравнению)
Ответ: V(CO2) = 4,
Задания 28. Расчеты объемных отношений газов при химической реакции. Тепловой эффект.
В результате реакции, термохимическое уравнение которой
выделилось 1452 кДж теплоты. Вычислите массу образовавшейся при этом воды (в граммах). (Запишите число с точностью до целых.)
Ответ: 108
Пояснение:
Из уравнения реакции следует, что при образовании 2 моль воды выделяется 484 кДж теплоты. У нас же выделилось 1452 кДж теплоты. Составим пропорцию
2 моль H2O — 484 кДж
x моль H2O — 1452 кДж
2 : x = 484 : 1452
x = 2 ∙ 1452 /484 = 6
т.е. n(H2O) = 6 моль, следовательно:
При взаимодействии оксида серы (IV) с 5,6 л (н.у.) кислорода в соответствии с уравнением
выделилось 19 кДж теплоты. Определите тепловой эффект реакции. (Запишите число с точностью до целых.)
Ответ: 76
Пояснение:
Рассчитаем количество вещества кислорода:
Т.е. при взаимодействии 0,25 моль кислорода с оксидом серы (IV) выделяется 19 кДж теплоты. Из представленного в условии термохимического уравнения следует, что при взаимодействии 1 моль кислорода с оксидом серы выделяется количество теплоты равное Q (тепловой эффект реакции). Тогда справедлива пропорция:
0,25 моль кислорода — 19 кДж
1 моль кислорода — Q
Исходя из этой пропорции:
Таким образом, тепловой эффект реакции составляет 76 кДж.
В соответствии с термохимическим уравнением реакции
выделилось 786 кДж теплоты. Какой объем (н.у.) углекислого газа при этом образовался? (Запишите число с точностью до десятых.)
Ответ: 44,8
Пояснение:
В соответствии с термохимическим уравнением реакции при образовании 1 моль углекислого газа выделяется 393 кДж теплоты. В нашем же случае вместо этого выделилось 786 кДж теплоты. Обозначив искомое количество вещества углекислого газа равным х моль, можно записать пропорцию:
1 моль CO2 — 393 кДж теплоты
x моль CO2 — 786 кДж теплоты
Следовательно, справедливо уравнение:
Решая которое получаем:
Т.е. количество вещества углекислого газа при образовании которого выделяется 786 кДж теплоты составляет 2 моль.
Рассчитаем объем такого количества углекислого газа при н.у.:
V(CO2) = 2 моль ∙ 22,4 л/моль = 44,8 л
В соответствии с термохимическим уравнением реакции
выделилось 2406 кДж теплоты. Определите объем (н.у.) израсходованного кислорода в литрах. (Запишите число с точностью до десятых.)
Ответ: 134,4
Пояснение:
Согласно термохимическому уравнению при участии в реакции горения метана 2 моль кислорода выделяется 802 кДж теплоты. В нашем же случае выделяется количество теплоты равное 2406 кДж. Обозначив количество вещества кислорода необходимое для выделения 2406 кДж теплоты через х моль мы можем записать следующую пропорцию:
2 моль O2 — 802 кДж теплоты
x моль O2 — 2406 кДж теплоты
Тогда, справедливо следующее уравнение:
2 ∙ 2406 = 802 ∙ x
Решая которое находим ,что:
Таким образом, количество вещества кислорода равно 6 моль. Рассчитаем его объем:
V(O2) = 6 ∙ 22,4 = 134,4 л.
Вычислите количество теплоты, которое потребуется для получения 25 г железа согласно уравнению реакции
(Запишите число с точностью до целых.)
Ответ: 6
Пояснение:
Рассчитаем количество вещества железа:
n(Fe) = m(Fe)/M(Fe) = 25/56 = 0,4464 моль,
Согласно термохимическому уравнению при образовании 2 моль металлического железа поглощается 27 кДж теплоты. Пусть количество поглощаемой в результате образования 0,4464 моль железа равно х кДж. Тогда можно записать пропорцию:
2 моль Fe — 27 кДж
0,4464 моль Fe — x кДж
Следовательно, справедливо уравнение:
2 ∙ x = 0,4464 ∙ 27
Таким образом, количество теплоты, которое необходимо для получения 25 г железа равно 6 кДж.
Вычислите объем сгоревшего согласно уравнению реакции
ацетилена, если при этом выделилось 67,5 кДж теплоты. (Запишите число с точностью до сотых.)
Ответ: 1,12
Пояснение:
Согласно термохимическому уравнению при сгорании 2 моль ацетилена выделяется 2700 кДж теплоты. В нашем же случае выделилось 67,5 кДж. Пусть, количество вещества ацетилена, которое сгорело при этом равно х моль. Таким образом можно записать пропорцию:
x моль — 67,5 кДж
2 ∙ 67,5 = 2700 ∙ x
Таким образом, количество вещества ацетилена равно 0,05 моль. Рассчитаем его объем:
V(C2H2) = 0,05 моль ∙ 22,4 л/моль = 1,12 л
В результате реакции, термохимическое уравнение которой
выделилось 280 кДж теплоты. Вычислите массу глюкозы, которая окислилась в результате этой реакции. (Запишите число с точностью до целых.)
Ответ: 18
Согласно термохимическому уравнению при окислении 1 моль глюкозы выделяется 2800 кДж теплоты. В нашем же случае выделилось 280 кДж теплоты. Пусть количество глюкозы, которое окислилось при этом равно x моль. Тогда можно записать следующую пропорцию:
1 моль глюкозы – 2800 кДж теплоты
x моль глюкозы – 280 кДж теплоты
Следовательно, справедливо уравнение:
1 ∙ 280 = 2800 ∙ x
Решая которое находим, что:
x = 0,1 моль, т.е. количество глюкозы составляет 0,1 моль. Рассчитаем ее массу:
Какое количество вещества аммиака вступает в реакцию в соответствии с термохимическим уравнением
если в результате реакции выделилось 634 кДж теплоты? (Запишите число с точностью до целых.)
Ответ: 2
Пояснение:
Согласно термохимическому уравнению при окислении 4 моль аммиака выделяется 1268 кДж теплоты. В нашем же случае выделилось 634 кДж теплоты. Обозначим количество вещества аммиака, которое при этом окислилось как x моль. Тогда можно записать пропорцию:
4 моль аммиака – 1268 кДж
x моль аммиака – 634 кДж
Следовательно, справедливо уравнение:
4 ∙ 634 = 1268 ∙ x
Решая которое находим, что:
x = 2, т.е. количество вещества аммиака составляет 2 моль.
В соответствии с термохимическим уравнением реакции
получено 1400 кДж теплоты. Какая масса (в граммах) глюкозы при этом окислилась? (Запишите число с точностью до целых.)
Ответ: 90
Пояснение:
Согласно термохимическому уравнению при окислении 1 моль глюкозы выделяется 2800 кДж теплоты. В нашем же случае выделилось 1400 кДж теплоты. Пусть количество глюкозы, которое окислилось при этом равно x моль. Тогда можно записать следующую пропорцию:
1 моль глюкозы – 2800 кДж теплоты
x моль глюкозы – 1400 кДж теплоты
Следовательно, справедливо уравнение:
1 ∙ 1400 = 2800 ∙ x
x = 0,5, т.е. количество вещества глюкозы для получения 1400 кДж тепла составляет 0,5 моль. Рассчитаем ее массу:
В соответствии с термохимическим уравнением реакции
выделилось 240 кДж теплоты. Определите массу полученного оксида магния. (Запишите число в точностью до целых.)
Ответ: 16
Пояснение:
Согласно термохимическому уравнению при образовании 2 моль оксида магния выделяется 1200 кДж теплоты. В нашем же случае выделилось 240 кДж теплоты. Пусть количество оксида магния, образовавшегося при этом равно x моль. Тогда можно записать пропорцию:
2 моль MgO – 1200 кДж
x моль MgO – 240 кДж
Следовательно, справедливо уравнение:
2 ∙ 240 = 1200 ∙ x
Решая которое находим, что:
x = 0,4, т.е. при выделении 240 кДж теплоты количество вещества образовавшегося оксида магния составляет 0,4 моль. Тогда его масса равна:
m(MgO) = n(MgO) ∙ M(MgO) = 0,4 ∙ 40 = 16 г
В ходе реакции, термохимическое уравнение которой
было затрачено 450 кДж теплоты. Определите объем (н.у.) получившегося при этом газа. (Запишите число с точностью до целых.)
Ответ: 56
Пояснение:
Выделившийся газ – CO2.
В соответствии с термохимическим уравнением при образовании одного моля CO2 поглощается 180 кДж теплоты. В нашем же случае поглощено 450 кДж теплоты. Обозначив количество вещества углекислого газа, образовавшегося при этом как x моль, можно записать следующую пропорцию:
1 моль CO2 – 180 кДж
x моль CO2 – 450 кДж
Следовательно, справедливо уравнение:
x = 2,5, т.е. количество вещества углекислого газа составляет 2,5 моль. Рассчитаем его объем:
В соответствии с термохимическим уравнением реакции
образовалось 168 г железа. Какое количество теплоты при этом выделилось? (Запишите число с точностью до целых.)
Ответ: 1110
Пояснение:
Рассчитаем количество вещества железа с массой 168 г:
n(Fe) = m(Fe)/M(Fe) = 168/56 = 3 моль,
В соответствии с термохимическим уравнением реакции при образовании 9 моль металлического железа выделяется 3330 кДж. В нашем же случае образуется 3 моль железа. Обозначив количество теплоты выделившейся при этом как x кДж можно составить пропорцию:
9 моль Fe — 3330 кДж
3 моль Fe — x кДж
тогда справедливо уравнение:
Таким образом, количество теплоты выделяющееся при образовании 168 г металлического железа составляет 1110 кДж.
Определите количество теплоты, которое выделится при взаимодействии 280 г негашеной извести с водой в соответствии с термохимическим уравнением реакции
(Запишите число с точностью до целых.)
Ответ: 324
Пояснение:
Негашеная известь — тривиальное название оксида кальция CaO. Рассчитаем его количество вещества, зная массу:
n(CaO) = 280 г/ 56 г/моль = 5 моль,
В соответствии с термохимическим уравнением реакции при взаимодействии с водой 1 моль CaO выделяется количество теплоты равное 64,8 кДж. В нашем же случае в реакции принимает участие 5 моль оксида кальция, в связи с чем мы можем записать следующую пропорцию:
1 моль CaO — 64,8 кДж
5 моль CaO — x кДж
Следовательно, справедливо уравнение:
Решая которое находим, что:
Таким образом, количество теплоты, которое выделится при взаимодействии 280 г негашеной извести водой составляет 324 кДж.
В результате реакции, термохимическое уравнение которой
выделилось 6620 кДж теплоты. Определите массу образовавшегося оксида железа (III). (Запишите число с точностью до целых.)
Ответ: 640
Пояснение:
В соответствии с термохимическим уравнением реакции при образовании 2 моль Fe2O3 выделяется 3310 кДж теплоты. В нашем же случае, выделилось 6620 кДж теплоты. Пусть количество вещества Fe2O3, образовавшегося при этом составляет x моль. Тогда можно записать следующую пропорцию:
Следовательно, справедливо уравнение:
2 ∙ 6620 = x ∙ 3310
Решая которое находим, что:
Таким образом, количество вещества Fe2O3 образовавшееся при этом составляет 4 моль. Следовательно масса образовавшегося Fe2O3 составляет:
При образовании 560 мл (н.у.) газообразного аммиака в соответствии с уравнением
выделилось 1,15 кДж теплоты. Чему равен тепловой эффект этой реакции? (Запишите число с точностью до целых.)
Ответ: 92
Пояснение:
Посчитаем какое количество вещества содержится в 560 мл газообразного аммиака. Прежде всего переведем его объем из мл в л:
Теперь, зная, что 1 моль любого газа при н.у. занимает объем равный 22,4 л, можно рассчитать количество вещества аммиака:
Из условия задания следует, что при образовании 0,025 моль (0,56 л) аммиака выделилось 1,15 кДж теплоты. В термохимическом же уравнении реакции фигурирует количество вещества аммиака равное 2 моль (коэффициент 2 перед NH3) и при этом выделяется количество тепла, равное Q (тепловой эффект реакции). Таким образом, мы можем записать следующую пропорцию:
0,025 моль — 1,15 кДж
Следовательно справедливо уравнение:
0,025 ∙ Q = 2 ∙ 1,15 кДж
Решая которое находим, что:
Т.е. тепловой эффект реакции равен 92 кДж.
В соответствии с термохимическим уравнением реакции
восстановили 464 г железной окалины. Какое количество теплоты при этом выделилось? (Запишите число с точностью до целых.)
Ответ: 2220
Пояснение:
Рассчитаем количество вещества железной окалины массой 464 г:
В соответствии с термохимическим уравнением реакции при восстановлении 3 моль Fe3O4 выделяется 3330 кДж теплоты. Пусть при восстановлении 2 моль Fe3O4 выделяется x кДж теплоты. Тогда можно составить следующую пропорцию:
Следовательно, справедливо уравнение:
Решая которое, получаем, что:
Таким образом, количество теплоты, выделившейся при восстановлении 464 г железной окалины составляет 2220 кДж.
В соответствии с термохимическим уравнением реакции
выделилось 2406 кДж теплоты. Определите объем (н.у.) израсходованного кислорода. (Запишите число с точностью до десятых.)
Ответ: 134,4
Пояснение:
В соответствии с термохимическим уравнением реакции при реакции с метаном 2 моль кислорода выделяется 802 кДж. В нашем же случае выделилось 2406 кДж теплоты. Пусть количество вещества израсходованного при этом кислорода составляет x моль. Тогда можно записать пропорцию:
2 моль O2 – 802 кДж
x моль O2 – 2406 кДж
Следовательно, справедливо уравнение:
2 ∙ 2406 = 802 ∙ x
Т.е. количество вещества кислорода составляет 6 моль. Найдем его объем:
В соответствии с термохимическим уравнением реакции
получено 422,2 кДж теплоты. Какой объем (н.у.) кислорода при этом израсходован? (Запишите число с точностью до целых.)
Ответ: 24
Пояснение:
В соответствии с термохимическим уравнением при израсходовании на горение угля 1 моля кислорода выделяется 393 кДж теплоты. В нашем же случае выделяется 422,2 кДж. Пусть при выделении такого количества теплоты расходуется x моль кислорода. Тогда, мы можем записать пропорцию:
1 моль O2 – 393 кДж
x моль O2 – 422,2 кДж
Следовательно, справедливо уравнение:
1 ∙ 422,2 = 393 ∙ x
Решая которое находим, что:
т.е. количество вещества израсходованного кислорода составляет 1,0743 моль. Рассчитаем его объем:
Какой объем (н.у.) кислорода потребуется для получения 5600 кДж теплоты в соответствии с термохимическим уравнением реакции
(Запишите число с точностью до десятых.)
Ответ: 268,8
Пояснение:
Исходя из термохимического уравнения:
6 моль O2 — 2800 кДж теплоты
В нашем же случае должно выделиться 5600 кДж. Пусть количество вещества кислорода необходимое для выделения такого количества тепла составляет x моль. Тогда справедлива пропорция:
6 моль O2 — 2800 кДж теплоты
x моль O2 — 5600 кДж теплоты
Следовательно, верным является уравнение:
6 ∙ 5600 = 2800 ∙ x
Таким образом, количество вещества кислорода, которое должно принять участие в окислении глюкозы для выделения 5600 кДж теплоты, составляет 12 моль. Рассчитаем объем такого количества кислорода при н.у.:
При сжигании ацетилена в соответствии с термохимическим уравнением реакции
выделилось 186 кДж теплоты. Какой объем (н.у.) кислорода затрачен на сжигание ацетилена? (Запишите число с точностью до десятых.)
Ответ: 22,4
Пояснение:
Из термохимического уравнения реакции следует, что когда в реакции принимает участие 5 моль O2 выделяется 930 кДж теплоты.
В нашем же случае выделяется 186 кДж теплоты. Пусть количество вещества кислорода, израсходованного при этом, составляет x моль. Тогда мы можем записать следующую пропорцию:
5 моль O2 – 930 кДж
x моль O2 – 186 кДж
Следовательно, справедливо уравнение:
Решая которое находим, что:
Таким образом, количество вещества кислорода составляет 1 моль. Найдем его объем:
В соответствии с термохимическим уравнением реакции
выделилось 2580 кДж теплоты. Определите количество вещества оксида азота(IV), вступившего в реакцию. (Запишите число с точностью до целых.)
Ответ: 40
Пояснение:
Из термохимического уравнения реакции следует, что когда в реакции принимает участие 4 моль NO2 выделяется 258 кДж теплоты.
В нашем же случае выделяется 2580 кДж теплоты. Пусть количество вещества оксида азота (IV), прореагировавшего при этом, составляет x моль. Тогда мы можем записать следующую пропорцию:
4 моль NO2 – 258 кДж
x моль NO2 – 2580 кДж
Следовательно, справедливо уравнение:
4 ∙ 2580 = x ∙ 258
Решая которое находим, что:
Таким образом, количество вещества оксида азота (IV) составляет 40 моль.
Определите объём газообразного продукта (в литрах), который получается при взаимодействии 1 л водорода с избытком хлора. Объёмы газов измерены при одинаковых условиях. (Запишите число с точностью до целых.)
Ответ: 2
Пояснение:
Запишем уравнение реакции взаимодействия водорода с хлором:
Одним из следствий закона Авогадро является то, что объемы прореагировавших и образовавшихся газов относятся друг к другу точно так же, как и коэффициенты перед этими газообразными веществами в уравнении реакции. Для газообразных водорода и хлороводорода, применительно к нашей реакции, мы можем записать что:
V(HCl) = V(H2) ∙ k(HCl)/k(H2) = 1 л ∙ 2/1 = 2 л
Определите количество теплоты, которое выделяется при окислении серы кислородом взятым в объёме 100,8 л (н.у.) в соответствии с термохимическим уравнением реакции
(Запишите число с точностью до целых.)
Ответ: 1341
Определите количество теплоты, которое выделится при обжиге 720 г FeS2 согласно термохимическому уравнению реакции
(Запишите число с точностью до целых.)
Ответ: 4965
Вычислите количество выделившейся теплоты, если в реакцию вступает 3,5 моль кислорода в соответствии с термохимическим уравнением реакции
(Запишите число с точностью до целых.)
Ответ: 903
Какое количество теплоты выделится при взаимодействии 3,6 моль кремния с фтором в соответствии с термохимическим уравнением реакции
(Запишите число с точностью до целых.)
Ответ: 5814
В реакцию, термохимическое уравнение которой
вступило 88 г углекислого газа. Какое количество теплоты выделится при этом? (Запишите число с точностью до целых.)
Вычисление количества вещества, массы или объема вещества по количеству веществ, массе или объему одного из реагентов или продуктов реакции
Основой для проведения количественных расчётов в химии является закон сохранения массы. Согласно этому закону масса реагентов равна массе продуктов реакции.
Отсюда следует, что для любой химической реакции массы реагентов и продуктов реакции относятся между собой как молярные массы веществ, умноженные на их стехиометрические коэффициенты.
Для расчёта по химическим уравнениям можно использовать два эквивалентных способа: через количество вещества или через пропорцию. Подчеркнём ещё раз: официального запрета на использование метода пропорций при решении задач на ОГЭ и ЕГЭ нет!
Для определения массы (или количества вещества) продуктов реакции или исходных веществ по уравнениям химических реакций вначале составляют уравнение химической реакции и устанавливают стехиометрические коэффициенты; затем определяют молярную массу, массу и количество вещества известных реагентов химической реакции; составляют и решают пропорцию, в которую в зависимости от условий задачи вводят числовые значение величин: молярные массы, массы, количества веществ или их объёмы (для газов).
При этом в одном столбце пропорций должны находиться одинаковые характеристики вещества с одной и той же размерностью.
Пример 1. Масса железа, вступившего в реакцию с 6 моль хлора, равна _________ г. (Ответ запишите с точностью до целого числа.)
Решение. Составляем уравнение химической реакции:
Из этого уравнения следует, что 3 моль Cl2 реагируют с 2 моль Fe, т. е.:
Определяем массу железа:
Пример 2. Масса нитрида лития, образовавшегося в результате его реакции с азотом объёмом 8,96 л, равна_______________ г.
Решение. Составляем уравнение химической реакции:
Определяем количество вещества азота, вступившего в реакцию:
Из уравнения реакции следует, что из 1 моль N2 образуется 2 моль Li3N, т. е.:
Определим массу Li3N:
Пример 3. Объём углекислого газа, образовавшегося в результате разложения карбоната магния количеством вещества 4 моль избытком соляной кислоты, равен________ л.
Решение. Составляем уравнение химической реакции:
Из этого уравнения следует, что количество вещества углекислого газа и карбоната магния равны между собой, т. е. n(CO2) = 4 моль.
Пример 4. Объём водорода, который выделится при растворении 16,8 г железа в избытке разбавленной соляной кислоты, равен _________ л.
Решение. Составляем уравнение химической реакции:
Определим количество вещества железа:
Количество вещества железа и водорода в данном уравнении реакции равны между собой. Следовательно, количество вещества водорода также равно 0,3 моль.
Вычислим объём водорода:
Пример 5. Масса осадка, который образуется в результате взаимодействия 40,0 г хлорида кальция с избытком карбоната натрия, равна _________г.
Решение. Составляем уравнение реакции:
Согласно уравнению химической реакции составим пропорцию и решим её:
Пример 6. 250 г раствора нитрата серебра смешали с избытком раствора йодида калия. Выпал осадок массой 11,75 г. Вычислите массовую долю нитрата серебра в исходном растворе.
Элементы ответа (допускаются иные формулировки ответа, не искажающие его смысла)
1) Составлено уравнение химической реакции:
2) По массе осадка йодида серебра рассчитано его количество вещества, а затем в соответствии с уравнением реакции — количество вещества и масса нитрата серебра, содержащегося в исходном растворе:
Из уравнения реакции следует, что n(AgI) = n(AgNO3) = 0,05 моль, тогда:
3) Вычислена массовая доля нитрата серебра в исходном растворе:
| Критерии оценивания | Баллы |
| Ответ правильный и полный, включает все названные элементы | 3 |
| Правильно записаны два первых элемента из названных выше | 2 |
| Правильно записан один из названных выше элементов (1-й или 2-й) | 1 |
| Все элементы ответа записаны неверно | 0 |
| Максимальный балл | 3 |
Тренировочные задания
1. К 300 г раствора нитрата бария прибавили избыток раствора сульфата натрия. Масса выпавшего осадка составила 23,3 г. Определите концентрацию соли в исходном растворе.
2. К 150 г раствора сульфата натрия прибавили избыток раствора хлорида бария. Масса выпавшего осадка составила 23,3 г. Определите концентрацию соли в исходном растворе.
3. К 300 г раствора силиката натрия прибавили избыток раствора нитрата кальция. Масса выпавшего осадка составила 12,0 г. Определите концентрацию соли в исходном растворе.
4. К 150 г раствора карбоната калия прибавили избыток раствора соляной кислоты. При этом выделился газ объёмом 3,36 л (н. у.). Определите концентрацию соли в исходном растворе.
5. К 250 г раствора гидрокарбоната натрия прибавили избыток раствора бромоводородной кислоты. При этом выделился газ объёмом 5,6 л. Определите концентрацию соли в исходном растворе.
6. К 50 г раствора карбоната натрия прибавили избыток раствора хлорида бария. Масса выпавшего осадка составила 7,88 г. Определите концентрацию соли в исходном растворе.
7. К 200 г раствора хлорида бария прибавили избыток раствора карбоната калия. Масса выпавшего осадка составила 7,88 г. Определите концентрацию соли в исходном растворе.
8. К 200 г раствора хлорида железа (II) прибавили избыток раствора гидроксида калия. Масса выпавшего осадка составила 18,0 г. Определите концентрацию соли в исходном растворе.
9. К 400 г раствора нитрата свинца прибавили избыток раствора йодида натрия. Масса выпавшего осадка составила 23,05 г. Определите концентрацию соли в исходном растворе.
10. К 300 г раствора йодида натрия прибавили избыток раствора нитрата свинца. Масса выпавшего осадка составила 23,05 г. Определите концентрацию соли в исходном растворе.
11. Определите массу осадка, который выпадет при взаимодействии 150 г 14,8%-ного раствора хлорида кальция с избытком раствора карбоната натрия.
12. Определите объём газа (н. у.), который выделится при взаимодействии 120 г 8,8%-ного раствора карбоната натрия с избытком раствора соляной кислоты.
13. Определите массу соли, которая выпадет в осадок при взаимодействии 140 г 13,5%-ного раствора нитрата цинка с избытком раствора сульфида натрия.
14. Определите массу осадка, который выделится при взаимодействии 200 г 18,8%-ного раствора нитрата меди с избытком раствора сульфида натрия.
15. Определите массу осадка, который выпадет при взаимодействии 200 г 6,1%-ного раствора силиката натрия с избытком раствора хлорида цинка.
16. Определите массу осадка, который выделится при взаимодействии 200 г 12,7%-ного раствора хлорида железа (II) с избытком раствора сульфида натрия.
17. Определите массу осадка, который выделится при взаимодействии 50 г 17%-ного раствора нитрата серебра с избытком раствора бромида калия.
18. Определите массу осадка, который образуется при взаимодействии 200 г 6,1%-ного раствора силиката натрия с избытком раствора нитрата кальция.
19. Определите массу осадка, который образуется при взаимодействии 50 г 5,8%-ного раствора хлорида магния с избытком раствора фосфата натрия.
20. Определите объём газа, который выделится при взаимодействии 200 г 6,9%-ного раствора карбоната калия с избытком раствора соляной кислоты.
21. Оксид фосфора (V) массой 21,3 г растворили в растворе гидроксида калия, в результате чего был получен раствор средней соли массой 500 г. Определите концентрацию фосфата калия в конечном растворе.
22. Раствор хлорида железа (II) полностью прореагировал со 120 г раствора гидроксида натрия, в результате чего образовалось 6,0 г осадка. Определите массовую долю гидроксида натрия в исходном растворе.
23. Какой объём аммиака (н. у.) может полностью прореагировать со 150 г 20%-ного раствора серной кислоты с образованием средней соли?
24. В 200 г 20%-ного раствора соляной кислоты растворили магний до прекращения выделения газа. Определите объём выделившегося при этом водорода (н. у.).
25. Аммиак объёмом 10 л (н. у.) пропустили через раствор серной кислоты с массовой долей 8% до образования средней соли. Определите массу исходного раствора.
26. Определите объём сероводорода (н. у.), который необходимо пропустить через 130 г 6%-ного раствора хлорида меди (II) до полного осаждения сульфида меди (II).
27. Сероводород объёмом 3,36 л (н. у.) пропустили через раствор гидроксида натрия, в результате чего получили 180 г раствора сульфида натрия. Определите массовую долю соли в полученном растворе.
28. Алюминий массой 8,1 г может нацело прореагировать с 250 г раствора серной кислоты. Определите массовую долю серной кислоты в исходном растворе.
29. К 250 г раствора нитрата серебра добавили раствор хлорида калия до прекращения выделения осадка, масса которого составила 14,35 г. Определите массовую долю нитрата серебра в исходном растворе.
30. К 300 г 5%-ного раствора хлорида магния добавили избыток раствора фосфата калия. Вычислите массу выпавшего при этом осадка.
http://scienceforyou.ru/reshenie-realnyh-zadanij-egje-2016-goda/raschety-obemnyh-otnoshenij-gazov-pri-himicheskoj-reakcii-teplovoj-jeffekt
http://himi4ka.ru/ogje-2018-po-himii/urok-29-vychislenie-kolichestva-veshhestva-massy-ili-obema-veshhestva-po-kolichestvu-veshhestv-masse-ili-obemu-odnogo-iz-reagentov-ili-produktov-reakcii.html