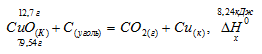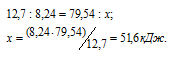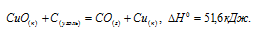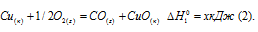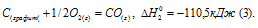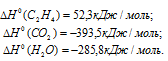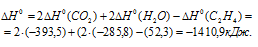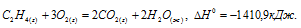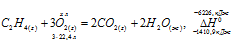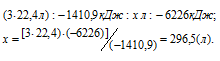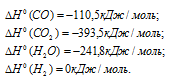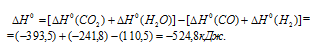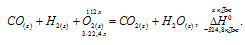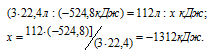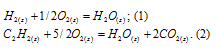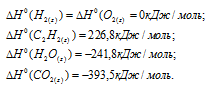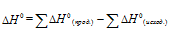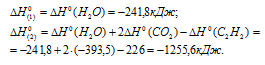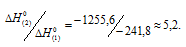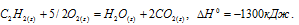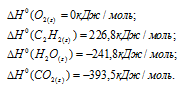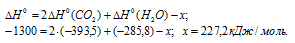Реакция фотосинтеза глюкозы протекает в соответствии с уравнением: 6СО2 + 6Н2О = С6Н12О6 + 6О2 — 2920 кДж. Определите объем
Ваш ответ
решение вопроса
Похожие вопросы
- Все категории
- экономические 43,296
- гуманитарные 33,622
- юридические 17,900
- школьный раздел 607,203
- разное 16,830
Популярное на сайте:
Как быстро выучить стихотворение наизусть? Запоминание стихов является стандартным заданием во многих школах.
Как научится читать по диагонали? Скорость чтения зависит от скорости восприятия каждого отдельного слова в тексте.
Как быстро и эффективно исправить почерк? Люди часто предполагают, что каллиграфия и почерк являются синонимами, но это не так.
Как научится говорить грамотно и правильно? Общение на хорошем, уверенном и естественном русском языке является достижимой целью.
Задания
№ 1. Ниже представлены два уравнения химической реакции процесса дыхания:
А) – аэробное дыхание в клетках организма,
В) – анаэробное дыхание (спиртовое брожение глюкозы).
A) С6Н12О6 + 6О2 ————> 6_______ + 6_______ + 36 АТФ
B) С6Н12О6 ————> 2_______ + 2_______ + 2АТФ
(этанол)
(a) Определите пропущенные вещества в уравнении химической реакции.
A. СО2; О2
B. H2O; СО2
C. H2O; О2
D. C2H5OH; СО2
(b) Заполните таблицу.
Критерии
Анаэробное дыхание
Аэробное дыхание
Место и Условие, при котором
происходит данный процесс
№2.
В процессе энергетического обмена произошло расщепление 7 моль глюкозы, из которых полному расщеплению подверглось только 2. Определите:
а) сколько моль молочной кислоты при этом образовалось;
б) сколько АТФ при этом синтезировано;
в) сколько израсходовано моль О2?
г) сколько моль СО2 при этом образовалось;
№3 Дайте определения следующим понятиям:
Ультрафильтрация- Абсорбция- Реабсорбция-
Первичная моча- Вторичная моча- Урология-
Энергетика химических реакций. Тепловой эффект реакции
Задача 288.
При восстановлении 12,7г оксида меди (II) углем (с образованием СО) поглощается 8,24кДж. Определить 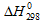
Решение:
Уравнение реакции имеет вид:
Находим тепловой эффект реакции восстановления оксида меди (II) углем из пропорции:
Значит, 
Обозначим искомую величину через x, запишем термохимическое уравнение образования CuO:
Из уравнения (20 и (3) можно получить уравнение (4). Для этого нужно вычесть уравнение (2) из уравнения (3), получим:
Сравнивая уравнение (1) и (4), получим:
Ответ: 162,1 кДж/моль.
Задача 289.
При полном сгорании этилена (с образованием жидкой воды) выделилось 6226 кДж. Найти объем вступившего в реакцию кислорода (условия нормальные).
Решение:
Уравнение реакции горения этилена:
Учитывая данные значения теплот образования веществ, находим 
Запишем данные задачи в уравнение, получим:
Рассчитаем объём кислорода, вступившего в реакцию с этиленом из пропорции:
Ответ: V(O2)=296,5 л.
Задача 290.
Водяной газ представляет собой смесь равных объемов водорода и оксида углерода (II). Найти количество теплоты, выделившейся при сжигании 112л водяного газа, взятого при нормальных условиях.
Решение:
Уравнение реакции сжигания водяного газа имеет вид:
Рассчитаем теплоту, которая выделяется при сжигании водяного газа, используя следствие из закона Гесса:
Следовательно, термохимическое уравнение будет иметь вид:
Рассчитаем теплоту, выделяющуюся при сжигании 112 л водяного газа из пропорции:
Ответ: Q = -1312 кДж.
Задача 291.
Сожжены с образованием Н2О(г) равные объемы водорода и ацетилена, взятых при одинаковых условиях. В каком случае выделится больше теплоты? Во сколько раз?
Решение:
Уравнения реакций сгорания водорода и ацетилена:
Стандартные теплоты образования исходных веществ и продуктов реакций находим из таблицы, получим:
Для расчета теплоты, которая будет выделяться при сгорании водорода и ацетилена, используем следствие из закона Гесса:
Рассчитаем, во сколько раз больше выделяется теплоты при сгорании ацетилена:
Таким образом, при сгорании равных объемов водорода и ацетилена, взятых при одинаковых условиях в случае ацетилена выделится больше теплоты в 5,2 раза.
Ответ: При сжигании С2Н2 в 5,2 раза больше
Задача 292.
Определить 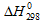
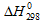
О2(г) и Н2О(ж) равно —1300кДж/моль, а 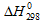
Решение:
Уравнение реакции горения ацетилена имеет вид:
Стандартные теплоты образования исходных веществ и продуктов реакций находим из таблицы, получим:
Обозначим искомую величину [

Уравнение реакции образования бензола имеет вид:
3C2H2 ⇔ C6H6, 
Находим 
http://znanija.org/biologiya/40815932.html
http://buzani.ru/zadachi/khimiya-glinka/1129-teplovoj-effekt-reaktsii-zadachi-288-292